 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
ACIZI CARBOXILICI
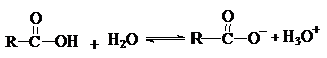
Clasificare si nomenclatura
Dupa numarul grupelor caboxil din molecula
acizi monocarboxilici
acizi dicarboxilici si policarboxilici
Dupa natura radicalului organic
Nomenclatura acizilor carboxilici
 I.U.P.A.C.
I.U.P.A.C.
sufixul -oic
Multi acizi organici au denumiri empirice intrate in uz, comune, care corespund originii (mai ales vegetale) sau proprietatilor lor.
HCOOH CH3COOH HOOC-COOH CH3-(CH2)3·COOH
Acid formic Acid acetic Acid oxalic Acid valerianic
(furnici) (acetum=otet) (macris) (valeriana)
CH3-(CH2)2·COOH C6H5-COOH HOOC(CH2)2-COOH
Acid butiric Acid benzoic Acid succinic
(grasime) (rasina de benzoe) (chihlimbar)
Dupa o alta nomenclatura se considera acizii organici ca produsi de substitutie formala a unui hidrogen din hidrocarburi cu o grupare caboxil.
CH3COOH C6H5COOH CH2=CH-COOH
Acid metan-carboxilic Acid benzen-carboxilic Acid etencarboxilic
Radicalii R-CO proveniti din acizi se numesc radicali "acil" si sunt utilizati la citirea altor compusi organici. Ionii proveniti din acizi (la ionizare) si din saruri schimba sufixul "oic" cu "oat" si astfel, carboxilul devine carboxilat, -COO-.
ACIZII MONOCARBOXILICI SATURATI (SI AROMATICI)
Metode de obtinere
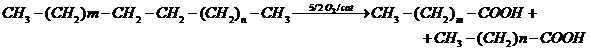 a. Metode oxidative. Oxidarea n-alcanilor cu C22-C36
prin barbotarea aerului in parafina, la 100-130oC, utilizand
drept catalizatori stearat de zinc sau de mangan, naftenat de cobalt sau
permanganat de potasiu.
a. Metode oxidative. Oxidarea n-alcanilor cu C22-C36
prin barbotarea aerului in parafina, la 100-130oC, utilizand
drept catalizatori stearat de zinc sau de mangan, naftenat de cobalt sau
permanganat de potasiu.
![]() Oxidarea catenei benzilice cu oxigen molecular,
urmata de tratare cu NaOBr sau cu KMnO4:
Oxidarea catenei benzilice cu oxigen molecular,
urmata de tratare cu NaOBr sau cu KMnO4:
![]() Oxidarea hidrocarburilor aromatice cu catena laterala cu KMnO4:
Oxidarea hidrocarburilor aromatice cu catena laterala cu KMnO4:
Oxidarea alchenelor (vezi alchene)
Oxidarea alcoolilor (vezi alcooli)
Oxidarea aldehidelor si cetonelor (vezi compusi carbonilici) .
![]() b. Metode de hidroliza. Prin hidroliza
derivatilor functionali ai acizilor caboxilici (dintre care
multi sunt produsi natuarali), rezulta acizi organici.
Reactia in mediu alcalin poarta numele de saponificare.
Nitrilii din seria alifatica rezulta usor din compusi
halogenati si cianuri alcaline (prin mecanism SN2) si pot fi
utilizati in acest scop.
b. Metode de hidroliza. Prin hidroliza
derivatilor functionali ai acizilor caboxilici (dintre care
multi sunt produsi natuarali), rezulta acizi organici.
Reactia in mediu alcalin poarta numele de saponificare.
Nitrilii din seria alifatica rezulta usor din compusi
halogenati si cianuri alcaline (prin mecanism SN2) si pot fi
utilizati in acest scop.
Clorura de benzil Benzonitril Acid fenilacetic
![]() Obtinerea acizilor aromatici prin
intermediul reactiei Sandmeyer are loc conform reactiilor:
Obtinerea acizilor aromatici prin
intermediul reactiei Sandmeyer are loc conform reactiilor:
Hidroliza esterilor naturali si sintetici conduce la acizi si alcooli . In prezenta de alcalii rezulta sapunuri (vezi esteri).
![]()
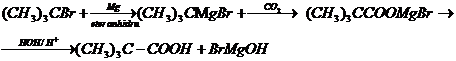 c.Obtinerea acizilor carboxilici prin sinteza. Acizii carboxilici rezulta din compusi
organometalici si dioxid de carbon ca saruri, din care se pun in
libertate prin tratare cu apa acidulata. Ca exemplu, obtinerea
acidului pivalic:
c.Obtinerea acizilor carboxilici prin sinteza. Acizii carboxilici rezulta din compusi
organometalici si dioxid de carbon ca saruri, din care se pun in
libertate prin tratare cu apa acidulata. Ca exemplu, obtinerea
acidului pivalic:
Alchenele aditioneaza oxid de carbon in prezenta Ni(CO)4 la 250-300oC si 100-200 at., formand intermediari ciclici, din care prin descompunere cu apa rezulta acizi caboxilici saturati (sinteza Reppe). La reactie pot participa si alcooli.:
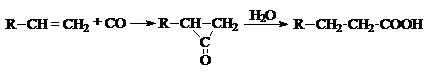
Acizii cicloalcancarboxilici se obtin pe baza reactiei Perkin jr. folosind un derivat dihalogenat (cu halogeni cu reactivitate diferita) si ester malonic monosodat. In reactie poate fi utilizat si un derivat monohalogenat si ester malonic sodat cu formarea acizilor carboxilici cu catena mai lunga
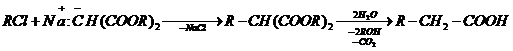
Sinteza anodica este utilizata la obtinerea acizilor superiori. Daca se supune sintezei acetatul de poatsiu si sarea de potasiu a esterului adipic rezulta acid capronic
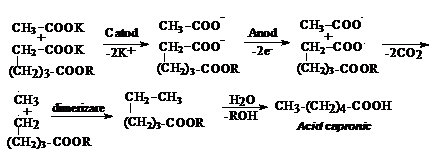
Structura. Unele proprietati ale carboxilului.
Grupa functionala caboxil -COOH, formal poate fi considerata ca fiind formata prin combinarea grupelor cabonil (> C=O) si hidroxil (-OH), legate la acelasi atom de carbon. Sau se poate considera ca rezulta dintr-un ortoacid, instabil, prin eliminare de apa. Rezulta o functie trivalenta reprezentata prin formulele I-III. Ca urmare grupa >C=O in carboxil nu este independenta (acizii dau putine reactii de aditie fata de aldehide si cetone) si nici grupa OH, pentru ca acizii caboxilici au tendinta de a ioniza spre deosebire de alcooli.
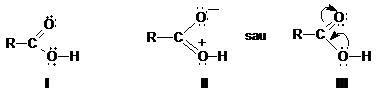
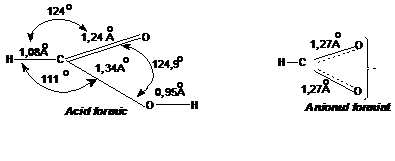
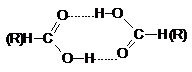
Aciditatea si constanta de aciditate
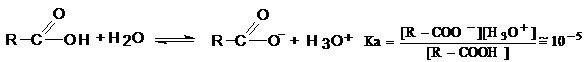
Constante de aciditate pentru unii acizi monocarboxilici
(date din literatura)
|
Acidul carboxilic |
Ka.10-5 |
|
Acidul formic Acidul acetic Acidul butiric Acidul caprilic Acidul fenilacetic Acidul benzoic |
Motive structurale care determina aciditatea carboxilului.
In anionul carboxilat rezultat prin deprotonare, conjugarea p-p este izovalenta.
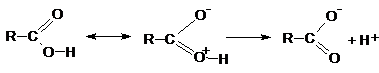
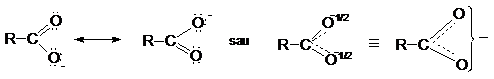
Masuratorile distantelor interatomice in anionul carboxilat confirma egalitatea legaturilor carbon-oxigen.
Efectul radicalului asupra aciditatii carboxilului
Grupele respingatoare de electroni (R ) micsoreaza aciditatea prin marirea sarcinii negative pe carboxilat si destabilizarea anionului (I).
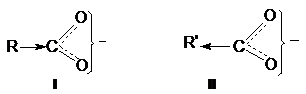
Grupele atragatoare de electroni (R' ) maresc aciditatea prin micsorarea sarcinii negative pe carboxilat (efect - I) si stabilizarea anionului (II). Acelasi efect se manifesta si in acidul nedisociat
Aciditatea acizilor aromatici (acid benzoic si acid benzoic substituit). Acidul benzoic este un acid mai tare decat acizii alifatici cu exceptia acidului formic.
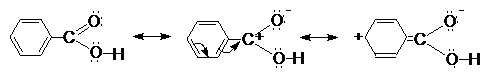
Substituentii respingatori de electroni (alchil) micsoreaza aciditatea, iar cei cu efect atragator de electroni maresc aciditatea (vezi efecte). Asa se explica de ce acidul p-nitrobenzoic este un acid tare (efect -I si efect de conjugare -E) iar acidul p-hidroxibenzoic (efecte -I si +E) este un acid mai slab in comparatie cu acidul benzoic. In acidul benzoic orto-substituit intervine efectul steric. Acizii benzoici orto-substituiti sunt acizi mai tari decat acidul benzoic.
punctele de fierbere ale acizilor nesolvatati sunt superioare
celor ale alcoolilor si aldehidelor, ceea ce se explica prin
existenta asociatiilor moleculare prin punti de hidrogen
(I).
Proprietati fizice. Termenii inferiori (C1-C11) ai seriei omoloage a acizilor monocarboxilici
saturati sunt substante lichide la temperatura obisnuita,
iar termenii superiori (incepand cu C12) sunt substante solide.
Temperaturile de topire si de fierbere cresc cu cresterea maselor
moleculare prezentand o alternanta; respectiv acizii cu numar
par de atomi de carbon se topesc mai sus decat acizii cu numar impar,
invecinati. In aceeasi serie omoloaga temperatura de fierbere
are o crestere regulata. Termenii superiori nu pot fi distilati
in vid pentru ca se descompun sub punctul de fierbere. Termenii inferiori
(C1-C4) sunt solubili in apa; solubilitatea scade cu cresterea masei
moleculare. Acizii superiori au solubilitate limitata in apa si
sunt solubili in solventi organici.

a).Punctele de topire in seria omoloaga a b).Temperaturile de fierbere ale acizilor, acizilor
acizilor monocarboxilici saturati liniari alcoolilor si aldehidelor cu acelasi numar de atomi
(acizi grasi) C1 . C20. de carbon in molecula, saturati, monofunctionali
Asa se explica de ce pentru o anumita concentratie
acizii C6 si in special C12-C18 formeaza micelii coloidale
|
Nr. at. C |
5 6 7 8 9 10 11 12 13 14 15 16 17 18 |
|
Solubilita-te in apa g/100 ml la 20oC |
0,968 0,068 0,015 0,0055 0,0020 0,00072 0,00029 4,97 0,244 0,026 0,0093 0,0033 0,0015 |
![]() Punctele de topire depind in mare masura si de
asezarea moleculelor in cristal. Moleculele acizilor cu catene mai lungi
adopta o configuratie plana cu asezarea atomilor in
zig-zag.
Punctele de topire depind in mare masura si de
asezarea moleculelor in cristal. Moleculele acizilor cu catene mai lungi
adopta o configuratie plana cu asezarea atomilor in
zig-zag. 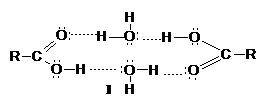
In cristal, catenele se dispun paralel prezentand impachetari cristaline cu unghiuri caracteristice si planuri de clivaj (datorita faptului ca radicalii R se atrag numai prin forte Van der Waals).
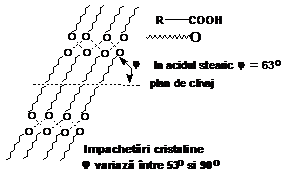
Densitatea acizilor carboxilici saturati este cu atat mai mare cu cat masa moleculara este mai mare. Acizii ciclici au densitate mai mare decat cei aciclici saturati.
Caracteristici spectrale. In UV, acizii carboxilici avand cromoforul >C=O prezinta benzi caracteristice ca si compusii carbonilici.
In IR, datorita conjugarii, se produc modificari fundamentale in natura legaturilor C=O si C-OH din grupa COOH si ca urmare apar proprietati noi, caracteristice grupei carboxil. Astfel frecventa nC=O apare la 1770-1790 cm-1 in acizii neasociati si la 1710-1740 cm-1 la dimeri; in ionul carboxilat nC=O = 1550-1600 cm-1. carbonilice.
Cu ajutorul spectrelor IR pot fi diferentiati acizii cu catena normala (CH3COOH 1721 cm-1) si cei tertiari (CH3)3-COOH 1704 cm-1).
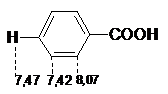 In spectrele RMN, protonul
carboxilic, dezecranat, la molecule asociate determina absorbtii la
campuri magnetice mai mici, la care corespund valori ale lui d > 10 ppm
(d 10-14
ppm). Protonii din pozitiile a, dezecranati de vecinatatea campului, apar la d 2-3
ppm, functie de structura. In acidul benzoic grupa COOH
influenteaza in mod diferit protonii din nucleu, acestia
prezentand deplasari chimice caracteristice.
In spectrele RMN, protonul
carboxilic, dezecranat, la molecule asociate determina absorbtii la
campuri magnetice mai mici, la care corespund valori ale lui d > 10 ppm
(d 10-14
ppm). Protonii din pozitiile a, dezecranati de vecinatatea campului, apar la d 2-3
ppm, functie de structura. In acidul benzoic grupa COOH
influenteaza in mod diferit protonii din nucleu, acestia
prezentand deplasari chimice caracteristice.
CH3-COOH CH3-CH2-COOH (CH3)2CH-COOH
2,08 1,16 2,36 1,21 2,56 ppm
Propietati chimice
Reactivitatea grupei carboxil poate fi reprezentata prin schema:
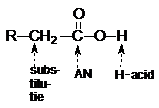
Formarea sarurilor. Acizii organici reactioneaza cu hidroxizi, oxizi bazici, carbonati si amine si formeaza saruri. La acidulare cu acizi minerali, sarurile ionizate pun in libertate acizii carboxilici corespunzatori. Sarurile acizilor carboxilici superiori au o solubilitate limitata in apa (vezi agenti tensioactivi si sapunuri). Sarurile cu aminele, in functie de bazicitate, disociaza reversibil.Acizii carboxilici sunt rezistenti fata de acizii minerali. Astfel ca acidul acetic este dizolvant in reactiile care au loc in prezenta acidului cromic.Acizii carboxilici sunt rezistenti si stabili la incalzire pana la circa 200oC; ei pot fi distilati fara descompunere. La temperaturi mai ridicate, acizii si sarurile lor pot suferi fenomenul de descompunere, prin decarboxilare.
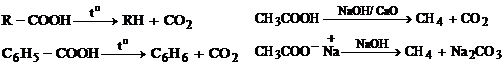
Reactia de decarboxilare este o substitutie electrofila (SE1) favorizata de prezenta in pozitia a a unor grupe cu efecte -I sau M care stabilizeaza carbanionul intermediar:
![]()
sau:
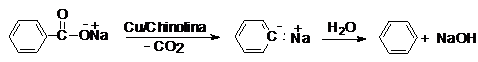
Decarboxilarea oxidativa (C.A.Grob - 1958), are loc in prezenta tetraacetatului de plumb cu formarea alchenelor, dupa urmatorul mecanism:
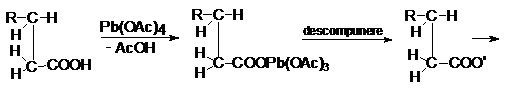
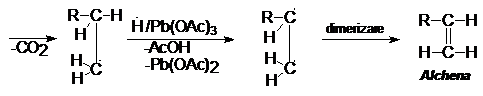
Sarurile de argint se decarboxileaza in prezenta bromului, reactie utilizata pentru marcarea cu carbon izotopic.
Decarboxilarea poate fi si un proces anodic. RCOOAg + Br2 → RBr + AgBr + CO2
Decarbonilarea. Reactia de decarbonilare a acizilor organici are loc in prezenta acidului sulfuric concentrat. Reactia sta la baza metodei de obtinere a CO in laborator.
![]()
Reducerea acizilor carboxilici se realizeaza cu LiAlH4, la 300oC si 325 at. Mai usor se reduc esterii (vezi esteri).
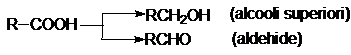
Reactii in pozitia a Radicalii hidrocarbonati din acizii carboxilici saturati dau reactii de substitutie declansata fotochimic, cu radiatii UV, sau catalitic. Astfel, acidul acetic conduce la un amestec de halogenacizi care se separa prin distilare. Reactia are aplicatii industriale.
![]()
Acizii monocarboxilici saturati importanti
Acidul formic, HCOOH, a fost descoperit in furnicile rosii in sec. XVII si in urzici. Se mai gaseste si in ace de brad si de pin. Este un lichid incolor, cu miros intepator, un iritant pentru piele si mucoase. Este un acid tare in comparatie cu omologii superiori. Acidul formic se obtine prin metoda M.Berthelot, 1855, avand la baza reactia dintre oxidul de carbon si hidroxidul de sodiu, la 200o C si 15 at, urmata de tratarea cu acid sulfuric, la 40oC.
![]()
In loc de NaOH se poate folosi lapte de var care asigura regenerarea NaOH.
![]()
Acidul formic obtinut prin acest procedeu se purifica prin distilare. In acidul formic grupa carbonil nefiind legata de un radical organic ci de hidrogen poate functiona ca o aldehida cu proprietati reducatoare, ceea ce se observa in reactia cu o solutie amoniacala de azotat de argint sau cu o solutie alcalina de permanganat de potasiu. Acidul formic este descompus de metalele din grupa platinei. De asemenea, este descompus de acidul sulfuric si de radiatiile UV.
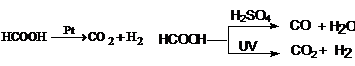
Sarurile acidului formic se descompun conform reactiilor:
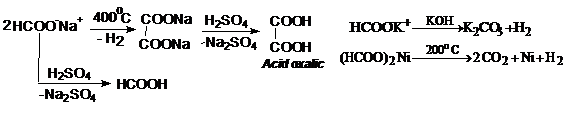
Ultima reactie este utilizata la hidrogenarea uleiurilor vegetale pentru obtinerea margarinei. Acidul formic are actiune antiseptica fiind activ fata de mucegaiuri si enzime; este conservant (0,15% si 1-2%) pentru legume murate si fructe. Este utilizat in tabacarie pentru decalcifierea pieilor si in industria textila ca mordant auxiliar.
Acidul acetic sau acidul etanoic, CH3COOH, este lichid (T.f. 118,5oC), cu miros intepator. Acidul acetic este o substanta polara (m = 1,73 D). Acidul acetic rezulta in concentratie de 3-15% prin fermentarea oxidativa a solutiilor etanolice cu ajutorul bacteriilor, microderma aceti, din aer. Metoda necesita in mediu de fermentatie compusi cu fosfor si azot ca hrana pentru bacterii. Industrial, acidul acetic rezulta pe cale de sinteza, prin oxidarea acetaldehidei, folosind acetatul de mangan drept catalizator, la 60oC. Rezulta acid acetic de concentratie 95-97%. Cu alti catalizatori se obtine un amestec de componente care se poate separa prin distilare. Rezulta la distilarea uscata a lemnului. Acidul acetic anhidru, obtinut prin rectificare, se numeste acid acetic glacial (se solidifica la rece, la +16,6oC) si este caustic. In cantitati mici acidul acetic este condiment si conservant (otet). Acetatul de calciu serveste la conservarea painii si branzei (0,4-1%). Acidul acetic este un bun solvent. Poate functiona ca mordant auxiliar in industria textila (acetat de aluminiu). Unele saruri sunt oxidanti (Pb(OAc)4). Acidul acetic poate fi materie prima pentru obtinerea acetonei. Acidul acetic poate participa la unele transformari cu importanta biochimica.
Acidul propionic sau propanoic, CH3CH2COOH, este un lichid incolor, solubil in apa, netoxic. Are actiune fungicida ca acid si ca sare de sodiu. Propionatii de natriu si de calciu sunt si buni antiseptici (pana la 0,2% in paine). Propionatul de calciu este un hemostatic. Acidul propionic se utilizeaza la obtinerea unor esteri ai celulozei.
Acidul butiric sau n-butanoic CH3-CH2-CH2-COOH, se gaseste in untul alimentar. Sintetic se obtine prin metoda "oxo" sau prin oxidarea butanalului. Se poate obtine si prin fermentatia oxidativa (cu bacterii) a glucozei. Acidul butiric este un lichid cu un miros respingator. Este component al grasimilor animale. Este utilizat la obtinerea unor esteri ai celulozei, in farmacie si mase plastice. Acidul izobutiric, (CH3)2CHCOOH, se gaseste in radacina de arnica si in uleiuri eterice, ca esteri. Acidul izovalerianic (CH3)2CH-CH2-COOH si alti izomeri se gasesc in radacina de valeriana officinalis (odolean) si Angelica archangelica, ca derivati odoranti. Acidul ca atare (si ca saruri) are actiune sedativa, calmanta.
Acizii monocarboxilici cu catena normala cu numar par de atomi de carbon, C4-C22, se numesc acizi grasi si se gasesc in natura ca esteri, (grasimi, uleiuri eterice). Mai raspanditi sunt: acidul butiric (C4) in untul de vaca, acidul capronic (C6), acidul caprilic (C8), acidul caprinic (C10) in unt de vaca, de capra si in unele grasimi vegetale (unt de cocos), acidul lauric (C12) in untul de cocos si in fruct de dafin (Laurus nobilis), acidul miristic (C14), acidul palmitic (C16), acidul stearic (C18) in grasime etc. Structura acestor acizi a fost dovedita prin sinteza si degradare.
Dintre acizii cu numar impar de atomi de carbon, cu catena normala, prezenti in uleiuri eterice ca esteri, poate fi amintit acidul pelargonic CH3(CH2)7 - COOH, izolat din ulei de muscata (Pelargonium roseum).
Ca acizi ciclici se mentioneaza acidul lactobacilic, C19, izolat din Lactobacillus arabinosus si L. casei, cu structura:
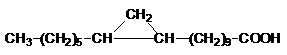
Acidul benzoic, C6H5-COOH, se gaseste in rasini vegetale si balsam, in tinctura de Tollu si de Peru. Acidul benzoic este o substanta cristalizata in foite albe, stralucitoare, care sublimeaza inainte de topire. Se poate separa si prin antrenare cu vapori de apa (T.t. 121,7oC si T.f. 249,2oC). Se obtine prin oxidarea toluenului sau prin hidroliza feniltriclormetanului (produs secundar la clorurarea toluenului). Acidul benzoic si sarea sa de sodiu se pot utiliza ca dezinfectanti (0,1%), conservanti pentru alimente si medicamente.
Acidul fenilacetic, C6H5-CH2-COOH, este o substanta cristalina, incolora.
Acizii din petrol (acizi naftenici), au fost pusi in evidenta in petrolul romanesc de catre C.D.Nenitescu si D.Isacescu (1938), in cantitati mici (sub 1%). Ei sunt acizi alchilcicloalcancarboxilici (cu cicluri de 5 si 6 atomi). Sarurile lor de cobalt si mangan sunt catalizatori importanti, iar sarurile de sodiu se utilizeaza ca sapunuri. Unii naftenati (de cupru, de exemplu), au proprietati fungicide.
ACIZI DICARBOXILICI SI POLICARBOXILICI SATURATI
Numele acizilor dicarboxilici se formeaza prin adaugarea sufixului "-dioic" la numele hidrocarburii cu acelasi numar de atomi de carbon, cu precizarea pozitiilor grupelor carboxil. La acizii cu mai multe grupe carboxil se pune sufixul corespunzator.
Se folosesc si denumiri empirice, intrate in uz ca de exemplu: acid oxalic, acid difenic, acid succinic, acid ftalic, acid trimesic
Metode de obtinere
a. Metode oxidative
Ciclohexanul se oxideaza catalitic conducand la acid adipic.
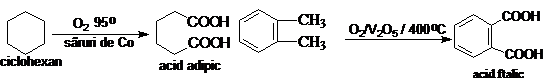
o-, m-, p-Xilenii se oxideaza cu aer, in conditii catalitice, cu formare de acizi dicarboxilici aromatici (acizii ftalici). Acidul o-ftalic se obtine si prin oxidarea naftalenului.
In ultimii ani s-a pus la punct o metoda economica pentru obtinerea acidului o-ftalic plecand de la benzoat de sodiu si monoetilcarbonat de sodiu, la 200oC.
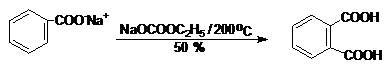
Acid ftalic
Glicolii primari se oxideaza la acizi organici dicarboxilici. De exemplu etilenglicolul se oxideaza la acid oxalic.
Ciclohexanolul se oxideaza cu permanganat de poatsiu sau cu acid azotic formand acid adipic, cu randament bun.

Compusii carbonilici ciclici sau dicarbonilici se pot oxida la acizi dicarboxilici. Oxidarea glioxalului ca si a altor dialdehide conduce la acizi dicarboxilici
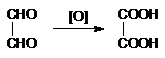
acid oxalic
b. Metode de hidroliza. Derivatii difunctionali, in special dinitrilii alifatici, hidrolizeaza usor la acizi dicarboxilici saturati. Metoda se aplica si pentru obtinerea acizilor policarboxilici, ca de exemplu acidul tricarbalilic (1,2,3 - propantricarboxilic).
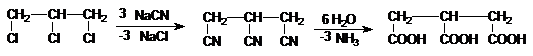
Acid tricarbalilic
c. Sinteze de acizi dicarboxilici cu ajutorul esterului malonic.
Condensarea esterului malonic cu metanal (CH2O), hidroliza produsului intermediar urmata de decarboxilare, este o metoda de sinteza pentru acidul glutaric.
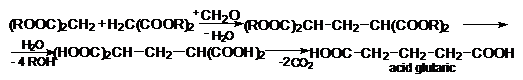
Structura. Proprietati caracteristice
Grupa carboxil are structura electronica identica cu cea descrisa la acizii monocarboxilici.
Prezenta celor doua grupe carboxil influenteaza aciditatea;
Acizii dicarboxilici saturati sunt mai tari decat acizii monocarboxilici.
Ei disociaza in doua trepte.
![]()
Efectul inductiv (-I) al grupelor carboxil se manifesta prin cresterea constantei in prima treapta de ionizare. In a doua treapta de ionizare, in general, K2 este mai mica.
In general K2 este mai mica decat K1 cu cel putin un ordin de marime datorita repulsiei electrostatice.
Face exceptie acidul oxalic, care are o aciditate marita (pK1 = 1,27 si pK2 = 4,27) datorita manifestarii efectului -I al primei grupe carboxil fata de a doua de care este legata direct (1,2).
Constantele de aciditate si solubilitatea unor acizi dicarboxilici
(date din literatura)
|
Acidul |
K1.10-5 |
K2.10-6 |
Solubilitate in apa la 20o C in % |
|
Acidul oxalic | |||
|
Acidul malonic | |||
|
Acidul succinic | |||
|
Acidul glutaric | |||
|
Acidul adipic | |||
|
Acidul pimelic | |||
|
Acidul suberic | |||
|
Acidul acelaic | |||
|
Acidul sebacic | |||
|
Acidul ftalic |
Acidul oxalic anhidru cristalizeaza diferit, a sau b, in functie de modul de formare a legaturilor de hidrogen.
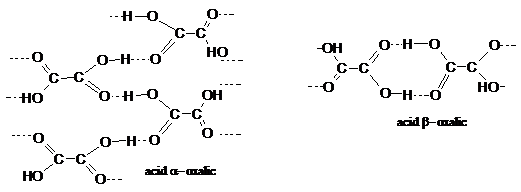
Acizii dicarboxilici superiori, de la patru atomi in sus, cu numar par de atomi de carbon, au moleculele plane si centrosimetrice, in timp ce la acizii cu numar impar moleculele sunt neplane, rasucite cu o axa de simetrie binara; grupele carboxil sunt inclinate cu un unghi de 60o. Moleculele acizilor cu numar impar de atomi de carbon sunt mai bogate in energie decat acizii din seria para si astfel se pot explica diferentele punctelor de topire sau solubilitatea.
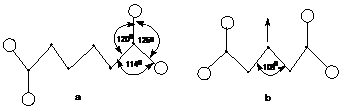
Proprietati fizice. Acizii dicarboxilici sunt solizi, ca urmare a numarului mare de legaturi de hidrogen intermoleculare.
Temperaturile de topire scad cu cresterea masei moleculare si prezinta alternanta: acizii cu numar par de atomi de carbon au puncte de topire mai mari decat acizii din seria impara. Punctele lor de topire raman superioare celor ale acizilor monocarboxilici.

Proprietati chimice
Proprietatea principala, care tine de pozitia reciproca a celor doua grupari carboxil este comportarea la incalzire sau descompunerea termica.
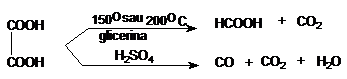
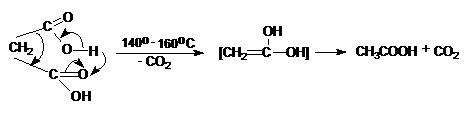
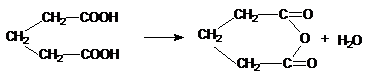
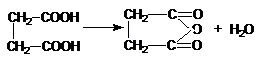
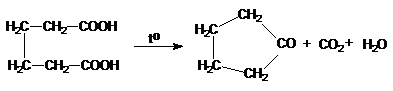
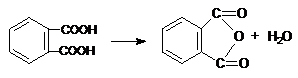
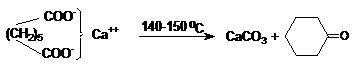
Acizi dicarboxilici importanti
Acidul oxalic este raspandit in natura ca sare de macris, oxalat acid de potasiu sau ca sare de calciu. Liber se gaseste in Aspergillus niger. Oxalatul de calciu se depune sub forma de calculi in litiaze. Acidul oxalic este toxic. Se poate obtine prin oxidarea unor compusi organici, etilenglicol, glucoza etc. Din punct de vedere chimic, acidul oxalic este un reducator.Pe aceasta proprietate se bazeaza utilizarea acidului oxalic ca decolorant in industria textila si in chimia analitica. Sarea de macris (KHC2O4.H2C2O4.2H2O) este folosita la scoaterea petelor de rugina.
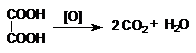
Acidul malonic, acid 1,3-dicarboxilic, se gaseste ca sare de calciu in sfecla de zahar.
Se obtine prin transformarea monocloracetatului de sodiu in nitril, urmata de hidroliza. Atomii de hidrogen din grupa CH2 din molecula acidului malonic (plasata intre grupele carboxil) sunt activi, participa la multe reactii in folosul sintezei organice. Acidul malonic se decarboxideaza usor, de aceea proprietatile sunt studiate pe diester.
Reactiile esterului malonic. Obtinerea esterului malonic sodat. Prin tratarea esterului malonic cu diferiti agenti bazici in mediu anhidru are loc formarea malonatului. De exemplu, sub actiunea etilatului de sodiu, a sodiului metalic sau a amidurii de sodiu rezulta ester malonic sodat.
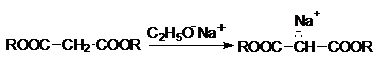
Anionul esterului se reprezinta prin formule limita sau structura mezomera: I,II sau III. In cele mai multe reactii esterul sodat se comporta ca si cum ar avea formula I, desi formula reala este III, in care exista un sistem conjugat cu repartizarea uniforma a electronilor pe cinci atomi.
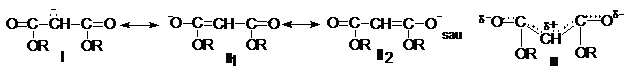
Multe sinteze au ca substanta de plecare esterul malonic sodat sau esterul ca atare.
Esterul malonic sodat participa la obtinerea acizilor monocarboxilici saturati liniari, ciclici, a acizilor dicarboxilici saturati sau a acizilor nesaturati. Obtinerea acizilor monocarboxilici saturati liniari:
![]()
(diacid instabil) Acid propanoic
Acidul succinic este un acid 1,4-dicarboxilic. Se gaseste in cantitati mici in organismele vii si in cantitati mari in chihlimbar (succinum). Se obtine prin hidrogenarea acidului maleic.
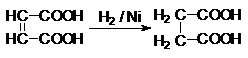
acid succinic
Sub forma de anhidrida intervine ca acidulant in produsele alimentare. Esterii sai, ca monogliceride, imbunatatesc calitatile produselor de panificatie. Acidul succinic si unii derivati alcatuiesc materia prima in sinteza organica.
Acidul adipic, 1,6-dicarboxilic, se obtine industrial prin oxidarea ciclohexanonei sau ciclohexanolului cu acid azotic sau permanganat de potasiu. Prin policondensare cu diamine alifatice formeaza poliamide din care se obtin fire si fibre sintetice (vezi poliamide). Unii esteri ai acidului adipic sunt buni plastifianti.
Acidul sebacic, 1,10-dicarboxilic, rezulta prin descompunerea uleiului de ricin, in mediu alcalin ; ricinoleatul de la hidroliza trece in 2-octanol si sarea monosodica a acidului sebacic. Unii esteri ai acidului sebacic sunt buni plastifianti pentru mase plastice.
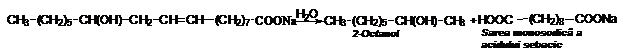
Acizii ciclici dicarboxilici. Acidul 1,2-ciclopropan-dicarboxilic prezinta izomerie cis-trans (Z-E). Acidul cis (Z) este inactiv prin analogie structurala cu acidul mezotartric, iar acidul trans (E) se prezinta ca racemic (aceeasi configuratie ca acizii + si - tartrici).
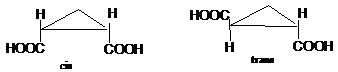
Acizi aromatici dicarboxilici
Acidul o-ftalic se obtine prin oxidarea o-xilenului sau naftalenului. Acidul ftalic este o substanta cristalizata, alba, cu T.t.208o (temperatura nu este neta din cauza formarii anhidridei). Este materie prima pentru industria colorantilor si maselor plastice.
Acidul tereftalic este greu solubil in solventi organici. Sublimeaza la 300oC. Este materie prima pentru fibra sintetica terilen.
Acizi tricarboxilici si policarboxilici
Acidul tricarbalilic (1,2,3-propan-tricarboxilic) a fost identificat in unele vegetale.
O cale de sinteza este saponificarea trinitrilului corespunzator, obtinut din 1,2,3-tribrompropan.
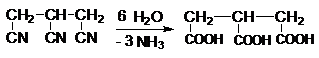
Acidul trimesic, 1,3,5-benzentricarboxilic, ca si ceilalti izomeri, se prepara prin oxidarea trimetilbenzenilor corespunzatori:
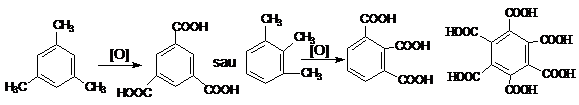
Mezitilen Acid trimesic Hemimeliten Acid hemimelitic acid melitic
Acidul melitic, benzen-hexacarboxilic, se formeaza prin oxidarea grafitului, a carbunilor fosili sau carbunelui activ cu acid azotic. Reactia confirma prezenta inelelor benzenice in grafit. La distilare cu calce sodata se decarboxileaza conducand la benzen. Acidul melitic este substanta solida, stabila, usor solubila in apa.
ACIZI NESATURATI CARBOXILICI
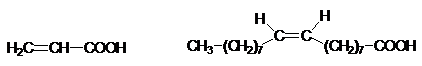
acid propenoic Acid cis-9-octadecenoic
Acid acrilic Acid oleic
Metode de obtinere a acizilor nesaturati monocarboxilici
a. Metode de eliminare.
Eliminarea apei din b-hidroxiacizi in mediu acid decurge usor, asemanator deshidratarii alcoolilor, conform schemei:

Dehidrohalogenarea acizilor b-halogenati in mediu de KOH alcoolic
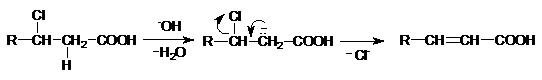
b. Metode oxidative in care oxidantul nu lezeaza dubla legatura
Oxidarea blanda a unei aldehide nesaturate cu oxid umed de argint sau cu oxidaze conduce la acid nesaturat.
![]()
Acid a b-nesaturat
c. Metode de condensare
Pentru a obtine acizi a b-nesaturati sau cu legaturi duble conjugate se aplica condensarea aldehidelor corespunzatoare cu acid malonic in prezenta de piridina sau piperidina.
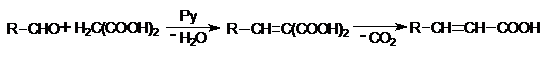
Acid a b-nesaturat
In acelasi mod pot sa rezulte si unii acizi cu mai multe duble legaturi: de exemplu acid sorbic
Aldehida benzoica, in conditiile reactiei Perkin, se condenseaza ca anhidrida acetica in prezenta acetatului de sodiu (baza) cu formarea acidului cinamic. Dupa acest mecanism, se pot obtine si alti acizi.
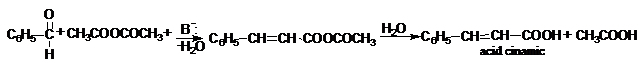
Structura. Proprietati fizice. Caracteristici spectrale
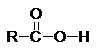 R, este
nesaturat: vinil-alil-, etinil- etc.
R, este
nesaturat: vinil-alil-, etinil- etc.
Radicalii organici nesaturati sunt grupe atragatoare de electroni, cu efect -I ca si halogenii, care maresc stabilitatea anionului carboxilat si deci, maresc aciditatea acidului respectiv. Peste efectul inductiv se suprapune efectul de conjugare, care actioneaza antagonist cu efectul -I, tinzand sa micsoreze partial aciditatea.
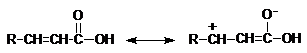
Constante de aciditate
|
Denumirea |
Formula |
Ka.10-5 |
|
Acid acrilic |
H2C=CH-COOH | |
|
Acid vinilacetic |
H2C=CH-CH2-COOH | |
|
Acid crotonic |
CH3-CH=CH-COOH(Z) | |
|
Acid cinamic |
C6H5-CH=CH-COOH | |
|
Acid tetrolic |
Acizii nesaturati sunt acizi mai tari decat acizii saturati,
Datorita dublei legaturi, unii acizi nesaturati apar, de cele mai multe ori, sub forma izomerilor geometrici cis-trans.

Izomerii trans se gasesc in natura in cantitati mai mici; in cantitati mai mari se formeaza la hidroliza grasimilor sau prin sinteza, prin reactii de eliminare; nu sunt asimilati de organism. Acizii cis sunt mai raspanditi, mai stabili si intervin in procesele biochimice. Unii acizi nesaturati apar in natura ca substante uleioase, altii in stare solida.
In UV, grupa carboxil are efect batocrom influentand tranzitiile p p* din sistemul nesaturat.
In spectrele IR acizii a b -nesaturati prezinta o frecventa caracteristica nC=C care apare la 1630-1660 cm-1 ; celelalte frecvente nC=O si nO-H apar, cu mici deplasari, in domeniile caracteristice acizilor saturati.
In spectrele RMN protonii vinilici sunt puternic dezecranati (acizi a b-nesaturati) avand deplasari chimice caracteristice.Protonul carboxilic apare la d 13-14 ppm.
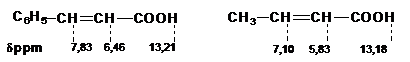
Proprietati chimice
Acizii organici nesaturati participa la reactii prin grupa carboxil cu formare de saruri si derivati functionali. Fiind acizi carboxilici nesaturati dau insa si reactii (cele mai multe) caracteristice sistemului nesaturat.
Aditia de hidrogen molecular in prezenta de catalizatori (Ni, Pd, Pt) sau de hidrogen in stare nascanda, cel mai usor reactia are loc la dubla legatura.
![]()
Reactia este utila tehnologiei de hidrogenare a uleiurilor vegetale pentru obtinerea margarinei.
Aditia halogenului este una din reactiile caracteristice. Aditia I2 serveste la caracterizarea gradului de nesaturare prin cifra de iod (indice de iod). La acizii cu duble legaturi conjugate, se formeaza produsul de aditie la capetele sistemului, cu o dubla legatura ecranata (de halogen si de grupa COOH), care nu se mai poate halogena (efect cusca).
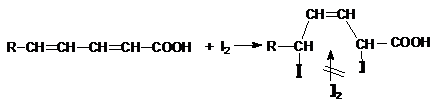
Cu ozonul, acizii nesaturati formeaza ozonide (ca si alchenele), care prin descompunere dau compusi cu catene mai scurte, cu structura cunoscuta, reactia servind la determinari structurale. Cu oxigenul molecular, acizii nesaturati, in special cei superiori, se autooxideaza in pozitie alilica generand epoxizi, hidroxiacizi sau se peroxideaza si se degradeaza.
Degradarea grasimilor are loc in procesul de prelucrare si in timpul pastrarii, sub actiunea luminii, a vaporilor de apa (umiditate), a caldurii, in contact cu aerul (oxigenul) sau in prezenta unor microorganisme, cu aparitia mirosului de alterare, gustului specific neplacut si cu cresterea aciditatii.Fenomenul de degradare (rancezire) poate fi o rancezire hidrolitica sub influenta umezelii sau a lipazelor cu formarea acizilor grasi liberi si drept urmare creste aciditatea (indice de aciditate) grasimii.
Rancezirea cetonica consta in oxidarea acizilor grasi sub influenta enzimelor sau a oxigenului cu formarea acizilor b-cetonici care imprima gust neplacut, iute. Prin decarboxilare, acizii trec in cetone care contin un radical metil, volatile si toxice. Aceasta rancezire cetonica conduce la modificari de gust si la miros neplacut. Degradarea este accentuata la grasimile care contin acizi grasi cu 6-12 atomi de carbon.
Reactiile se petrec dupa schema:
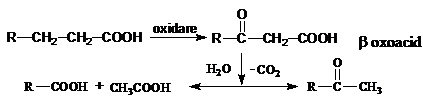
Aditia compusilor nesimetrici are loc contrar regulii lui Markovnikov deoarece orientarea aditiei este determinata de efectul atragator de electroni al grupei COOH asupra legaturii -HC=CH-

Izomerizarea. La incalzirea acizilor nesaturati cu dubla legatura in pozitii departate de carboxil (b g g d si d e), in prezenta bazelor puternice, se produc deplasari ale dublei legaturi in a b
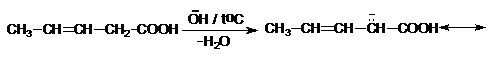
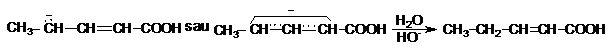
![]()
Elaidizarea
-poate fi considerata o reactie de izomerizare. Acidul oleic (cis) in prezenta urmelor de acid azotos (NO2*) sau a razelor UV, trece in acid elaidic (trans).
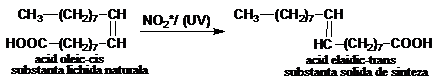
Lactonizarea
Daca acizii nesaturati contin dubla legatura in pozitia b g- sau in g d-, in mediu acid, are loc o interactie dubla legatura - grupa carboxil, cu formarea unui ester ciclic denumit lactona.
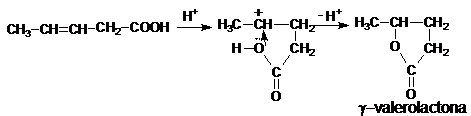
Analog se formeaza d - lactona :
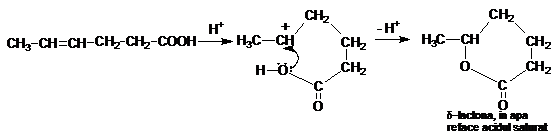
In conditii speciale, prin fierbere in alcalii, acizii nesaturati pierd dioxidul de carbon cu formarea alchenelor corespunzatoare.


Acizi nesaturati monocarboxilici mai importanti
Acidul metilacrilic este un lichid care polimerizeaza usor. Esterul sau metilic este monomerul sticlei plexi, "sticla organica" care are o transparenta foarte buna si o masa moleculara mare.
Reactia are la baza acetona si acidul cianhidric. In solutie de H2SO4 concentrat are loc hidroliza si in acelasi timp deshidratarea.
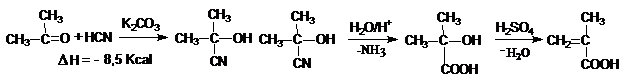
In solutie de H2SO4 concentrat si alcool metilic, pe langa saponificare si eliminare de apa, are loc esterificarea.
Metacrilatul de metil se polimerizeaza dupa mecanismul radicalic, in bloc, la 125oC, cu formarea polimetacrilatului de metil.
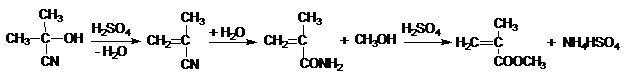
Acidul atropic rezulta la degradarea produselor vegetale unde se gaseste sub forma condensata.
Acidul crotonic b-metilacrilic, se prezinta ca izomeri cis-trans (Z-E). Se obtine prin sinteza (vezi metode generale de preparare). Acidul crotonic -trans este o substanta solida stabila (izomerul cis este lichid, T.f.=169oC). Prin oxidare, acidul crotonic trece in acid oxalic si acid acetic (confirma structura), iar prin hidrogenare duce la acid butiric.
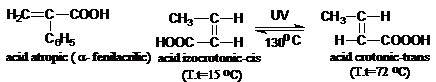
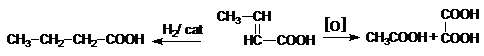
Acidul vinilacetic, CH2=CH-CH2-COOH, este instabil si in mediu acid sau bazic se izomerizeaza in acid crotonic
Acidul cinamic, C6H5-CH=CH-COOH, se gaseste in natura ca ester in unele rasini si balsamuri. Un ulei de scortisoara se gaseste liber ca izomer trans (E). Izomerul cis (Z) este numit acid alocinamic si se gaseste in natura numai ca ester. Acidul cinamic se obtine prin sinteza din aldehida benzoica si anhidrida acetica, in cataliza bazica (vezi condensarea Perkin). Acidul alocinamic se formeaza din acid cinamic prin iluminare UV. Prin hidrogenare acizii cinamic si alocinamic conduc la acelasi acid b-fenilpropionic sau hidrocinamic.
Prin cicloaditie sub actiunea luminii, acidul cinamic trece in acizii truxilic si truxinic care au fost izolati si din frunzele de coca. Din acid cinamic se poate obtine acidul fenilpropiolic.

Acidul crizantemic a fost identificat in florile de piretru. El a fost obtinut si prin sinteza (vezi sinteze de acizi nesaturati). Acidul si esterii prezinta proprietati insecticide.
Acizii nesaturati superiori, prezinta un interes deosebit; ei intra in constitutia grasimilor.
Acidul palmitoleic, cis-9-hexadecenoic (C16-D , unde D reprezinta pozitia dublei sau dublelor legaturi), este prezent in uleiuri vegetale si in ceruri. Pana la 20% se gaseste in ulei de peste
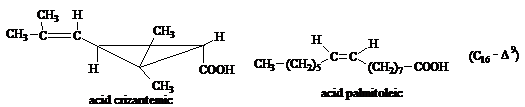
Acidul oleic, cis-9.-octadecenoic, este cel mai raspandit acid in regnul vegetal.
Este principala componenta a uleiului de masline, de floarea soarelui si a altor grasimi unde se gaseste ca ester al glicerinei. Structura acidului oleic a fost stabilita prin hidrogenare in acid stearic, apoi prin ozonoliza si descompunerea ozonidei in aldehide.(aldehidele se transforma prin oxidare in acizii corespunzatori sau prin sinteze). Acidul oleic (C18, D9 sau cis-9-octadecenoic) este lichid incolor, inodor. Acidul elaidic este solid si nu se gaseste in natura. Acidul oleic este solvent pentru unele vitamine si medicamente.
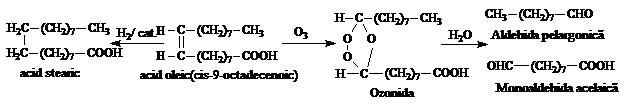
Acidul petroselic(C18,D ;cis-6-Octadecenoic) a fost pus in evidenta in ulei de patrunjel etc.
Acidul vaccenic (C18, D ; trans-11-Octadecenoic) este singurul acid superior care se gaseste ca izomer trans in grasimi animale.
Acidul sterculic (C19, D ciclic) a fost izolat din grasimea plantei Sterculia foetida. Contine 19 atomi de carbon si un ciclu de trei atomi.
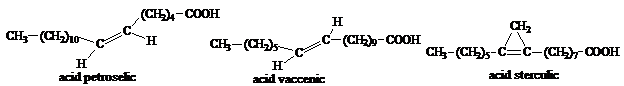
Acidul chaulmoogric si acidul hydnocarpic au fost izolati din fructele unor arbori tropicali. Esterii lor au fost utilizati mult timp la combaterea leprei.
Acidul gadoleic (C20, D ), cis-9-eicosaenoic este raspandit in grasimile animalelor de mare.
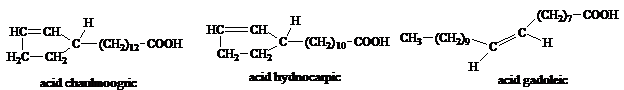
Acidul erucic (C22, D ), cis-13-docosaenoic se gaseste ca izomer cis in uleiul de rapita si mustar. Izometrul trans, acidul brasidic nu se gaseste in natura. Ei formeaza o pereche de izomeri geometrici.
Acidul micolipenic, C27, D - ramificat, a fost izolat din bacilii tuberculozei unde se gaseste sub forma de esteri ai zaharurilor.
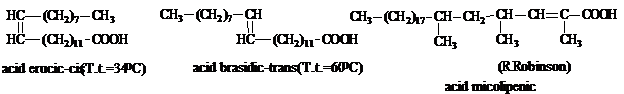
In unele uleiuri, acizii nesaturati sunt insotiti de hidroxiacizi nesaturati.
Acidul ricinoleic este extras din ulei de ricin. La temperatura, el se descompune in acidul undecilenic important in parfumerie si farmacie si heptanal.
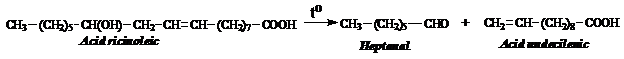
Acizi polinesaturati monocarboxilici
Acizii polinesaturati monocarboxilici sunt compusi naturali sau de sinteza si prezinta un sistem de duble legaturi conjugate sau legaturi duble izolate
Acidul sorbic, 2,4,-hexadien-carboxilic, a fost izolat din fructele scorusului de munte si din alte plante samburoase (Sorbus). Sintetic se prepara prin condensarea aldehidei crotonice cu acid malonic in prezenta piridinei, sau folosind ester malonic.
Acidul sorbic este solid si are T.t. 134oC. Este netoxic. Are actiune selectiva asupra drojdiilor si mucegaiurilor. In concentratii 0,1-0,2% are proprietati conservante si stabilizante pentru unele produse (vin, branza, stafide).
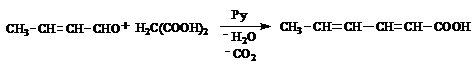
Folosind metoda de sinteza data mai sus, au fost obtinuti acizi polienici de forma:
CH3-(CH=CH)n-COOH, in care n = 3-8. Cand n >3, acizii polienici sunt colorati. Pornind de la acizii polienici s-au realizat sinteze de acizi grasi superiori.
In grasimi, au fost identificati si izolati acizi superiori cu mai multe duble legaturi din care unii au fost sintetizati.
Acidul linolic, (C18 D ), cis, cis - 9,12 - octadecadienoic, se gaseste in grasimi. Prezinta izomeri geometrici. Structura a fost demonstrata prin degradare oxidativa si prin sinteza.
Acidul linolenic, (C18, D ), cis, cis, cis-9,12,15-octodecatrienoic, este prezent in uleiuri sicative, de in sau rapita. Structura a fost stabilita prin ozonoliza si prin sinteza cand s-a precizat si configuratia cis-cis-cis.Avand mai multe legaturi duble se oxideaza si se polimerizeaza.
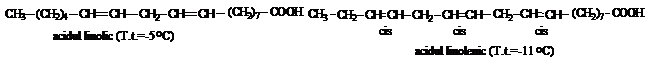
Acidul elaeostearic, (C18 D a sau b -9,11, 13-octadecatrienoic, apare in ulei de tung (China) si alte grasimi vegetale. Prezinta o forma a labila trans-trans-cis cu T.t. 48oC (in ulei de tung), care sub influenta luminii sau a caldurii si a catalizatorilor trece in forma b-stabila trans-trans-trans cu T.t. 71oC.
Acidul arahidonic, (C20, D5,8,11,14), acid 5,8,11,14-eicosatetraenoic, este precursor al prostaglandinelor. Se gaseste in creier si sange in cantitate mica.
Acidul clupanodonic, (C22, D4,8,12,15,19), acid 4,8,12,15,19-docosapentaenoeic, se gaseste in ulei de peste si animale marine. Este un acid instabil (se izomerizeaza repede). Structura dublelor legaturi izolate se determina prin degradare oxidativa.
Acidul docosahexaenoic, (C22, D5,8,11,14,17,20), a fost de asemenea pus in evidenta in unele grasimi. In unele grasimi a fost identificat si un cetoacid polinesaturat(acidul licanic, acid D9,11,13-4-ceto-octadecatrienoic).

Acizi nesaturati dicarboxilici si tricarboxilici
Acidul maleic este un compus obtinut industrial prin oxidarea benzenului, in faza gazoasa, cu aer in prezenta de vanadiu cand se izoleaza sub forma de anhidrida: C4H2O3.
Este solubil in apa. Functioneaza ca acid tare. Nu se gassete in natura. Are utilizari in obtinerea rasinilor sintetice si a altor produsi, fiind o materie prima ieftina.
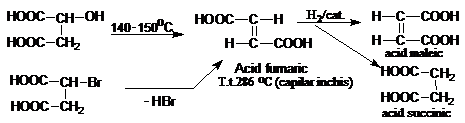
Acidul fumaric se gaseste in natura, dar poate fi obtinut si prin sinteza. In celulele vii, acidul fumaric este intermediar in metabolismul hidratilor de carbon. A fost identificat in Fumaria officinalis, in licheni si ciuperci. Prin sinteza se obtine din aciudul a-hidroxisuccinic (acid malic) prin incalzire la 140-150oC, sau din acidul bromsuccinic prin eliminarea acidului bromhidric Acidul fumaric este greu solubil in apa. Este acid mai slab (Ki= 9,5.10-4) decat acidul maleic (Ka= 142.10-4). Peste 200oC sublimeaza.
La hidrogenare, atat acidul maleic -cis cat si acidul fumaric -trans trec in acid succinic. Rezulta ca sunt izometri geometrici.
Acidul muconic se formeaza prin oxidarea benzenului, fenolului sau pirocatehinei cu peracizi. In natura se gaseste esterificat. Acidul muconic prezinta izomerie cis-trans. Se cunosc trei izomeri: cis-cis- T.t. 187oC, cis-trans- T.t. 184oC, trans-trans-T.t. 300oC.
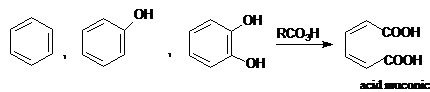
Acidul aconitic rezulta din transformarile acidului citric. Acidul aconitic este un antioxidant si un stabilizant al aromelor volatile (v. prajirea cafelei).
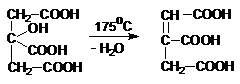
Acizi nesaturati cu triple legaturi
Acizii din aceasta grupa sunt in general compusi de sinteza si mai rar prezenti in natura.
Acidul propiolic are structura: HCsC-COOH. Se obtine prin sinteza din acetilena prin metoda carboxilarii sau prin decarboxilarea partiala a acidului acetilencarboxilic.
Acidul propiolic este un compus incolor, T.t. 18oC si T.f 144oC. Are miros accentuat de acid acetic. Polimerizeaza usor trecand in acid trimesic.
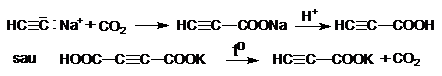
Acidul fenilpropiolic se obtine din acidul cinamic prin aditie de brom urmata de eliminarea hidracidului:
C6H5-CH=CH-COOH + Br2 C6H5-CHBr-CHBr-COOH
![]()
In natura se gaseste un acid superior monocarboxilic cu o tripla legatura in molecula, acidul tariric.
Acidul tariric, (C18, D ), a fost izolat din uleiul extras din semintele de Picramnia tariri (Sörrensen).
CH3-(CH2)10-CΞC-(CH2)4-COOH
Acidul de matricaria a fost izolat sub forma de ester metilic din ulei de flori de musetel. El contine pe langa tripla legatura si doua legaturi cis, cis, duble
![]()
Acidul acetilen-dicarboxilic se obtine din acidul fumaric prin bromurare urmata de dehidrohalogenare:
Esterii acidului acetilen dicarboxilic participa la reactii de cicloaditie
![]()
Copyright © 2025 - Toate drepturile rezervate