 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
Zeolitii si materialele microporoase inrudite se obtin prin sinteza hidrotermala din amestecuri de reactie (hidrogeluri) ce contin elementele T capabile sa coordineze tetraedric si sa formeze retelele zeolitice precum si diversi anioni si cationi. Fiecare component al sistemului are o contributie specifica in formarea gelului si final, in cristalizarea unui anumit zeolit.
Factorii care influenteaza primordial cristalizarea unui zeolit sunt compozitia amestecului de reactie, temperatura si timpul la care se adauga factorii ajutatori.
Factorii care influenteaza sinteza zeolitilor din hidrogeluri.
1. Compozitia amestecului de reactie:
1.1. raportul molar SiO2/Al2O3 sau Si /Al (SAR)
1.2. [OH![]() ]; OH
]; OH![]() /SiO2
/SiO2
1.3. cationii:
a. anorganici: Na2O/SiO2; K2O/SiO2
b. organici: R2O/SiO2
1.4. anioni (altii
decat OH![]() )
)
1.5. alte specii neionice:
a. gaze dizolvate
b. compusi organici
1.6. H2O; H2O/SiO2
2. Timpul de cristalizare
3. Temperatura de lucru:
a. ambientala: 25 - 60 oC
b. joasa: 90 - 120 oC
c. moderata: 120 - 180 oC
d. inalta: 250 oC si mai sus
4. Factori ajutatori:
a. maturarea hidrogelului
b. agitarea amestecului de reactie
c. natura amestecului (solutie, solutie coloidala, gel)
d. ordinea de adaugare a reactantilor
Compozitia amestecului de reactie se exprima in moli si in rapoarte molare si are in vedere forma initiala sub care se introduc elementele T formatoare ale retelei zeolitice.
a. sursa de silice
- solutie apoasa tehnica de silicat de sodiu (~ 9,0% Na2O si 29% SiO2);
- silice coloidala stabilizata (colloidal silicasol) cu 30 sau 40% SiO2
- silice amorfa de ardere (fumed silica) (Cab-O-Sil, Aerosil)
- silice de precipitare (Hi-Sil, Ultrasil, Romsil)
- tetrametil
si tetraetilortosilicat (
Rolul silicei este de constructor al retelei zeolitice.
b. sursa de alumina
- aluminat de sodiu -cu raportul Na/Al = 1,0-1,2;
- sulfat de aluminiu: Al2(SO4)3. 18 H2O ( 48,6% apa);
- azotat de aluminiu: Al(NO3)3. 9 H2O (43 % apa);
- fosfat de aluminiu: Al PO4.2H2O;
- alumina böhmit, AlOOH;
- alumina pseudo hidratata ,Al(OH)3.
Rolul aluminei este acela de constructor al retelei zeolitice si furnizor de sarcina negativa a retelei.
c. surse pentru alte elemente T ale retelei : compusi cu B, Fe, Cr, Ga, Ti, V.
Pentru fiecare compozitie utilizata, cristalizarea se urmareste in timp (pentru o temperatura data) si se exprima sub forma curbei de cristalizare: variatia cantitatii de zeolit cristalizat (%) vs timp de cristalizare. O curba de cristalizare care prezinta un timp relativ scurt pentru perioada de nucleiere, o viteza mare a cristalizarii in perioada de cristalizare si un grad de cristalinitate maxim (100 %) corespunde amestecului cu compozitie optima.
Prin modificarea compozitiei amestecului initial se poate stabili domeniul sau campul de cristalizare al structurii zeolitice cercetate.
Prepararea amestecului are in vedere omogenizarea sistemului prin agitare mecanica, formarea sistemului sub forma de solutie, gel amorf sau sol amorf, ordinea de adaugare a reactantilor, insamantarea sistemului cu cristale ale zeolitului ce urmeaza a fi obtinut (pentru cresterea vitezei de cristalizare), perioada de incubare (imbatranire) a sistemului la temperatura camerei sau alta temperatura cu sau fara agitare inainte de a fi supus cristalizar
Raportul molar SiO2/Al2O3 din amestecul initial
Este un parametru chimic principal al sintezei si variaza de la ~ 2,0 pentru zeolitul LTA la ∞ pentru silicalit -1 sau silicalit-2. Raportul SiO2/Al2O3 din amestecul initial influenteaza raportul SiO2/Al2O3 din zeolitul obtinut. Zeolitii cu raport Si /Al ridicat prezinta mare stabilitate termica si hidrotermica, o aciditate controlata a retelei precum si o hidrofobicitate tot mai accentuata. Compozitia retelei controleaza sarcina retelei si influenteaza stabilitatea structur Sarcina retelei determina campul electrostatic care modifica puternic interactiunea dintre zeolit si moleculele adsorbite. Cu cresterea raportului SiO2/Al2O3 in zeoliti are loc:
cresterea rezistentei la substantele acide;
cresterea stabilitatii termice;
cresterea hidrofobicitatii;
scaderea afinitatii suprafetei pentru moleculele polare;
scaderea continutului de cationi si deci scaderea capacitatii de schimb ionic.
Agentul
de mineralizare specific cristalizarii zeolitilor
silicoaluminosi este ionul hidroxid, OH-. pH-ul alcalin este
realizat prin adaugarea unei baze anorganice si /sau organice, ultima
pentru cazul in care cationul organic indeplineste rol de "formator" de
retea (template). pH-ul
hidrogelului are influenta asupra fazei de nucleere, a randamentului
cristalizarii, a raportului Si/Al din zeolit si asupra morfologiei
zeolitului. Valori mari ale pH-ului conduc la zeoliti cu raport mic Si/Al
si la obtinerea de cristale mici. Continutul in ioni OH![]() din gelul initial influenteaza natura
speciilor (monomerice si polimerice) prezente in amestecul de reactie
si viteza cu care aceste specii reactioneaza prin hidroliza
si prin schimb intre faza solida si cea lichida cu formare
de noi specii in solutie. In plus, continutul in ioni -OH influenteaza viteza de
crestere a cristalelor, scurteaza perioada de inductie si determina tipul de retea.
din gelul initial influenteaza natura
speciilor (monomerice si polimerice) prezente in amestecul de reactie
si viteza cu care aceste specii reactioneaza prin hidroliza
si prin schimb intre faza solida si cea lichida cu formare
de noi specii in solutie. In plus, continutul in ioni -OH influenteaza viteza de
crestere a cristalelor, scurteaza perioada de inductie si determina tipul de retea.
Alcalinitatea amestecului de reactie dirijeaza cristalizarea zeolitilor influentand asupra tipului structural obtinut final. Alcalinitatea si respectiv "alcalinitatea libera" este un parametru critic al sintezei si al raportului Si /Al din zeolitul cristalizat .
In timpul cristalizarii pH-ul mediului variaza, mai intai scade si apoi la final este mai mare decat initial datorita incorporarii unitatilor SiO2 in reteaua zeolitica. Alcalinitatea libera este data de diferenta dintre alcalinitatea totala (MOH) si alcalinitatea aluminatului de sodiu (MAlO2).Valori ale pH -ului amestecului de sinteza intre 12,3-13,8 sunt caracteristice cristalizarii zeolitilor de tip faujazit X si Y, intre 11,3- 12,7 celor de tip mordenit iar sub 11,5 celor de tip ZSM-5. Alcalinitatea mediului determina formarea anumitor specii de silicat, aluminat si aluminosilicat sub forma de monomeri, dimeri, trimeri, tetrameri cu formarea inelelor de 4-membri si a inelelor de 5-membri: [SiO2(OH)2]2-, [SiO(OH)3]-, [Al(OH)4]-, [Al(OH)3OSi(OH)3]-, etc.
Raportul
molar OH![]() /SiO2 influenteaza tipul structural
si morfologia cristalelor. Continutul de hidroxid, OH
/SiO2 influenteaza tipul structural
si morfologia cristalelor. Continutul de hidroxid, OH![]() , se calculeaza prin sumarea molilor OH
, se calculeaza prin sumarea molilor OH![]() ce provin din NaOH, [AlK4N]OH, silicatul de sodiu
(NaOH + SiO2) si aluminatul de sodiu (NaOH + Al2O3)
si apoi scaderea molilor de acid adaugat (ca acid liber sau
sare). Este cazul folosirii sulfatului de aluminiu ca sursa de aluminiu,
considerat echivalent cu Al2O3 + 3H2SO4.
Un mol de Al2O3 este echivalent cu 2 moli H2SO4
atunci cand trece in ioni aluminat necesari formarii retelei.
ce provin din NaOH, [AlK4N]OH, silicatul de sodiu
(NaOH + SiO2) si aluminatul de sodiu (NaOH + Al2O3)
si apoi scaderea molilor de acid adaugat (ca acid liber sau
sare). Este cazul folosirii sulfatului de aluminiu ca sursa de aluminiu,
considerat echivalent cu Al2O3 + 3H2SO4.
Un mol de Al2O3 este echivalent cu 2 moli H2SO4
atunci cand trece in ioni aluminat necesari formarii retelei.
Prin
inlocuirea anionului hidroxid OH- cu anionul fluorura F![]() a facut posibila sinteza zeolitilor silicoaluminosi
si din medii slab acide (pH ~5). In
conditiile de pH ~ 5, silicea este solubilizata sub forma speciilor
de hexaflouro - silicat SiF62- care prin hidroliza
conduc la specii policondensate hidroxilate prin a caror unire se
formeaza reteaua zeolitica. Drept sursa pentru anionul F-
se utilizeaza NH4F, NH4HF2 si HF sau
substante ce contin si elementele T ale retelei, (NH4)2SiF6
si AlF3·H2O.
a facut posibila sinteza zeolitilor silicoaluminosi
si din medii slab acide (pH ~5). In
conditiile de pH ~ 5, silicea este solubilizata sub forma speciilor
de hexaflouro - silicat SiF62- care prin hidroliza
conduc la specii policondensate hidroxilate prin a caror unire se
formeaza reteaua zeolitica. Drept sursa pentru anionul F-
se utilizeaza NH4F, NH4HF2 si HF sau
substante ce contin si elementele T ale retelei, (NH4)2SiF6
si AlF3·H2O.
Cationii anorganici (Na+, K +) si cei organici (AlK4N+) in mediul de sinteza joaca rol de formatori ai retelelor zeolitice (template ) iar in produsul cristalizat de compensatori ai sarcinii negative excedentare a retelei. Formatorii de retea sunt specii cationice anorganice sau organice care intervin in formarea anumitor blocuri anionice de constructie prin asamblarea carora rezulta retelele zeolitice tipice. Conceptul de agent de formare (template) al unui anumit tip de retea, specific in special cationilor organici mari a fost introdus de catre Aiello si Barrer. Unele structuri zeolitice se formeaza numai in prezenta anumitor cationi (LTA, LTX si LTY-Na+, Sil-1-TPA+, etc), alte structuri se obtin folosind amestecuri de cationi dar cele mai multe structuri rezulta prin folosirea unui numar mare de cationi formatori de structura (structure - directing agent). Cationii stabilizeaza formarea anumitor subunitati structurale care prin cristalizare vor da forma porilor din interiorul structurii zeolitice.
In general, cationii alcalini, puternic hidrofili, sunt efectivi in cristalizarea din medii bazice a zeolitilor cu raport Si /Al scazut iar cationii organici (tetraalchilamoniu) - hidrofobi sunt efectivi in cristalizarea zeolitilor mediu si inalt siliciosi, precum si a materialelor microporoase de tip AlPO, SAPO, MAPO, MAPSO.
Cationii influenteaza morfologia cristalelor, cristalinitatea produsului si randamentul in produs.
Aditivii
organici - cationici (ioni cuaternari de amoniu) si neionici (amine
organice) prin modificarea gelului permit obtinerea unor structuri cu
raport SiO2/Al2O3 mai ridicat decat se
obtin in absenta lor (cazurile N - A, ZK - 4, alfa), duc la
modificarea pH-ului sau au o actiune tampon (cazul aminelor organice
slabe), la modificarea solubilitatii anumitor specii, a
proprietatilor de transport si termice cat si a duratei de
cristalizare. Aditivii organici indeplinesc rol de agent de directionare a
structurii cat si de material de umplere a volumului intern. Unii aditivi
organici sunt incorporati (inchisi) in porii zeolitului iar eliminarea
lor presupune un tratament termic sever la
Sinteza zeolitilor poate fi condusa in prezenta anumitor gaze dizolvate sau in prezenta unor substante organice neionice (solventi nepolari) care folosesc in special ca agenti de "umplere" a porilor structurilor formate (alcooli, DMSO, sulfolan, HCOOH, HCONH2, H2O2 ).
Apa interactioneaza puternic cu
cationii prezenti in amestecul de reactie astfel ca
produsii de interactiune (ionii hidratati) indeplinesc rol de
agent template pentru directionarea unor anumite structuri cristaline
zeolitice (![]() 1 Ǻ,
1 Ǻ, ![]() 3,6 Ǻ;
3,6 Ǻ; ![]() = 3,45 Ǻ,
= 3,45 Ǻ, ![]() = 3,65 Ǻ). Un al doilea rol al apei il constituie cel de
material de umplere a volumului liber al zeolitului. De asemenea,
continutul de apa influenteaza proprietatile de
transport in gel precum si vascozitatea gelului reactant.
= 3,65 Ǻ). Un al doilea rol al apei il constituie cel de
material de umplere a volumului liber al zeolitului. De asemenea,
continutul de apa influenteaza proprietatile de
transport in gel precum si vascozitatea gelului reactant.
Astfel, in cazul sintezei mordenitului un raport molar initial Na2O/SiO2 mare inseamna concentratii mai mici ale aluminiului si siliciului in faza lichida si conduce la cristalizarea unor faze zeolitice putin stabile. Un raport molar Na2O/SiO2 mic in gelul initial inseamna concentratii mai mari ale aluminiului si siliciului in faza lichida iar ca rezultat se formeaza faze zeolitice mai stabile.
Cristalizarea
zeolitilor poate avea loc la temperatura ambientala (25-60
In general,
zeolitii aluminosi cu raport Si /Al mic cristalizeaza
hidrotermal prin incalzire pe baie de apa (~95
In timpul cresterii temperaturii la nivelul amestecului de reactie au loc urmatoarele evenimente :
- accelerarea dizolvarii gelului cu formarea speciilor monomerice de silicat, aluminat si silicoaluminat;
- formarea dimerilor, trimerilor si tetramerilor,
- asocierea speciilor cu formarea unor anumite unitati secundare de constructie;
- nucleierea si cristalizarea zeolitului.
Cresterea temperaturii influenteaza viteza de crestere a cristalelor (scurteaza durata cristalizarii) iar pentru unii zeoliti duce si la cresterea dimensiunilor cristalelor (ZSM-5). Cresterea temperaturii de cristalizare are influenta si asupra densitatii produsului, produsul cristalin devenind cu structura inchisa.
Presiunea este un parametru fizic putin relevant deoarece cristalizarea zeolitilor are loc in general sub presiune autogena.
Timpul de cristalizare a unui zeolit variaza de la cateva ore pana la 100 de zile, in functie de compozitia amestecului si de temperatura la care se realizeaza cristalizarea. Pentru fiecare sinteza exista un timp optim pentru care randamentul in produsul cristalin si cristalinitatea zeolitului sunt maxime. Se determina pe baza curbei de cristalizare: % zeolit cristalizat vs. timp de cristalizare.
Agitarea amestecului supus cristalizarii conduce la modificarea concentratiei punctuale a reactantilor, la ruperea structurii gelului si formarea anumitor specii de silicat, aluminat si silico-aluminat precum si la uniformizarea temperaturii in masa de reactie.
Sinteza celor mai multe structuri zeolitice este favorizata de agitarea amestecului (continua sau discontinua) in timpul cristalizarii dar se cunosc cazuri cand agitarea nu permite obtinerea aceleiasi structuri obtinute din sistem fara agitare.
Tinand seama de fenomenele chimice care au loc in timpul genezei zeolitilor, procesul de cristalizare cuprinde 3 etape:
a. realizarea suprasaturarii solutiei in speciile formatoare de retea;
b. nucleierea si formarea germenilor de cristalizare;
c. cresterea cristalelor.
Curbele de cristalizare corespunzatoare au o forma sigmoidala evidentiind perioada de inductie (mai scurta sau mai lunga), perioada de cristalizare accelerata si perioada finala de atingere a cristalinitatii maxime (fig. 1).
Mecanismul sintezei difera de la zeolitii aluminosi la cei siliciosi si poate fi reprezentat simplificat astfel. (fig. 2).
In sinteza zeolitilor s-au urmarit doua obiective:
I. Cresterea
raportului Si/Al din reteaua zeolitica de la 1 in zeolitul LTA la
∞ in silicalit-1 (
Acest
lucru a fost posibil prin folosirea bazelor organice (cationi de
tetraalchilamoniu) cu rol de agenti de formare a structurilor zeolitice (template),
idee realizata pentru prima data
de catre R.M.Barrer in 1961 si care a condus la obtinerea
zeolitilor din familia PENTASIL,
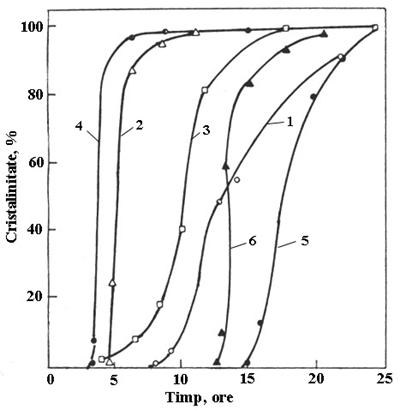
Fig. 1. Curbe de cristalizare specifice zeolitilor ZSM-5 [203]: temperatura
170
de Si, Al (P, Ge, Ga, Ti . )]
(alti cationi)
|
Gelifiere (amestecare)

![]()
Hidrogel amorf
![]()
Incalzire, T = 50-300
Agent de mineralizare
![]()
Dizolvare![]()
-OH -F
![]()
![]()
![]()
![]()
![]()
![]()
Formarea SBU
Nucleiere si crestere a cristalelor Agent de formare sau modelare a structurii
Cristale de
zeolit cu retea rigida ce contine cavitati
si/sau canale -Na+, K+ - -H2O -molecule
organice
Fig. 2. Mecanismul sintezei zeolitilor.
II. Introducerea altor elemente T in reteaua de silicoaluminat prin substitutie izomorfa partiala sau totala a Si4+ si Al3+. Au fost obtinuti astfel metalosilicatii cu B3+, Ga3+, Fe3+, Cr3+, Be2+, Ge4+, Ti4+, metaloaluminatul cu Ge4+ si apoi aluminofosfatii AlPO4-n, silicoaluminofosfatii SAPO-n si materialele micro-poroase MAPO, MAPSO, ElAPO si ElAPSO [16-20].
Substitutia izomorfa a Si4+ sau Al3+ cu alti atomi T aflati in stari diferite de valenta prezinta deosebit interes teoretic si practic. Se pot intalni patru tipuri de substitutie izomorfa si anume:
1. substitutie izomorfa cu un ion trivalent (B3+, Fe3+, Cr3+ Ga3+) cand reteaua cristalina isi pastreaza sarcinile negative excedentare dar se modifica parametrii celulei elementare, campul electrostatic, numarul si taria centrelor acide, caracterul hidrofil/hidrofob al retelei;
2. substitutia izomorfa a Al3+ cu un ion tetravalent ( Ge4+, Cr4+, Ti4+, Sn4+, Zr4+) cand reteaua cristalina devine electric neutra iar materialele respective nu au proprietatea de schimb cationic;
3. substitutia izomorfa cu un ion pentavalent ( P5+, As5+, V5+ . ) cand reteaua cristalina este neutra sau devine pozitiva cu proprietatea de schimb anionic. Prin inlocuirea totala a Si4+ cu P5+ s-au obtinut sitele moleculare AlPO, cu retea neutra si fara proprietatea de schimb ionic. Prin inlocuirea partiala a Al3+ si/sau a P5+ cu Si4+ s-au obtinut zeolitii de tip SAPO a caror retea este negativa (in anumite cazuri poate fi pozitiva).
4. substitutia izomorfa cu un ion divalent (Be2+, Mg2+, Mn2+, Co2+, Zn2+..) cand fiecare tetraedru substituit poarta doua sarcini negative ce trebuie compensate sau cand apar defecte de retea la atomii de oxigen.
Substitutia izomorfa cu un ion divalent duce la cresterea numarului de centre acide Brönsted iar substitutia cu un ion tetravalent duce la cresterea tariei centrelor acide.
Pentru a se realiza coordinarea tetraedrica trebuie sa fie indeplinita conditia de raport a razelor dintre atomul Tz+ si O2- :
0,225 < r Tz+ / r O2- < 0,414
In
sinteza zeolitilor unul din obiectivele cercetarii a fost
cresterea raportului Si/Al din reteaua zeolitica de la 1 in NaA
la ![]() in Silicalitul-1 (SiO2
microporos cu structura
in Silicalitul-1 (SiO2
microporos cu structura
Obtinerea zeolitilor siliciosi a fost posibila odata cu introducerea bazelor organice cu azot: hidroxizi de tetraalchilamoniu, saruri de tetraalchil amoniu (bromura, iodura, clorura), amine tertiare, secundare, primare, diamine.
Zeolitii
din familia PENTASIL avand drept termeni de capat ai seriei ZSM-5 (
Hidroxidul sau bromura de tetrapropilamoniu genereaza ZSM-5 din geluri de silicoaluminat si Silicalit-1 din geluri de silicat. iar hidroxidul sau bromura de tetrabutilamoniu genereaza ZSM-11 sau Silicalit-2.
Din cauza ca moleculele organice sunt incorporate in canalele zeolitice, acesti zeoliti au fost denumiti si "zeoliti cu azot" (nytrogeneous zeolite) sau organosilicati.
Zeolitii ZSM-5
prezinta proprietati specifice neintalnite la zeolitii
comuni. Prin
sinteza hidrotermala au fost obtinute structuri
Obtinerea zeolitilor de tip ZSM-5 din geluri si soluri de silicoaluminat alcalin s-a utilizat in primul rand prin folosirea unor baze organice cu azot in molecula, (baze organice si sarurile lor) capabile sa formeze cationi care sa complexeze si sa ordoneze tetraedrele [SiO4] si [AlO4] -. Ulterior, au fost folosite si alte substante organice ca de exemplu: alcooli, amide, hidroxilamine, detergenti etc.
Tabelul 2. Proprietati fizice ale structurilor ZSM-5 si Silicalit-.
|
Proprietatea |
ZSM-5 |
Silicalit-1 |
|
Indice de refractie la
25 -forma initiala -forma calcinata la 600
Difractograma DRX-tip structural: Dimensiunile canalelor, Å - drepte [010]; - sinusoidale [100]; Densitatea retelei, atom T/1000 Ǻ3 Densitatea, g/cm3 - experimentala - calculata Volumul microporilor (cm3/g) Volumul de adsorbtie la
25 - n-hexan - benzen |
identic ZSM-5 5,3 x 5,6 5,1 x 5,5 1,79 c 0,18 b 0,18 b 0,13 b |
identic silicalit-1 (ZSM-5) 5,0 x 5,6 1,80 c |
a - ZSM-5 cu raport molar SiO2 /Al2O3 = 6400; b - HZSM-5 cu raport molar SiO2/Al2O3 = 75; c - HZSM-5 cu raport molar SiO2/Al2O3 = 8660;
Sintezele in prezenta
cationilor organici conduc la structuri ZSM-5 cu rapoarte SiO2/Al2O3
care variaza in limite foarte largi, de la 10 la ![]() in Silicalitul-1, iar
sintezele efectuate in prezenta substantelor organice capabile
sa complexeze sau sa solvateze speciile ionice existente in gelul de
silicoaluminat conduc la structuri ZSM-5 in care raportul SiO2/Al2O3
nu depaseste valoarea 100 si care, de cele mai multe
ori sunt impurificate cu ZSM-8, ZSM-11 si cuart.
in Silicalitul-1, iar
sintezele efectuate in prezenta substantelor organice capabile
sa complexeze sau sa solvateze speciile ionice existente in gelul de
silicoaluminat conduc la structuri ZSM-5 in care raportul SiO2/Al2O3
nu depaseste valoarea 100 si care, de cele mai multe
ori sunt impurificate cu ZSM-8, ZSM-11 si cuart.
Din literatura de brevete si publicatii stiintifice privind obtinerea zeolitilor de tip ZSM-5, rezulta urmatoarele posibilitati de sinteza:
a. Sinteze in prezenta cationilor organici (AlK)4N + proveniti din hidroxid sau bromura de tetraalchil amoniu.
Comportarea lor in sinteza este diferita ca tip structural, puritate cristalografica, morfologie a cristalelor si ca durata a cristalizar Astfel, (CH3)4NBr sau (CH3)4NOH nu conduc la structuri de tip ZSM-5, iar (C2H5)4NBr, respectiv (C2H5)4NOH conduc la structuri de tip ZSM-5 si ZSM-8, dupa o perioada mai mare de cristalizare. (C3H7)4NBr sau (C3H7)4NOH conduc usor la structuri pure ZSM-5, in timp ce (C4H9)4NBr sau (C4H9)4NOH favorizeaza formarea structurii pure ZSM-11. (C5H11)4NBr sau (C5H11)4NOH si (C6H13)4NBr sau (C6H13)4NOH, conduc la ZSM-5 dupa 4 si respectiv 8 zile de cristalizare; (C7H15)4NBr sau (C7H15)4NOH conduc la ZSM-5 impurificat cu material amorf dupa 8 zile de cristalizare. Cationii (AlK)4N+ sunt folositi in amestec cu Na+ sau cu NH4+.
b. Sinteze in prezenta trialchilaminelor (AlK)3N. Numai tripropilamina (C3H7)3N si tributilamina (C4H9)3N joaca rol de modelator de structura (agent "template") pentru nucleerea si cristalizarea zeolitului ZSM-5, dar in amestec cu ZSM-11 si cuart.
c. Sinteze in prezenta dialchilaminelor (AlK)2NH.
Dipropilamina (C3H7)2NH, dibutilamina (C4H9)2NH, dipentilamina (C5H11)2NH cat si alte diamine conduc la zeoliti ZSM-5 in amestec cu ZSM-11, iar viteza de cristalizare creste cu cresterea numarul de atomi de C ai dialchilaminei.
d. Sinteze in prezenta n-alchilaminelor, n-AlKNH2 .
Alchilaminele primare din seria C1 - C12 conduc la zeoliti ZSM-5 in amestec cu ZSM-11 si silice.
e.Sinteze in prezenta de alchildiamine, H2N-(H2C)n-NH2 .
Diaminele C2-C12 conduc la ZSM-5 si ZSM-11, continutul in ZSM-11 creste de la C2 la C8 dupa care scade de la C9 la C12. Sintezele in prezenta aminelor diquaternare (CH3)3N(CH2)nN(CH3)3 in care n = 1 - 8, nu conduc la ZSM-5 sau ZSM-11.
f.Sinteze in prezenta de ioni complecsi MDO (C7H15N2)+ (1-metil-1,4-diazoniaciclo(2,2,2)octan2+) si DDO (C8H18N2)2+ (1,4-dimetil-1,4-diazonia-ciclo(2,2,2)octan2+ [31] si N-metilpirolidona [44]. In prezenta ionilor complecsi se obtin de cele mai multe ori amestecuri ZSM-5 si ZSM-11.
g. Sinteze in prezenta de alcooli.
Au fost utilizati alcoolii monohidroxilici C2 - C6 , diolii (etilen - glicol, 1-6 hexandiol), trioli (propantriol) si tetraoli in prezenta cationilor Na+ sau NH4+.
h. Sinteze in prezenta de amide.
In prezenta de oxietillactamida s-au obtinut structuri ZSM-5 pure.
i. Sinteze in prezenta de hidroxilamine HO(CH2)n-NH2.
j. Sinteze in prezenta de detergenti: structuri ZSM-5 impurificate cu alte faze au fost obtinute in prezenta de n - do - decilbenzensulfonat de Na sau n - alchil - polioxietilen sulfonat de Na.
k. Sinteze in absenta substantelor organice.
S-a reusit sinteza zeolitului ZSM-5 (de cele mai multe ori in amestec cu cuart) in absenta substantelor organice in care rolul de modelator de structura revine ionilor Na + hidratati, prin efectul de clatrare.
Cristalizarea zeolitului ZSM-5 este dependenta de urmatorii factori:
-compozitia amestecului initial;
-timpul de maturare a amestecului de reactie;
-temperatura si presiunea de lucru;
-durata cristalizar
Compozitia amestecului de reactie are rol hotarator in sinteza zeolitilor ZSM-5. Compozitiile de granita conduc usor la amestecuri de faze cristaline. In cazul sintezei zeolitului ZSM-5, pot aparea ca impuritati si zeolitii mordenit, ZSM-8, ZSM-11, ZSM-12 precum si a-cuart
Numai anumite compozitii initiale conduc la ZSM-5 de puritate si cristalinitate maxima si cu morfologie perfecta a cristalelor.
Amestecul initial supus cristalizarii (hidrogelul) contine silice (SiO2), alumina (Al2O3), oxid alcalin (Na2O) si/sau cationi de tetrapropilamoniu sau alte substante organice formatoare de retea si apa.
Compozitia
amestecului de reactie este bine exprimata sub forma
urmatoarelor rapoarte molare: SiO2/Al2O3,
HO![]() /SiO2, H2O/SiO2, Na2O/SiO2,
R2O/SiO2.
/SiO2, H2O/SiO2, Na2O/SiO2,
R2O/SiO2.
In cazul sintezelor realizate in prezenta unor substante organice care nu pun in libertate cationi organici se foloseste raportul molar R/SiO2 in care R reprezinta numarul de moli de substanta organica adaugata.
Gelul aluminosilicatic alcalin poate fi obtinut plecand de la surse diferite de silice si aluminiu, iar produsul final este adesea dependent de sursa folosita si de tratamentele initiale.
Drept surse de silice se folosesc cel mai adesea silicatul de sodiu (solutie), silicagelul sau silicea coloidala, silicea aerosil (fumed silica) dar si unele combinatii organice ale siliciului cum ar fi tetrametil- sau tetraetilortosilicatul, iar drept sursa de alumina se folosesc sulfatul de aluminiu, aluminatul de Na, g-alumina proaspat preparata, hidrargilit, gipsit, pseudoboehmit sau unele argile (caolin, haloisit, ilit, atapulgit, montmorilonit).
Alcalinitatea
amestecului initial este asigurata de prezenta hidroxizilor
alcalini (NaOH, KOH), a hidroxizilor si sarurilor cuaternare de
amoniu sau a aminelor tertiare, secundare sau primare. Valoarea
rapoartelor molare H2O/SiO2 si HO![]() /SiO2 influenteaza puternic forma sub care se
afla speciile initiale ale siliciului (mono sau oligomerice), cat
si viteza prin care trec din una in alta prin hidroliza pentru a
forma reteaua tridimensionala a zeolitului. In comparatie cu
zeolitii aluminosi, zeolitii pentasil se obtin din medii
care au valori reduse ale rapoartelor molare HO
/SiO2 influenteaza puternic forma sub care se
afla speciile initiale ale siliciului (mono sau oligomerice), cat
si viteza prin care trec din una in alta prin hidroliza pentru a
forma reteaua tridimensionala a zeolitului. In comparatie cu
zeolitii aluminosi, zeolitii pentasil se obtin din medii
care au valori reduse ale rapoartelor molare HO![]() /SiO2 (la ZSM-5 cuprins intre 0,1-0,8). Zeolitul ZSM-5 se
obtine plecand de la anumite compozitii initiale, iar modificarea
rapoartelor molare caracteristice conduce la rezultate diferite. Pentru un
anumit domeniu compozitional, viteza de cristalizare a zeolitului ZSM-5
creste cu cresterea raportul SiO2/Al2O3,
un indiciu ca reteaua zeolitului ZSM-5 prefera siliciul tetraedric
in dauna aluminiului tetraedric.
/SiO2 (la ZSM-5 cuprins intre 0,1-0,8). Zeolitul ZSM-5 se
obtine plecand de la anumite compozitii initiale, iar modificarea
rapoartelor molare caracteristice conduce la rezultate diferite. Pentru un
anumit domeniu compozitional, viteza de cristalizare a zeolitului ZSM-5
creste cu cresterea raportul SiO2/Al2O3,
un indiciu ca reteaua zeolitului ZSM-5 prefera siliciul tetraedric
in dauna aluminiului tetraedric.
Temperatura influenteaza mult procesul
de cristalizare. Comparativ cu zeolitii aluminosi, zeolitii
inalt siliciosi de tip ZSM-5 se obtin prin sinteza
hidrotermala sub presiune autogena, la temperaturi mai mari de 100
Valori
joase ale temperaturii de cristalizare in cazul amestecurilor bogate in siliciu
conduc la o durata mare de cristalizare, iar valori ridicate ale
temperaturii de cristalizare (peste 200
Este cunoscuta si cristalizarea zeolitului ZSM-5 si la 100 0C. Fiind un factor cinetic, temperatura influenteaza considerabil perioada de nucleatie, in care apar germenii cristalini, precum si viteza de crestere a cristalelor.
Formarea
si cresterea cristalelor de ZSM-5 depind de compozitia
amestecului initial, de temperatura si de viteza de incalzire
pana la temperatura de regim. Scurtarea perioadei de cristalizare se realizeaza prin
micsorarea raportului H2O/SiO2, cresterea
temperaturii si prin utilizarea germenilor de cristalizare.![]()
Cristalizarea amestecului reactant presupune parcurgerea urmatoarelor etape:
-precipitarea gelului initial;
-dizolvarea in timp a gelului;
-nucleerea unei /unor structuri zeolitice (poate avea loc din gel sau din solutii suprasaturate);
-cristalizarea continua si cresterea cristalelor structurii /structurilor initiate in etape de nucleere (are loc atat din faza de gel cat si din solutie);
-dizolvarea fazei /fazelor metastabile formate initial;
-cristalizarea continua si cresterea cristalelor noii faze cristaline mult mai stabila pe seama dizolvarii cristalelor fazei metastabile;
-dizolvarea fazei/fazelor metastabile formate ulterior;
-nucleerea fazei /fazelor la echilibru;
-cristalizarea si cresterea cristalelor fazei/fazelor cristaline finale.
-Transformarile succesive sunt reprezentate in fig. 3.
-procesul de formare initiala a unor specii simple sau polinucleare;
-embrionarea speciilor intr-un tot;
-formarea unor substructuri asemanatoare zeolitilor;
-agregarea ulterioara a structurilor in structuri mari.
Sistem oxidic (sol) nuclee ai fazei la echilibru gel faza I-a


-nucleiere -dizolvare
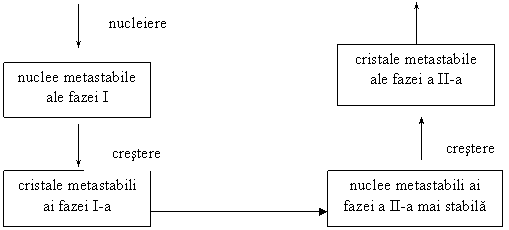
-dizolvare -nucleiere
Fig.3. Reprezentarea schematica a transformarilor succesive a fazei metastabile si a fazei stabile (la echilibru)
Mecanismul
cristalizarii zeolitilor de tip ZSM-
cristalizarea indirecta a hidrogelului (din faza lichida, sinteza de tip A );
cristalizarea prin transformarea directa a hidrogelului (din faza solida, sinteza de tip B).
Cristalizarea se realizeaza preponderent dupa unul din mecanisme in functie de compozitia si natura substantelor initiale care formeaza hidrogelul (sursa de silice, raportul molar Si /Al, Al /Na + si (Si +Al) / R+ (Tabelul 3).
Tabelul 3. Influenta conditiilor de sinteza asupra unor caracteristici ale zeolitului ZSM-5.
|
Sinteza tip A |
Sinteza tip B |
|
|
Materii prime |
Al metalic, NaOH, SiO2 activ (solutie coloidala), (C3H7)4NOH (TPA) |
Al2(SO4)3·18H2O, silicat de sodiu (SiO2/Na2O = 3,34) (C3H7)4NBr |
|
Rapoarte molare: Si /Al Al / Na+ (Si + Al) /TPA+ H2O /(Si + Al) | ||
|
Conditii de sinteza: Temperatura, Timp de cristalizare, ore | ||
|
Dimensiunile cristalelor, |
Plecand de la silice activa, solutie de aluminat de sodiu si hidroxid de tetrapropilamoniu, sinteza zeolitului ZSM-5 are loc prin cristalizare din faza lichida (sinteza tip A). Solutia de silice in (C3H7)4OH este un amestec de silice coloidala si de anioni monosilicatici si polisilicatici. Pe de alta parte, solutia diluata de aluminat de sodiu contine specii monomerice Al(OH)4-. Prin amestecarea celor doua solutii se formeaza un gel aluminosilicatic bogat in Al, iar datorita depolimerizarii cu viteza mica a solului de silice, ionii silicat capabili sa condenseze cu speciile monomerice Al(OH)4- vor fi prezenti in concentratii mici.
Depolimerizarea continua care are loc de la suprafata particulelor de silice coloidala conduce la obtinerea ionilor silicat care formeaza imediat complexul aluminosilicatic insolubil pe suprafata particulelor de silice. In acest fel, particulele de silice coloidala sunt transformate intr-un sol hidratat de silice - alumina. Paralel se formeaza un numar limitat de nuclee de ioni silicat in solutie, iar odata cu cresterea numarului de nuclee incepe cresterea cristalelor. Consumarea ionilor silicat din solutie are loc prin dizolvarea continua a solului de silice -alumina. In jurul miezului (nucleului) bogat in siliciu al cristalelor se adauga alte straturi de siliciu - aluminiu, in felul acesta rezultand concentratii diferite de Al in cristalul format.
Mecanismul de tip A are loc in medii puternic alcaline. In acest caz, depolimerizarea silicei active la anionii silicat monomerici reprezinta etapa determinata de viteza. Ca rezultat se formeaza un numar redus de specii monomerice incarcate negativ. Aceste specii pot fie sa condenseze cu speciile aluminat cu formarea complecsilor aluminosilicat, fie sa interactioneze direct cu cationii Pr4N+ cu formarea unor unitati silicat (eventual aluminosilicat) bogate in siliciu care formeaza nucleie stabile. Este demonstrat ca in timpul cristalizarii ZSM-5 cresterea cristalelor are loc preferential pe seama Si. Prin urmare nucleiele vor creste cu o viteza mare, pe seama consumului speciilor dizolvate in solutii rezultate in urma dezagregarii fazei de gel.
Schema propusa pentru acest mecanism este redata in fig. 4.
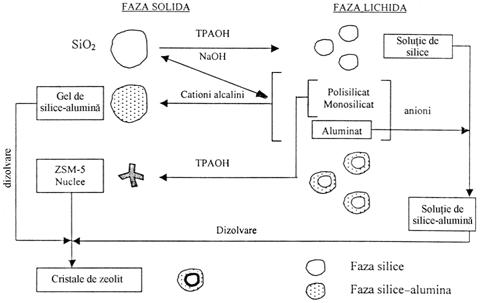
Fig.4. Reprezentarea mecanismului de sinteza a zeolitilor ZSM-5 prin transportul ionilor in faza lichida (sinteza tip A).
Plecand de la solutii apoase
de silicat de sodiu (ce contin deja speciile mono- sau oligomerice de
siliciu Si2O3(OH)![]() , Si3O3(OH)
, Si3O3(OH)![]() , Si4O8(OH)
, Si4O8(OH)![]() ) si sulfat de aluminiu in prezenta bromurii de
tetrapropilamoniu (sinteza tip B Tabelul 3), se formeaza un hidrogel
aluminosilicatic care contine cationii Na + si (C3H7)4N+.
Gelul format
avand aproximativ acelasi raport Si/Al ca cel corespunzator
reactantilor, nu mai participa la depolimerizare.
) si sulfat de aluminiu in prezenta bromurii de
tetrapropilamoniu (sinteza tip B Tabelul 3), se formeaza un hidrogel
aluminosilicatic care contine cationii Na + si (C3H7)4N+.
Gelul format
avand aproximativ acelasi raport Si/Al ca cel corespunzator
reactantilor, nu mai participa la depolimerizare.
In acest gel, are loc rapid formarea unui numar mare de nuclee prin interactia anionilor reactivi de silicat si aluminat cu cationii (C3H7)4N+. Reprezentarea mecanismului de sinteza a zeolitului ZSM-5 dupa sinteza tip B este redata in fig. 5.
Cristalizarea hidrogelului cu rapoarte Si/Al si Na/Si mari dupa sinteza tip B are loc cu viteza mare si conduce la cristale mici in care aluminiul este uniform distribuit. In general, un numar relativ mic de nuclee formate in solutie conduce la cristale mari de ZSM-5. Daca cristalele sunt mentinute mai mult timp in solutie, atunci poate avea loc formarea la exterior a Silicalitului-1.
Studii ulterioare au aratat ca aceste doua mecanisme nu se exclud ci au loc simultan, atat in faza de nucleere cat si in faza de cresterea a cristalelor.
In perioada de cristalizare prin sinteza tip A, raportul Si /Al nu se modifica, in timp ce prin sinteza tip B creste.
Putem spune ca prin sinteza tip A cristalizarea are loc prin consumarea ionilor din faza lichida, iar prin sinteza tip B are loc intre precursorii cristalini din faza de hidrogel, ceea ce explica diferenta dintre dimensiunile cristalelor formate precum si diferenta de compozitie din interiorul si exteriorul particulelor cristaline.
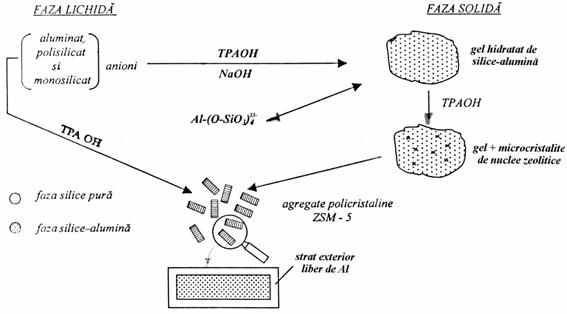
Fig. 5. Reprezentarea mecanismului de sinteza prin transformarea fazei solide (sinteza tip B).
Structura
retelei zeolitului ZSM-
c = 13,1 Ǻ. Parametrii
celulei elementare ortorombice reale a zeolitilor ZSM-5 avand formula |Na![]() (H2O)16| [AlnSi96-nO192]
cu n < 27 au valorile: a = 20,07Ǻ, b = 19,92 Ǻ, c = 13,42 Ǻ.
De asemenea a fost observata si simetria aparent monoclinica.
Drept unitate secundara de constructie ce contine inele 5-1 este
unitatea T12O24 (fig.
(H2O)16| [AlnSi96-nO192]
cu n < 27 au valorile: a = 20,07Ǻ, b = 19,92 Ǻ, c = 13,42 Ǻ.
De asemenea a fost observata si simetria aparent monoclinica.
Drept unitate secundara de constructie ce contine inele 5-1 este
unitatea T12O24 (fig.
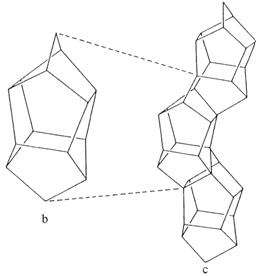 Prin legarea lanturilor in plan se obtine
structura bidimensionala a retelei, a carei proiectie este
reprezentata in fig. 7.
Prin legarea lanturilor in plan se obtine
structura bidimensionala a retelei, a carei proiectie este
reprezentata in fig. 7.
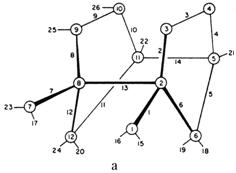
Fig. 6. Unitatea secundara de constructie ce contine inele 5-1 (a si b) si formarea lanturilor de tetraedre in reteaua zeolitului ZSM-5 (c)
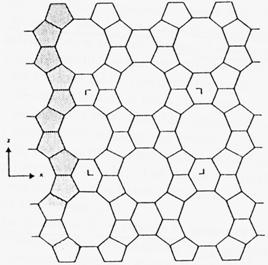
Fig. 7. Proiectia in plan a retelei ZSM-5 in care sunt reprezentate lanturile constructoare (hasurate)
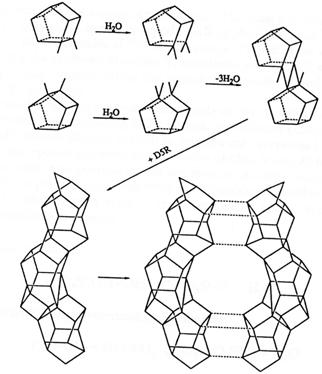 Inelele duble D5R identificate prin analiza Si-29
Inelele duble D5R identificate prin analiza Si-29
Fig.8. Formarea lanturilor pentasil prin polimerizarea /rearanjarea anionilor silicat D5R.
SB4 "dimeric" SBU condensare lant condensare start condensare strat
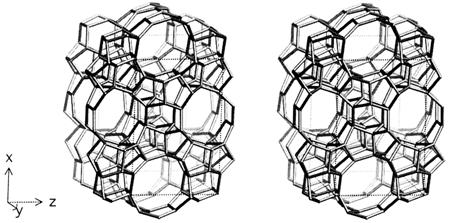 Topologia retelei
Topologia retelei
Fig. 9. Structura retelei ZSM-5 vazuta in directia [010]
In cadrul retelei tridimensionale se formeaza doua sisteme de canale intersectabile, unul sinusoidal si unul drept, a caror deschideri sunt date de inelul eliptic si de cel aproape circular de 10 atomi de oxigen (fig. II10).
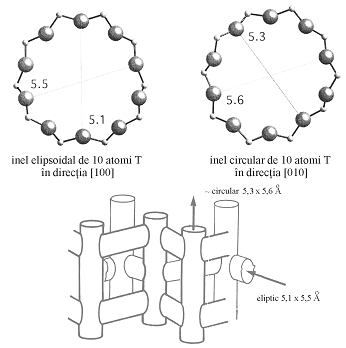
Fig. 10. Dimensiunile inelelor 10 T si sistemul de canale din zeolitul ZSM-5
Copyright © 2025 - Toate drepturile rezervate