 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
UNIVERSITATEA "TRANSILVANIA" BRASOV
Facultatea de Stiinta si Ingineria Materialelor
Specializarea Ingineria si Protectia Mediului in Industrie
Studiul termodinamic al reactiei dioxidului de seleniu cu carbonul cu formare de seleniu si manoxid de carbon
CAPITOLUL 1.NOTIUNI INTRODUCTIVE
Termodinamica studiaza fenomenele termice folosind marimi ce pot fi masurate direct (presiunea,volum,temperature) sau care pot fi calculate cu ajutorul altor marimi ce pot fi stabilite pe cale experimentala.
Termodinamica opereaza cu o serie de notiuni si marimi , cu ajutorul carora se defineste orice process sau fenomen termic.Una dintre acestea este notiunea de sistem temodinamic.
Sistemul temodinamic reprezinta un sistem fizic macroscopic ale carui dimenisiuni spatiale si existenta in timp permit efectuarea unor procese normale de masurare.
Carbonul
Este un element remarcabil din mai multe motive: printre formele sale diferite se afla una dintre cele mai moi (grafit) si una dintre cele mai dure(diamant).
Este unic prin proprietatile sale chimice pentru ca formeaza cel mai mare grup de combinatii,in special cu hidrogenul (compusi organici).Toate plantele si animalele sunt formate din combinatii complexe organice unde carbonul e combinat cu oxigenul,hidrogenul,azotul si alte elemente.
Carbonul este in general sigur,dar poate lua foc la temperaturi inalte si poate arde puternic (ca in accidental nuclear din Windscale,Marea Britanie,10 octombrie 1957).
Seleniu
Este un microelement antioxidant si se presupune si anticancerigen.In organism contribuie la realizarea respiratiei celulare,la protejarea hemoglobinei celulelor rosii,ca si la absorbtia si sporirea eficientei vitaminei E.
In cantitati mici se gaseste in diferite produse(mai ales de origine vegetala),ca de exemplu:ceapa,rosii,germeni de grau etc.
Excesul de selenium poate duce la orbire,paralizarea muschilor si tulburari respiratorii.Se foloseste in celule fotoelectrice,camere de filmat,la redresarea curentului electric,copiatoare etc.
Seleniul pur isi creste conductivitatea de o mie de ori cand este mutat de la intuneric la lumina solara puternica,lucru care il face utilizat la construirea luxumetrelor.
Monoxidul de carbon
Este o combinatie intre un atom de carbon si un atom de oxigen.
Este un gaz asfixiant,toxic,incolor si indoor,care ia nastere printr-o ardere(oxidare) incomplete a substantelor care contin carbon.
Acest proces are loc in cazul arderii la temperaturi inalte intr-un loc sarac in oxygen,formandu-se monoxide de carbon in locul dioxidului.Este un gaz inflamabil care arde cu flacara albastra,este otravitor.
Monoxidul de carbon este utilizat in metalurgie unde reactioneaza cu oxizii de fier; o parte din acesta ajunge in aer unde actioneaza ca poluant
Efectul toxic asupra organismului e determinat de reactia monoxidului de carbon cu hemoglobina din sange.
DATE NECESARE STUDIULUI TERMODINAMIC
Reactia studiata este:
SeO2(s) + 2C(s)→Se(s)+2CO(g)
In tabel sunt prezentate datele termodinamice necesare calculului:
Tabel 1. Date termodinamice
|
substanta |
H°f, 298 [kcal/mol] |
S°f, 298 [cal/mol·k] |
C°P=f(T) [cal/mol·k] |
T [k] |
||
|
a |
b·10³ |
c·10ˉ |
||||
|
SeO2(s) |
- |
- |
||||
|
C(s) | ||||||
|
Se(s) | ||||||
|
CO(g) |
47.18 | |||||
Unde: ∆H°f, 298 - caldura de formare standard
S°f, 298 - entropia de formare standard
C°p - capacitatea calorica molara la temperatura T = 298 [ k ] si presiunea p = 1 [atm ]
∆T - interval de temperatura pe care e valabila C°p = f ( T )
CAPITOLUL 2.
Trasformarea temperaturii de tranzitie de faza a substantelor principale in toate scarile termodinamice abordate.
Temperaturi:
Tabel 2. Formulele scarilor termodinamice
|
°C |
K |
°Re |
°F |
°R |
|
4/5·°C+0 |
9/5·°C+32 |
9/5·°C+491.67 |
Unde: °C=grade Celsius
K=grade Kelvin
°Re=grade Reanmur
°F=grade Farenheit
°R=grade Rankin
Trasformarea temperaturii de topire
Tabel 3. Exprimarea temperaturilor de topire ale substantelor din reactie
|
Substanta |
°C |
K |
°Re |
°F |
°R |
|
SeO2(s) |
272 |
644 | |||
|
C(s) |
| ||||
|
Se(s) | |||||
|
CO(g) |
Transformarea temperaturii de fierbere
Tabel 4. Exprimarea temperaturilor de fierbere ale substantelor din reactie
|
Substanta |
°C |
K |
°Re |
°F |
°R |
|
SeO2(s) |
- | ||||
|
C(s) | |||||
|
Se(s) | |||||
|
CO(g) |
CAPITOLUL 3.
CALCULUL ENTALPIEI DE REACTIE IN CONDITII STANDARD:
∆H°R,298
Entalpia de formare standard a unei substante reprezinta cantitatea de caldura cedata sau acceptata la formarea unui mol de substanta din element in stare standard.
Entalpia este o marime termodinamica egala cu suma dintre energia interna a unui corp si lucrul mecanic de deslocuire a volumului sau la o presiune constanta.
H = L+U =pV+U
Unde :
H - entalpia
U - energia interna
V - volumul molar al substantei la o presiune constanta
P - presiunea
L - lucrul mecanic
Unitatile de masura pentru entalpie sunt:
[ H ] = [ cal ], [ kcal ], [ kj ] ,[j]
n n
H°R,298 i H°f,p,298 j H°f,r,298
i=1 j=1
Pentru reactia studiata:
H R,298 i,Se H f,Se,298 i,CO H f,CO,298 jSeO2 H f,SeO2,298 jC H f,C,298
H R,298 =[(1·24.5+2·0)-(0+2·(-26.41)]=77.32[kcal/mol]
H R,298 =77.32[kcal/mol]
Entalpia de reactie fiind pozitiva ∆H°r,298>0 rezulta ca reactia este endoterma.
APRECIERI ASUPRA STABILITATII PARTICIPANTILOR LA REACTIE IN COMPARATIE CU ALTI COMPUSI DIN ACEEASI CLASA
Stiind ca orice sistem devine mai instabil daca are energia de formare mare,rezulta ca substantele caracterizate de entalpie de formare pozitiva vor fi instabile in timp ce substantele care au entalpie de formare negative cat mai indepartate de 0 vor fi stabile.
Tabel 5. Entalpiile standard de formare a altor compusi similari
|
Nr. crt. |
Substanta |
H R,298[kcal/mol] |
|
H SeO | ||
|
H SeO |
DETERMINAREA ECUATIEI DE DEPENDENTA A ENTALPIEI DE REACTIE IN FUNCTIE DE TEMPERATURA
Capacitatea calorica molara este cantitatea de caldura necesara unui mol de substanta pentru a-si creste temperatura cu un grad ,care are intotdeauna valoarea pozitiva ,deoarece incalzirea este un proces endoterm.
Formula generala la substante anorganice in functie de temperatura a capacitatii calorice molare pentru substante anorganice este:
C=a+bT+c/T²
HR,T CpdT
∆HR,T=∆a*T+∆b*T²/2-∆c*1/T+IH
IH=constanta de integrare
Unde: ∆a=∑ jap iar
∆b*10³=∑ jbp ibr
∆c*10ˉ jcp icr
Inlocuind in formule vom obtine:
∆a=(1*4.53+2*6.79)-(1*12.8+2*4.10)=-2.89 [cal/mol*k]
∆b=(1*5.50+2*0.11)-(1*6.1+2*1.02)=-2.42*10ˉ³[cal/mol*k]
∆c=2*(-0.11)-(2*-2.10)=3.98*10[cal/mol*k]
IH= ∆HR,T-∆a*T-∆b*T²/2+∆c*1/T
IH
IH=76765.01[cal/mol]
PARTICULARIZAREA SI TRASAREA GRAFICA A DEPENDENTEI ENTALPIEI LA TEMPERATURA DE 330K,530K,730K,930K PENTRU 1 MOL DE SUBSTANTA PRINCIPALA
Substanta principala: SeO
∆H°R,330=∆H°R,298+∆a*T│³³s +∆b/2*T²│³³s ∆c/T│³³s
∆H°R,330 *(1/330-1/298)]=77332.71[cal/mol]
∆H°R,330=77.35[kcal/mol]
∆H°R,530=∆H°R,298+∆a*T│ ³s +∆b/2*T²│ ³s ∆c/T│ ³s
∆H°R,530 *(1/530-1/298)]=77.23[kcal/mol]
∆H°R,730 *(1/730-1/298)]=76.82[kcal/mol]
∆H°R,930 *(1/930-1/298)]=76.40[kcal/mol]
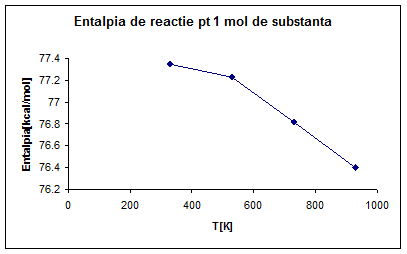
Fig.1 Entalpia de reactie pentru un mol de substanta
PARTICULARIZAREA SI TRASAREA GRAFICA A DEPENDENTEI ENTALPIEI LA TEMPERATURA DE 330K,530K,730K,930K PENTRU 200 KG DE SUBSTANTA PRINCIPALA.
Pentru 200kg de substanta principala: SeO
=m/M; MSeO2
=200*10³/111=1801.8 moli de SeO
Vom inmulti rezultatele obtinute pentru un mol de substanta cu 1801.8:
∆H°R,330=77.35*1801.8=139.369*10³[cal]=139.369[kcal]
∆H°R,530=77.23*1801.8=139.153[kcal]
∆H°R,730=76.82*1801.8=138.414[kcal]
∆H°R,930=76.40*1801.8=137.657[kcal]
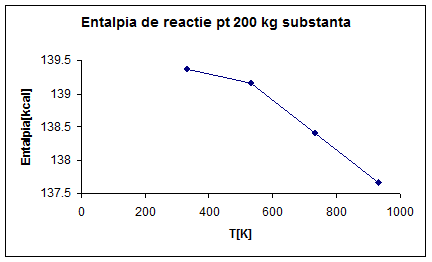
Fig 2. Entalpia de reactie pentru 200 kg substanta
CAPITOLUL 4.
CALCULUL ENTROPIEI DE REACTIE IN CONDITII STANDARD ∆S°R,298
Entropia este o functie termodinamica de stare care se ocupa cu masurarea spontaneitatii unei transformari.
Entropia este o marime fizica care caracterizeaza starea unui sistem fizico-chimic.
dS=dQT
Unde: S=entropia
Q=caldura
T=temperatura
Variatia de entropie poate fi definita intr-o reactie chimica astfel:
S°R,298 i S°f,p,298 j S°f,r,298
Pt reactia studiata:
S R,298 iSer S f,Se,298 iCOr S f,CO,298 jSeO2 ∆S f,SeO2,298 j,f,C S f,C,298
Unde: i j - coeficienti stoechiometrici
S f,p,298-entropiile de formare a produsilor de reactie
S f,r,298 entropiile de formare a reactantiilor de reactie
S R,298=(1·10.15+2· 47.18)-(1· 40.6+2·1.37)=61.17[cal/mol·K]
S>0 →proces posibil in sistem izolat.
APRECIERI CALITATIVE ASUPRA ENTROPIEI DE REACTIE IN CONDITII STANDARD
Se stie ca entropia de reactie intr-un sistem reprezinta starea de dezordine a particulelor,ea va avea valoare pozitiva, deoarece daca ar fi negativa nu ar avea sens.
Entropia unei transformari poate sa fie:
S>0 in sistem izolat,conditie de spontaneitate a transformarii
S<0 este proces imposibil intr-un sistem izolat
S=0este proces de echilibre
Atunci reactia studiata care are S=61.17>0[cal/mol*K] este un proces posibil in sistem izolat.
APRECIERI ASUPRA SPONTANEITATII REACTIEI
Se stie ca, conditia de spontaneitate a transformarilor in sistem izolat este aceea ca ∆S>0,lucru demonstrat si in cazul reactiei studiate. In functie de semnul de variatie al entalpiei si entropiei se pot face urmatoarele aprecieri asupra regimului termic al reactiei:
∆H>0 si ∆S>0 proces spontan numai la temperaturi mari
∆H>0 si∆S<0 proces imposibil
∆H<0 si ∆S<0 proces spontan la temperaturi reduse
∆H<0 si∆S>0 proces spontan la orice temperatura.
Pentru reactia studiata avem ∆H>0 si ∆S>0 ,din care va rezulta ca procesul este spontan numai la temperaturi mari.
DETERMINAREA ECUATIEI DE DEPENDENTA A ENTROPIEI DE REACTIE IN FUNCTIE DE TEMPERATURA
Pentru reactia studiata vom aplica urmatoarea relatie:
∆SR,T=∆a*lnT+∆b*T-∆c*1/2*T²+IS
Unde:
IS=
IS= ∆S°R,298-∆a*lnT-∆b*T+∆c*1/2*T²
IS=61.17+2.89*ln298+(-2.42)*10ˉ³*298-3.98*1/2*298²
IS=-176642.53 [cal/mol*k]
PARTICULARIZAREA SI TRASAREA GRAFICA A DEPENDENTEI ENTROPIEI LA TEMPERATURA DE 330K,530K,730K,930K PENTRU 1 MOL DE SUBSTANTA PRINCIPALA
Calculam:∆S°R=f(T)
Substanta principala: SeO
∆S°R,330= ∆S°R,298+ ∆a*lnT│³³s + ∆b*T│³³s -1/2* ∆c/T²│³³s
∆S°R,330=61.17+(-2.89*ln(330-298))+[-2.42*10ˉ³*(330-298)-1/2*[3.98*10*(1/330²-1/298²)= 51.49[cal/mol*k]
∆S°R,530=61.17+(-2.86*ln530-298)+[-2.42*10ˉ³*(530-298)]-1/2*[3.98*10*(1/530²-1/298²)]=47.52[cal/mol*k]
∆S°R,730=61.17+(-2.86*ln730-298)+[-2.42*10ˉ³*(730-298)]-1/2*[3.98*10 *(1/730²-1/298²)]=44.45[cal/mol*]
∆S°R,930=61.17+(-2.86*ln930-298)+[-2.42*10ˉ³*(930-298)]-1/2*[3.98*10*(1/930²-1/298²)]=41.00[cal/mol*k]
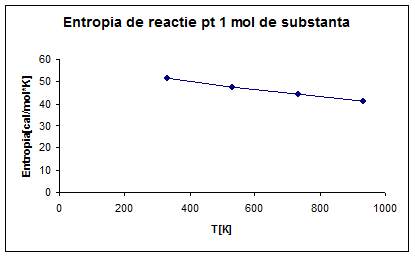
Fig. 3 Entalpia de reactie pentru un mol de substanta
PARTICULARIZAREA SI TRASAREA GRAFICA A DEPENDENTEI ENTROPIEI LA TEMPERATURA DE 330K,530K,730K,930K PENTRU 200 KG DE SUBSTANTA PRINCIPALA. REPREZENTARE GRAFICA.
Pentru 200kg de substanta principala: SeO
Vom inmulti rezultatele obtinute pentru un mol de substanta cu 1801.8
∆S°R,330=51.49*1801.8=92.774[kcal/K]
∆S°R,530=47.52*1801.8=85.621[kcal/K]
∆S°R,730=44.45*1801.8=80.090[kcal/K]
∆S°R,930=41.00*1801.8=73.873[kcal/K]
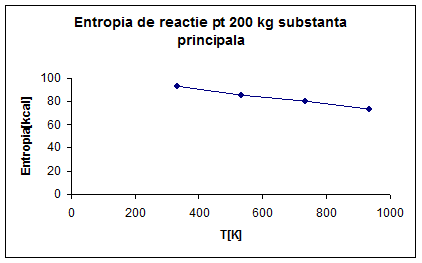
Fig 4. Entropia de reactie pentru 200 kg substanta principala
CAPITOLUL 5.
CALCULUL ENERGIEI LIBERE GIBBS:
Energia libera Gibbs se poate calcula in functie de entalpia si entropia de reactie in conditii standard cu urmatoarea formula:
G R,298 H R,298-T S R,298
Unde avem: ∆S°R,298=61.17[cal/mol*K]
∆H°R,298=77.32*10³[cal/mol]
T=298[k]
∆G°R,298=77.32*10³-298*61.17=59.091*10³[cal/mol]
APRECIERI ASUPRA SPONTANEITATII REACTIEI IN SISTEM IZOLAT SI NEIZOLAT
Se pot face aprecieri asupra regimului termic al reactiei in functie de semnul de variatie al entalpiei si entropiei procesului astfel:
H>0 si S>0 → proces spontan la temperaturi mari
H>0 si S<0 → proces imposibil
H<0 si S>0 → proces spontan la orice temperaturi
H<0 si S<0 → proces spontan la temperaturi reduse
Pentru reactia studiata H>0 si S>0 .Rezulta deci ca procesul e spontan la temperaturi mari.
DETERMINAREA ECUATIEI DE DEPENDENTA A ENERGIEI LIBERE GIBBS IN FUNCTIE DE TEMPERATURA
Dependenta de temperatura a energiei libere se poate determina calculand:
HR,T CpdT
∆HR,T=∆a*T+∆B*T²/2-∆C*1/T+IH
∆G=-∆a*T*lnT-∆b/2*T²-∆c/2*T+IH+IG*T
IG=∆G°R,298/T+∆a*lnT+∆b*T/2-∆c*1/2*T²-IH/T
IG=59.091*10³/298+(-2.89*ln298)+(-2.42*10ˉ³*298/2)-(3.98*10
IG=-78.88[cal]
PARTICULARIZAREA SI TRASAREA GRAFICA A DEPENDENTEI ENERGIEI LIBERE GIBBS LA TEMPERATURILE DE 330K,530K,730K,930K PENTRU 1 MOL DE SUBSTANTA PRINCIPALA.
Calculul ∆G°R,T=f(T)
Substanta principala: SeO
∆G°R,330=∆H°R,330+330*∆S°R,330
∆G°R,330=77.35+330*51.49=17.06[kcal/mol]
∆G°R,530=77.23+530*47.52=25.26[kcal/mol]
∆G°R,730=76.82+730*44.45=32.52[cal/mol]
∆G°R,930=76.40+930*41.00=38.20[kcal/mol]
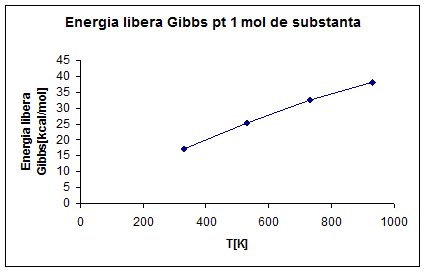
Fig 5. Energia libera Gibbs pentru un mol de substanta
PARTICULARIZAREA SI TRASAREA GRAFICA A DEPENDENTEI ENERGIEI LIBERE GIBBS LA TEMPERATURA DE 330K,530K,730K,930K PENTRU 200 KG DE SUBSTANTA PRINCIPALA.
Pentru 200kg de substanta principala: SeO
Vom inmulti rezultatele obtinute pentru un mol de substanta cu 1801.8
∆G°R,330=17.06*10³*1801.8=307.387*10[cal]
∆G°R,530=25.26*10³*1801.8=455.134*10[cal]
∆G°R,730= [cal]
∆G°R,930= [cal]
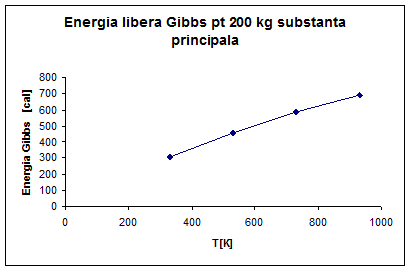
Fig 6. Energia libera Gibbs pentru un 200 kg substanta principala
CALCULUL AFINITATII DE REACTIE A°R,298
Scaderea energiei libere a sistemului este egala cu lucrul mecanic maxim reversibil pe care un sistem poate sa-l efectueze in cadrul unei transformari.
Acest lucru se numeste afinitate si se calculeaza cu relatiile :
A=- G pentru p=constant
A=- F pentru v=constant
∆G°R,298=59.091*10³[cal/mol]
Rezulta :
A°R,298 =-∆G°R,298
A°R,298=-59.091*10³[cal/mol]
Unde:
A°R,298=afinitatea de reactie la presiunea p=1[atm] si temperatura de T=298
CONCLUZII
Aceasta analiza termodinamica ofera informatii referitoare la stabilitatea compusilor din categoria sulfatilor,care avand entalpiile de reactie positive in conditii standard,sunt substante instabile.
Deasemeni,in urma acestui studiu termodinamic putem mentiona urmatoarele concluzii:
deoarece:
∆H R,T>0 rezulta ca reactia este una endoterma;
S R,T>0 rezulta ca procesul e spontan la orice temperaturi in sistem izolat.
BIBLIOGRAFIE
1.Handbook of Chemistry and Physics
2.Gavril
Niac-Formule,Tabele si Probleme de chimie fizica,editura
3.Silvia Patachia-Curs
de Chimie fizica,Reprografia Universitatii 'Transilvania'
4.Silvia Patachia-Ghid pentru realizarea si prezentarea unui raport stiintific in chimie,Lux-Libris.
Copyright © 2025 - Toate drepturile rezervate