 | Alimentatie | Asistenta sociala | Frumusete | Medicina | Medicina veterinara | Retete |
CARACTERIZAREA BIOCOMPOZITELOR LIPOZOMI / POLIPEPTIDUL ANTICANCERIGEN BORTEZOMIB
Cancerul, boala care are un mecanism de proliferare celulara anarhica și necontrolata, continua sa fie una dintre cele mai grave boli, alaturi de cele cardiovasculare, cu care se confrunta omenirea. Terapiile moderne utilizate in oncologie pot conduce la distrugerea cu succes a tumorilor, permițand o recuperare rapida a pacientului daca diagnosticarea este realizata timpuriu.
Protein turnover reprezinta echilibrul intre sinteza proteinei și degradarea ei și este esențiala pentru funcționarea normala a celulelor [Shringarpure R., Davies K.J.A., 2002 Proteazomul este un complex proteic avand principala func ie de degradare a proteinelor inutile prin procesul de proteoliza [Adams J., 2003], [Maldonado M., Wang J., 2007]. Capacitatea proteazomului de a degrada proteinele tumorale este dereglata in multe tumori maligne, oferind motivația pentru alegerea sa ca ținta pentru terapia cancerului [Crawford L.J. și colab., 2011 Kisselev A.F, Goldberg A.F., 2001], [Cvek B., Dvorak Z., 2008], [Ruggeri B. și colab., 2009]. Exista o mare varietate de inhibitori proteazomali naturali, cei mai mulți dintre ei fiind oligopeptide. Dintre aceștia, peptide boronates [Adams J. și colab., 1998], epoxomicin [Groll M. și colab., 2000] și lactacystin [Groll M. și colab., 2008] au o specificitate mare pentru proteazom și prin urmare reprezinta o perspectiva pentru proiectarea și dezvoltarea medicamentelor.
Studiile preclinice au evidențiat diferite efecte ale agentului bortezomib, precum perturbarea ciclului celular al celulelor maligne și inducerea apoptozei, modificarea micromediului maduvei osoase și inhibarea proteazomilor [Blaney S. M. și colab., 2004], [Richardson P. G. și colab., 2003]. Prin blocarea proteazomului, bortezomibul perturba numeroase cai biologice, inclusiv cele legate de creșterea și supraviețuirea celulelor canceroase. Astfel, provoaca o intarziere in creșterea tumorii
Transportul la ținta prezinta o importanța deosebita in cazul administrarii agenților terapeutici din clasa peptidelor și proteinelor, incapsularea lor in vectori de transport imbunatațind randamentul terapiei.
Avand in vedere toate acestea, un alt obiectiv al acestei lucrari este obținerea și caracterizarea biocompozitelor lipozomi/polipeptidul bortezomib. Pentru aceasta, in prima etapa a fost realizata caracterizarea electrochimica a acestui medicament prin voltametrie ciclica, voltametria cu puls diferențial și voltametrie cu unda patratica și s-a propus un model atat pentru mecanismul de oxidare, cat și pentru mecanismul de reducere al agentului la suprafața electrodului de carbon vitros.
Intr-o a doua etapa, s-a realizat evaluarea eficienței de incapsulare a bortezomibului in lipozomii preformați, prin investigarea a 2 parametri (raportul molar medicament:lipid și pH-mediului) .
La realizarea acestui obiectiv pentru prepararea lipozomilor s-a utilizat lipidul DPPC (1,2-dipalmitoyl-sn-glycero-3-phosphocholine). Lipozomii au fost preparati prin metoda simplei hidratari a filmului lipidic, iar pentru optimizarea eficientei incapsularii, s-a creat un gradient transmembranar de pH, obtinandu-se o diferenta de pH intre mediul intern apos al lipozomilor (pH 8.2) si mediul exter (pH 6) in care lipozomii se afla in suspensie.
Biocompozitele au fost obținute prin mixarea unei soluții de bortezomib cu lipozomii SUV, rapoartele molare medicament: lipide DPPC fiind de 1:15; 1:10; 1:7; 1:5. Complexele au fost incubate la 47 0C timp de 8 ore.
Bortezomib is the first therapeutic agent designed to inhibit mainly the activity of the 26S proteasome. It is used for the treatment of multiple myeloma and other cancers such as lung, ovarian, renal, colorectal cancer, and not only. The objective of this study is to developing and optimizing liposomal formulation of bortezomib anticancer drug in order to improve the encapsulation efficiency. Liposomes were prepared from DPPC lipids using two methods: the conventional thin-film hydration technique and a pH gradient method. The encapsulation efficiency was of optimized by the investigation of the influence of various drug:lipids molar ratios during 8 hours of incubation bortezomib molecules with the preformed liposomes. Based on the obtained results, also was calculated the binding constant of the drug to the DPPC lipids in both cases of liposomes preparation. The data demonstrate that the highest encapsulation efficiency was obtained for drug:lipids molar ratios 1:7, and in the case of liposomal preparation by the pH-gradient method the encapsulation efficiency was with 15% greater than when using the conventional thin-film hydration technique.
1. Aspecte generale privind polipeptidul bortezomib
Bortezomib, denumit și PS-341 sau Velcade de catre Millennium Pharmaceuticals, este un oligopeptid care conține acid pirazinoic, fenilalanina și leucina, avand acid boronic in locul acidului carboxilic. Formula chimica este [(1R)-3-Methyl-1-[[(2S)-1-oxo -3-phenyl-2-[(pyrazinylcarbonyl) amino]propyl]amino]butyl]-boronic acid, iar structura chimica este reprezentata in schema urmatoare:
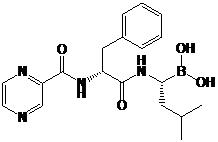
Schema 1. Structura chimica a oligopeptidului bortezomib [www.drugbank.ca]
Este un agent terapeutic relativ nou, ce prezinta efecte antitumorale prin inhibarea cu precadere a proteazomului 26 S. Acest proteazom este un complex enzimatic ce se gasește in nucleul și citoplasma tuturor celulelor. Rolul sau este de a degrada proteinele de care se leaga ubiquitina, prin calea metabolica ubiquitin proteazomala Inhibarea acestui proteazom afecteaza celulele canceroase, avand ca rezultat stoparea ciclului celular și conducand in final la apoptoza lor C. Lu, 2006
Substanța activa bortezomib este primul inhibitor proteazomal aprobat de catre US Food and Drug Administration (FDA) and the European Agency for the Evaluation of Medicinal Products (EMEA) pentru tratarea mielomului multiplu și a limfoamelor maligne non-Hodgkins [Richardson P. G. și colab., 2003], [Mazumder A., 2008], [Abraham J., 2009], [Mitsiades C. S. și colab., 2007], A. Mahindra, 2010 M. Venkataramanna, 2012 Datorita succesului observat in tratarea acestor boli, cercetarea asupra agentului bortezomib a fost extinsa și in profilaxia altor tipuri de cancer.
Astfel, bortezomib este utilizat ca agent terapeutic in cancerul pulmonar [Schenkein D. P., 2005], limfomul Non-Hodgkin [Holkova B., Grant S., 2012], și cancerul pancreatic [Awasthi N. și colab., 2010].
Cu toate ca are o eficiența mare, agentul anticancerigen prezinta totuși reacții adverse, precum un grad moderat de oboseala, varsaturi, febra, anemie, scaderea apetitului alimentar [Frankland-Searby S., Bhaumik S.R., 2012]. In vederea depașirii acestor inconveniente, au fost dezvoltate diferite strategii, cum ar fi combinarea bortezomibului cu diferite medicamente precum temozolomide [Kubicek G. J. și colab., 2009] și analogi nucleozidici [Hung S.W. și colab., 2012]. Ca urmare, exista o nevoie continua pentru determinarea farmacocineticii bortezomibului, astfel incat aspecte precum interacțiile medicament - medicament, sau medicament - complexe biomoleculare, sa poata fi evaluate [Venkatakrishnan K. și colab., 2009]. O mai buna ințelegere a comportamentului inhibitor este esențiala pentru a imbunatați raspunsul la tratament și pentru a identifica noi combinații de terapii atat pentru mieloamele multiple cat și pentru alte boli maligne. Fiind un medicament relativ nou, nu sunt inca disponibile in literatura de specialitate metodologii analitice pentru cuantificarea bortezomibului. Prin urmare, pentru a sprijini studiile farmacocinetice, sunt necesare proceduri analitice adecvate.
Investigarea electrochimica permite explicarea proceselor biologice, in timp ce interfața dintre electrod și soluția analizata reprezinta un model excelent pentru simularea și clarificarea mecanismelor de interacție dintre biomolecule [Oliveira-Brett A.M. și colab., 2006 Diculescu V.C. și colab., 2006 Intrucat acest agent anticancerigen participa in cadrul unor reacții redox in mediul intracelular, scopul acestui studiu a fost investigarea proprietaților de transfer de electroni ale bortezomibului. Astfel, a fost studiat comportamentul redox la suprafața electrodului de carbon vitros intr-un interval mare al valorilor pH-ului și utilizand tehnicile electrochimice- voltametria ciclica, voltametria cu puls diferențial și voltametria cu unda patratica.
2. Caracterizarea electrochimica a polipeptidului bortezomib
2.1. Materiale și metode
Medicamentul anticancerigen bortezomib obținut de la Millennium Pharmaceuticals, a fost utilizat fara o purificare suplimentara. Concentrațiile dorite au fost obținute prin diluția unei cantitați corespunzatoare din soluția stoc, direct in electrolitul suport aflat in celula electrochimica.
Toate experimentele au fost realizate la temperatura camerei (25 ± 1 sC). Probele au fost preparate in soluții de electroliți cu forța ionica 0.1 M, Tabel 1, utilizand reactivi cu grad de puritate analitica și apa purificata cu sistem Milli - Q (conductivitate < 0.1 S cm-1).
Tabel 1. Solutii de electroliti, forta ionica 0.1 M
|
pH |
CompoziȚie |
|
HCl + KCl |
|
|
HAcO + NaAcO |
|
|
HAcO + NaAcO |
|
|
HAcO + NaAcO |
|
|
NaH2PO4 + Na2HPO4 |
|
|
NaH2PO4 + Na2HPO4 |
|
|
NaH2PO4 + Na2HPO4 |
|
|
NH3 + NH4Cl |
|
|
NH3 + NH4Cl |
|
|
NaOH + KCl |
Pentru inregistrarea voltamogramelor in domeniul negativ de valori (reducere), au fost obtinute solutii saturate cu azot prin barbotare N2 de inalta puritate, timp de minim 10 minute in solutie. In timpul experimentelor, pentru a evita difuzarea oxigenului atmosferic in interiorul probelor, s-a menținut un flux constant de N2 deasupra soluției de electroliți. Masuratorile de pH au fost realizate cu ajutorul unui pH-metru Crison micropH 2001 cu electrod de sticla Ingold.
Parametrii voltametrici
Toate voltamogramele au fost inregistrate cu ajutorul unui potențiostat IVIUM, Figura 1, ce ruleaza cu software-ul IviumSoft 1.922, Olanda. Masuratorile au fost realizate cu ajutorul unui sistem de 3 electrozi: electrodul de lucru - electrod de carbon vitros (glassy carbon electrod) cu diametrul de 1 mm, un electrod de referința Ag/AgCl (3 M KCl) și un electrod auxiliar (contraelectrod) confecționat din platina. S-a utilizat o celula electrochimica cu un volum de 0.5 mL.

Figura 1. Potențiostat Ivium compact [www.ivium.nl]
Condițiile experimentale pentru voltametria ciclica au fost: incrementul potențialului 2 mV și viteza de scanare 100 mV s-1, iar pentru voltametria cu puls diferențial (DPV) au fost: amplitudinea pulsului - 50 mV, durata pulsului -100 ms, viteza de scanare de 5 mV s-1. Pentru voltametria cu unda patrata (SWV), condițiile experimentale au fost: frecvența pulsurilor - 10, 25 și respectiv 50 Hz, amplitudinea pulsului - 50 mV și incrementul potențialului 2 mV.
Inaintea inregistrarii fiecarei voltamograme, electrodul de carbon vitros a fost curațat cu ajutorul unui spray cu particule de diamant Kemet (marimea particulelor 3 µm). Dupa curațare, electrodul clatit cu apa ultrapura Milli-Q a fost introdus in soluția de electroliți inregistrandu-se 2 - 3 voltamograme inaintea obținerii unei linii de baza corecte. Aceasta procedura conduce la obținerea unor rezultate experimentale reproductibile.
Achiziția și prelucrarea datelor voltametrice
Corecția voltamogramelor a fost realizata prin eliminarea liniei de baza utilizand programul IviumSoft 1.922. Acest tratament matematic imbunatateste identificarea și vizualizarea picurilor fara a introduce nici un artefact, desi inaltimea picurilor este, in unele cazuri redusa <10%), comparativ cu cea a picurilor din voltamogramele necorectate [V. C. Diculescu și colab., 2010 Cu toate acestea, acest tratament matematic al voltamogramelor originale a fost folosit in prezentarea tuturor voltamogramelor pentru o mai clara identificare a picurilor. In toate graficele prezentate, valorile intensitaților picurilor au fost determinate din voltamogramele originale necorectate cu linia de baza.
Determinarea ariei electroactive a electrodului de carbon vitros
In studiile de electrochimie, se opereaza nu numai cu parametri funcționali, ci și cu o serie de parametri constructivi care vizeaza, de cele mai multe ori, natura, forma și dimensiunile electrozilor de lucru. Astfel, masuratorile au fost realizate cu ajutorul unui electrod de carbon vitros cu diametrul de 1 mm, a carui arie electroactiva a fost determinata.
Pentru aceasta s-a utilizat o soluție de ferocianat 1 mM, pH 6.96, al carui coeficient de difuzie este cunoscut, iar metoda de analiza a fost voltametria ciclica.
Aria electroactiva a electrodului de carbon vitros s-a determinat conform urmatoarei ecuații valabile pentru un sistem reversibil:
![]() (1)
(1)
unde n este numarul de electroni, A aria electroactiva a electrodului (cm2), D0 coeficientul de difuzie 7.35X10 -6 cm2s-1, [F] concentrația soluției de ferocianat (mol x cm-3), iar v viteza de scanare.
S-au efectuat cate 2 masuratori pentru fiecare viteza de scanare.
Tabel 2. Tabel valori IPA in functie de viteza de scanare
|
v mV s |
Ipa (X10-6) (A) |
Ipa (X10-6)(A) |
|
0.025 |
1.72 |
1.897 |
|
0.05 |
2.149 |
2.132 |
|
0.075 |
2.44 |
2.534 |
|
0.1 |
2.508 |
2.736 |
|
0.125 |
2.724 |
2.816 |
|
0.15 |
3.022 |
2.922 |
|
0.175 |
2.96 |
3.124 |
|
0.2 |
3.012 |
3.267 |
|
0.25 |
3.357 |
3.525 |
|
0.3 |
3.737 |
3.536 |
|
0.35 |
3.749 |
3.873 |
|
0.4 |
4.261 |
4.124 |
|
0.45 |
4.333 |
4.204 |
|
0.5 |
4.453 |
4.291 |

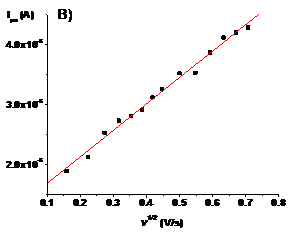
Figura 2. Reprezentarea grafica a intensitații funcție de patratul vitezei de scanare
A) prima masuratoare; B) a doua masuratoare
Cu ajutorul pantelor dreptelor (I/v1/2) s-a calculat aria electroactiva ca fiind 0.00523 cm2.
2.2. Comportamentul electrochimic al polipeptidului bortezomib
Comportamentul electrochimic al bortezomibului la suprafața electrodului de carbon vitros a fost investigata in pH 7.0, potențialul fiind cuprins intre +1.40 V și - 1.20 V. Voltamogramele ciclice au fost obținute intr-o soluție saturata cu N2 de bortezomib de concentrație 1.3 × 10-3 M, Figura 3. In timpul masuratorilor voltametrice, un flux constant de N2 a fost pastrat deasupra soluției, cu scopul de a evita difuzia oxigenului atmosferic in soluția de bortezomib.
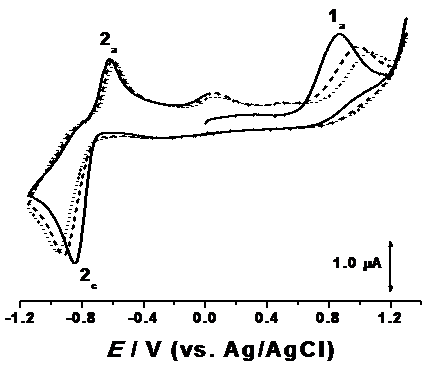
Figure 3. Voltamograme ciclice corectate cu linia de baza, inregistrate intr-o soluție de M bortezomib, pH = 7.0, v = 100 mV s-1, (▬) primul scan, ( ) al doilea scan și (...) al treilea scan
Inregistrarea potențialului a inceput de la 0.00 V catre limita pozitiva și a fost observat un singur pic de oxidare 1a. Atunci cand scanarea s-a realizat spre domeniul negativ de valori, a fost observat un singur pic de reducere 2c, iar dupa schimbarea direcției de scanare a primei voltamograme, un pic anodic corespondent 2a a fost observat.
De asemenea, au fost inregistrate voltamogramele ciclice pornind de la potențialul 0.00 V spre valori negative, observandu-se un comportament similar. Deoarece procesele de oxidare și reducere al bortezomibului la suprafața electrodului de carbon vitros au loc independent, acestea au fost studiate separat.
1.3.1.Oxidarea la suprafața electrodului de carbon vitros
Voltametria ciclica (CV)
Oxidarea bortezomibului la suprafața electrodului, a fost inițial studiata prin voltametrie ciclica (CV), utilizand o soluție de concentrație 1.3 × 10-3 M, intr-un domeniu de pH al electrolitului suport cuprins intre 2.0 și 12.0, 0.1 M.
La pH 7.00, in prima voltamograma inregistrata de la potențialul 0.0 V catre limita potențialului pozitiv + 1.4 V, apare un singur pic de oxidare 1a la Epa + 0.95 V, datorat oxidarii bortezomibului, Figura 4.A. Dupa schimbarea direcției de inregistrare a voltamogramei, nu apare nici un pic catodic corespondent, ceea ce indica faptul ca procesul de oxidare al polipeptidului este ireversibil.
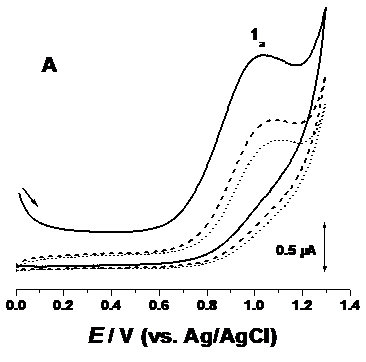
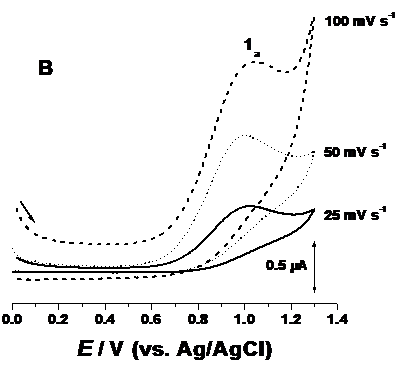
Figura 4. Voltamograme ciclice corectate cu linia de baza, inregistrate intr-o soluție de 1.3 × 10-3 M bortezomib, pH 7.0, A) (▬) primul scan, ( ) al doilea scan și (...) al treilea scan, n = 100 mV s-1; B) primul scan la diferite viteze de scanare
Inregistrand scani succesivi fara a curața suprafața electrodului de lucru, Figura 4.A, valoarea intensitații picului 1a scade datorita adsorbției produsului de oxidare al bortezomibului la suprafața GCE. Nici un pic anodic adițional nu apare la inregistrarea scanilor succesivi, acest lucru demonstrand faptul ca produșii de oxidare rezultați in urma oxidarii bortezomibului nu sunt electroactivi.
De asemenea, voltamograme ciclice au fost inregistrate la diferite viteze de scanare, Figura 4.B. Intre masuratori, suprafața electrodului de lucru a fost intotdeauna curațata, pentru a evita posibilele probleme datorate adsorbției produsului de oxidare al bortezomibului. Prin creșterea vitezei de scanare, picul 1a s-a deplasat catre valori pozitive ale potențialului. Diferența dintre potențialul picurilor și potențialele lor la jumatatea inalțimilor este Epa - Epa/2 αan') ~ 110 mV [Brett C. M. A., Oliveira-Brett A. M., 1993], [Compton R.G., Banks C.E., 2011], astfel αan Considerand αa = 0.5 [Compton R.G., Banks C.E., 2011], s-a calculat numarul de electroni transferați ca fiind n' = 1. In soluțiile de electroliți cu valori diferite ale pH-ului, un comportament similar a fost observat, dar potențialul picului 1a este dependent de pH-ul electrolitului suport.
Voltametria cu puls diferențial ( DPV)
De asemenea, oxidarea electrochimica a polipeptidului bortezomib a fost studiata intr-un domeniu de valori ale pH-ului cuprins intre 2 și 12, taria ionica 0.1 M, utilizand voltametria cu puls diferențial, Figura 5.A. Pentru pH < 3.4 și pH > 9.2 nu a fost observat nici un pic de oxidare chiar și la concentrații mai mari, ceea ce arata faptul ca polipeptidul nu se oxideaza la suprafața electrodului in aceste condiții. Pentru domeniul de pH cuprins intre 3.0 și 9.2, in voltamogramele DP apare un singur pic de oxidare 1a.


Figura 5. A) Graficul 3D al voltamogramelor de puls diferențial corectate cu linia de baza și inregistrate in domeniul anodic intr-o soluție de 2.6 × 10-4 M bortezomibin funcție de pH-ul electrolitului; B) Dependența Ep1a a picului de oxidare al bortezomib-ului in funcție de pH-ul electrolitului
Pentru pH < 7.5, potențialul picului 1a s-a deplasat catre valori negative odata cu creșterea valorii pH-ului, Figura 5.B. Pentru acest domeniu de valori ale pH-ului dependența Epa = f(pH) este liniara și respecta relația
![]() (2)
(2)
Panta dreptei, 60 mV/unitate, sugereaza faptul ca mecanismul de oxidare al oligopeptidului implica transferul aceluiași numar de electroni și protoni.
In plus, largimea la jumatatea inalțimii
picului este intotdeauna ![]() , fiind mult
mai mare decat valoarea teoretica pentru o reacție electrochimica reversibila
care implica transferul unui singur electron. Valoarea lui W poate fi explicata prin aceea ca oxidarea
electrochimica (picul 1a) a fost urmata de o reacție
chimica omogena - dimerizare, cu adsorbția dimerilor la
suprafața electrodului de carbon vitros. Procesul de
oxidare al dimerilor bortezomibului are loc la potențiale mari, ducand la
suprapunerea picurilor datorate oxidarii acestora și picurile
datorate oxidarii bortezomibului.
, fiind mult
mai mare decat valoarea teoretica pentru o reacție electrochimica reversibila
care implica transferul unui singur electron. Valoarea lui W poate fi explicata prin aceea ca oxidarea
electrochimica (picul 1a) a fost urmata de o reacție
chimica omogena - dimerizare, cu adsorbția dimerilor la
suprafața electrodului de carbon vitros. Procesul de
oxidare al dimerilor bortezomibului are loc la potențiale mari, ducand la
suprapunerea picurilor datorate oxidarii acestora și picurile
datorate oxidarii bortezomibului.
Pentru soluțiile de electroliți avand 7.5 < pH < 9.2, picul 1a este independent de pH, Figura 5.B, fiind caracteristic pentru o reacție electrochimica care implica transferul doar a unui electron, permițand determinarea valorii pKa pentru bortezomib ~7.5.
De asemenea, au fost inregistrate voltamograme DP succesive intr-o soluție de bortezomib de concentrație 0.26 mM, tampon fosfat pH = 7.0. La prima scanare apare un singur pic de oxidare la potențialul Ep1a = + 0.77 V, Figura 6. La inregistrarea celei de a doua voltamograme DP, obținuta in aceleași condiții, fara curațarea suprafeței electrodului de lucru, valoarea intensitații picului 1a scade, datorita adsorbției produșilor de oxidare ai bortezomibului la suprafața electrodului de lucru. In același timp, potențialul picului 1a s-a deplasat la Epa = + 0.82 V. Largimea la jumatatea inalțimii picului este W ~ 95 mV, specifica unei reacții electrochimice care implica transferul unui singur electron. Odata cu creșterea numarului de scani, intensitatea picului scade, dar potențialul ramane constant. Adsorbția produșilor de oxidare ai bortezomibului la suprafața electrodului de lucru a fost demonstrata prin inregistrarea succesiva a voltamogramelor DP in soluție, electrodul fiind spalat cu un jet de apa deionizata și introdus in celula electrochimica ce conține doar electrolitul. Voltamogramele DP inregistrate in aceste condiții, arata doar picul la potentialul Epa = + 0.82 V, Figura 6.

Figura 6. Voltamograme DP corectate cu linia de baza inregistrate intr-o soluție de bortezomib
0.26 mM, tampon acetate pH = 5.4, (▬) primul scan, ( ) al doilea scan, (...) al treilea scan si ( ) primul scan dupa transferarea electrodului in electrolit
Voltametria cu unda patratica
Voltamogramele cu unda patratica obținute pentru o soluție de bortezomib de concentrație 2.6 × 10-4 M, pH 5.03 și 7.0, Figurile 6.A și B arata un comportament al polipeptidului similar cu cel inregistrat in cadrul voltamogramelor ciclice și cu puls diferențial. Astfel, prin inregistrarea curentului direct și curentului invers, s-a subliniat inca o data comportamentul ireversibil al mecanismului de oxidare al agentului terapeutic, intrucat curentul invers nu prezinta nici un pic de reducere.
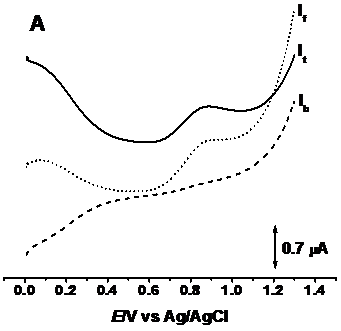
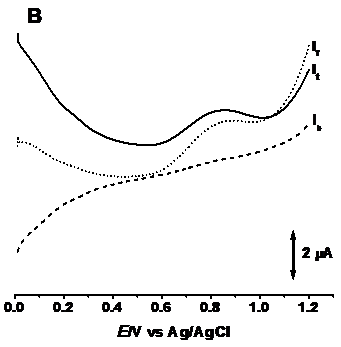
Figura 6. Voltamograme cu unda patratica inregistrate intr-o soluție de 2.6 × 10-4 M bortezomib: A) pH 5.03, B) pH 7.0, f = 25 Hz, It - curentul total, If - curent direct, Ib - curent invers, amplitudinea pulsului 50 mV, f = 10 Hz, v = 20 mV s-1
Au fost inregistrate voltamograme SW succesive intr-o soluție de bortezomib de concentrație 2.6 × 10-4 M, in tampon acetat pH = 5.03, Figura 8. In cadrul inregistrarii primei voltamograme, picul 1a apare la potențialul Ep1a = + 0.85 V. Odata cu creșterea numarului de scani, intensitatea picului 1a scade, potențialul este deplasat catre valori mai pozitive si apar noi picuri de oxidare picul 3a, la potențialul Ep3a = + 0.55 V, și picul 4a, la potențialul Ep4a = + 1.03 V. Aceste noi picuri sunt datorate oxidarii produșilor de oxidare ai bortezomibului formați la suprafața electrodului de lucru și acumulați in timpul scanarilor anterioare.
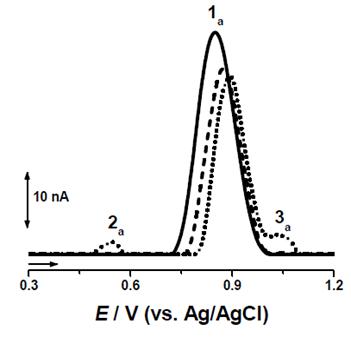
Figura 8.Voltamograme cu unda patratica corectate cu linia de baza, inregistrate intr-o soluție de bortezomib 0.26 mM, tampon acetate pH = 5.4, (▬) primul scan, ( ) al doilea scan și (...) al treilea scan, amplitudinea pulsului 50 mV, f = 10 Hz, v = 20 mV
1.3.2. Reducerea la suprafața electrodului de carbon vitros
Voltametria ciclica (CV)
In cadrul acestor experimente, reducerea polipeptidului la suprafața electrodului de lucru a fost mai intai studiata pentru o soluție de concentrație 1.3 × 10-3 M bortezomib, pH 7.0, 0.1 M, in care a fost barbotat N2 pana la saturare. In prima voltamograma inregistrata de la potențialul 0.0 V catre potențialul limita de detecție al electrodului de carbon vitros - 1.3 V, apare un singur pic de reducere 2c la Ep2c = - 0.87 V, ceea ce se poate traduce prin faptul ca in aceste condiții experimentale, polipeptidul se reduce la suprafața electrodului, Figura 7.A. Dupa schimbarea direcției de scanare, apare un pic anodic corespondent 2a la potențialul Ep2a = - 0.63 V. Diferența dintre valorile intensitaților și ale potențialelor celor doua picuri 2c și 2a corespunde unei reacții cvasi-reversible.
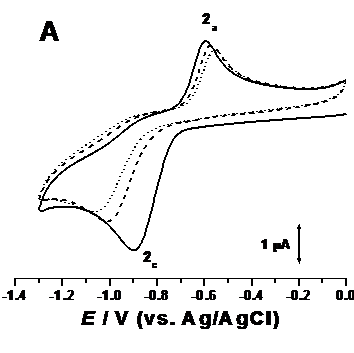

Figura 7. Voltamogramele ciclice corectate cu linia de baza, obținute pentru o soluție de 1.3 × 10-3 M bortezomib, pH 7.0: A) (▬) primul scan, ( ) al doilea scan și (...) al treilea scan, n = 100 mV s-1 și B) primul scan la diferite viteze de scanare
Utilizand aceeași soluție și inregistrand scani succesivi fara a curața suprafața electrodului de lucru, se observa scaderea intensitaților corespunzatoare picurilor 2c, in timp ce valoarea potențialului se deplaseaza catre valori negative, Figura 7.A. Acest lucru se datoreaza formarii produșilor de reacție care raman adsorbiți la suprafața electrodului, reducandu-i aria electroactiva. In același timp, nu a fost observat nici un pic nou, aratand faptul ca produșii de reducere formați, nu sunt electroactivi.
De asemenea, au fost inregistrate voltamograme ciclice pentru o soluție de concentrație 1.3 × 10-3 M bortezomib saturata cu N2, pH 7.0, 0.1 M, la diferite viteze de scanare, Figura 7.B. Intre masuratori, suprafața electrodului de lucru a fost intotdeauna curațata pentru a evita eventualele probleme legate de adsorbția produșilor la suprafața electrodului. Marind viteza de scanare, valoarea intensitații picului 2c crește liniar cu v1/2.
Se observa ca odata cu creșterea vitezei de scanare, valoarea potențialului picului catodic 2c a suferit o ușoara deplasare catre valori mai negative, iar diferența dintre potențialul picului Ep2c și potențialul la jumatatea inalțimii picului Ep2c/2 este aproximativ 90 mV.
![]() (3)
(3)
Intrucat pentru un sistem ireversibil este valabila ecuația
![]() (4)
(4)
unde, ![]() este coeficientul catodic de
transfer de sarcina,
este coeficientul catodic de
transfer de sarcina, ![]() numarul de electroni, poate fi
calculat factorul
numarul de electroni, poate fi
calculat factorul ![]()
Intensitatea picului masurata in amperi pentru un sistem ireversibil este data de ecuația 5:
![]() (5)
(5)
unde, n este numarul de electroni transferați in timpul procesului de reducere, A este aria electroactiva a electrodului de lucru (cm2), D este coeficientul de difuzie masurat in cm2 s-1, C este concentrația in mol cm-3, iar v este viteza de inregistrare masurata in V s-1.
Prin trasarea graficului Ipc=f(v1/2) și considerand n = 2, calculat cu ajutorul voltametriei cu puls diferențial, pentru soluția de bortezomib in pH 7.0, a fost determinata valoarea coeficientului de difuzie. Aria electroactiva a GCE a fost calculata in secțiunea A = 5.0 × 10-3 cm2.
In urma masurarii valorii
pantei dreptei![]() , a fost calculata valoarea coeficientului de difuzie
, a fost calculata valoarea coeficientului de difuzie ![]()
Voltametria cu puls diferențial ( DPV)
De asemenea, mecanismul de reducere al bortezomibului la suprafața electrodului de carbon a fost studiat intr-un domeniu mare al pH-ului cuprins intre 2 și 12 prin voltametrie cu puls diferențial. Toate voltamogramele DP au fost inregistrate utilizand soluții de bortezomib de concentrație 6.5 × 10-5 M, saturate cu N2. In cazul tuturor soluțiilor de electroliți studiate, apare un singur pic de reducere 2c dependent de pH, Figura 8.A. S-a remarcat faptul ca intensitatea picului este mai mare la pH 7.0 - tampon fosfat.
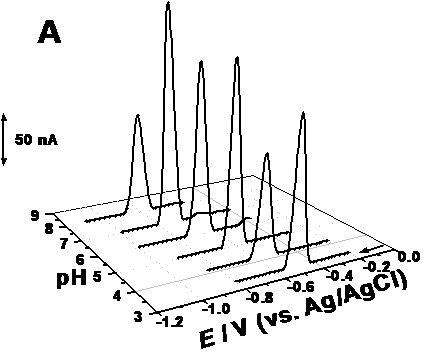
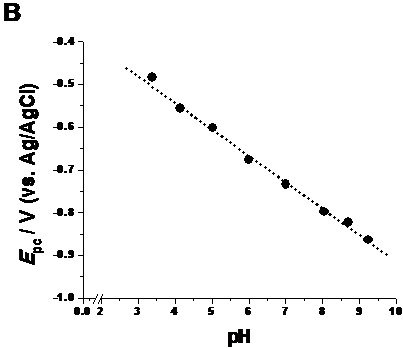
Figura 8. A) Graficul 3D al voltamogramelor cu puls diferențial corectate cu linia de baza, obținute pentru o soluție de 6.5 × 10-5 M bortezomib redus la suprafața electrodului de lucru in funcție de pH-ul electrolitului; B) Dependența Ep2a a picului de reducere al bortezomib-ului in funcție de pH-ul electrolitului
Odata cu creșterea pH-ului, se observa o deplasare a valorii potențialului picului de reducere catre valori mai negative și o dependența liniara intre Ep și pH, Figura 8.B, conform ecuației:
![]() (6)
(6)
Valoarea pantei dreptei, - 60 mV/ unitate pH, sugereaza faptul ca mecanismul de reducere al polipeptidului bortezomib implica transferul aceluiași numar de electroni și protoni. Valoarea largimii la jumatatea inalțimii picului catodic W1/2 = 60 mV, apropiata de valoarea teoretica pentru transferul a doi electroni, sugereaza faptul ca procesul de reducere al agentului anticancerigen se realizeaza prin transferarea a doi electroni și a doi protoni.
Voltametria cu unda patratica (SWV)
Contrar, in cazul voltamogramei inregistrata in pH 8.0, Figura 9.B, valorile intensitaților celor doi curenți, direct și respectiv indirect, sunt egale și sunt inregistrate la același potențial, indicand faptul ca in mediu alcalin, procesul de reducere al bortezomibului este reversibil.

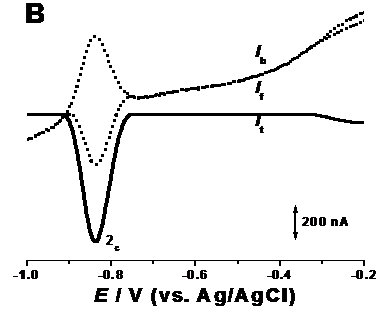
Figura 9. Voltamograme cu unda patratica corectate cu linia de baza și inregistrate pentru o soluție de 6.5 × 10-5M bortezomib saturata cu N2 și redusa la suprafața electrodului de lucru; A) pH 3.4;B) pH 8.0,
It - curentul total, If - curent direct, Ib - curent invers, amplitudinea pulsului 50 mV, f = 10 Hz, v = 20 mVs-1
1.3.3. Mecanismul redox
Rezultatele obținute au aratat faptul ca procesul de oxidare al bortezomibul la suprafața electrodului de carbon vitros are loc intr-o singura etapa, așa cum s-a indicat prin inregistrarea unui singur pic de oxidare in direcția pozitiva de scanare, Figurile 4. și 5. Mecanismul de oxidare al oligopeptidului este ireversibil, Figura 4, și corespunde electro-oxidarii aminei secundare alifatice. Pentru pH < 7.5, procesul de oxidare implica transferul unui singur electron și a unui proton, Figura , conducand la formarea unui radical, Schema 2.A, care poate fi supus procesului de dimerizare. Oxidarea dimerilor bortezomibului a fost observata prin voltametrie cu unda patratica Figura 8, și are loc la potențiale mai mari, picul 4a. In soluții de electroliți cu pH > 7.5, bortezomib sufera deprotonare chimica și mecanismul sau de oxidare implica transferul unui singur electron, insa a nici unui proton, Figura 5.B. Acest mecanism de oxidare este propus prin comparare cu mecanismul de oxidare al compușilor ce conțin amine secundare [Adenier A. și colab., 2004], [Garrido J.M.P.J. și colab., 2004].
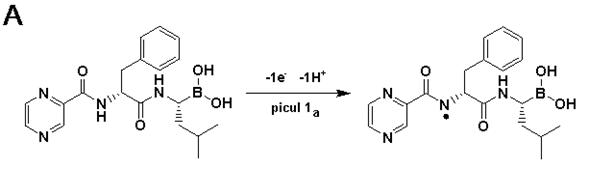
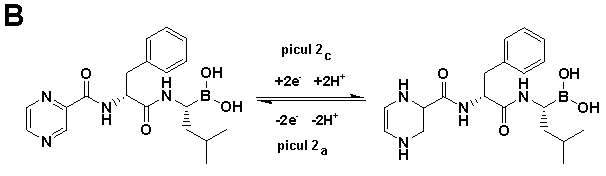
Schema 2. A) Mecanismul de oxidare și B) reducere al bortezomibului propus
Pe de alta parte, mecanismul de reducere al medicamentului bortezomib la suprafața electrodului de carbon vitros, are loc intr-o singura etapa, așa cum s-a indicat prin inregistrarea unui singur pic de reducere in direcția negativa de scanare, Figura 7. Procesul de reducere este cvasi-reversibil și implica transferul a doi electroni și respectiv a doi protoni, Figura 8. Reacția electrochimica are loc la inelul pirazin conducand la formarea unui derivat dihidro, Schema 2.B, similar compușilor ce conțin the pyrazine moiety [Pontinha A.D.R. și colab., 2012], [Diculescu V.C. și colab., 2010]. Așa cum s-a observat, utilizand voltametria cu unda patratica, Figura 9.B, in mediu alcalin mecanismul de reducere al bortezomibului devine reversibil.
3. Dezvoltarea sistemelor de livrare lipozomale pentru polipeptidul anticancerigen bortezomib
Transportul substantelor active, incapsulate in sisteme de transport, la celulele tinta pot furniza multiple avantaje, de exemplu, micsorarea toxicitatii medicamentelor, alterarea proprietatilor farmacocinetice sau imbunatatirea solubilitatii medicamentului [P. G. Richardson, 2003]. Cercetarile actuale din domeniul tehnologiei farmaceutice urmaresc proiectarea si dezvoltarea unor "vehicule" de livrare a agentilor terapeutici, precum si realizarea unor strategii de cedare controlata a acestora in vecinatatea receptorilor biologici tinta. Principalul obiectiv al sistemelor de transport al medicamentelor este acela de a ceda medicamentul eficient si specific la locul tinta si de a minimiza efectele toxice ale agentilor terapeutici.
In acest sens, aplicatiile lipozomilor atat ca modele de membrane artificiale, cat si ca sisteme de cedare controlata a agentilor au cresut.
Lipozomii sunt intens studiati ca "drug delivery system" intrucat au abilitatea de a incorpora si de a proteja multe tipuri de biomolecule terapeutice atat in bistratul lipidic cat si in mediul intern apos. Selectarea protocolului de incapsulare este in mare masura dictata de aspecte precum eficienta de incapsulare si de retinere a substantei active, raportul medicament: lipid, usurinta prepararii, eficienta costurilor, stabilitatea lipozomilor, si nu numai U. D. Shivhare, 2009]. Tehnicile de preparare a veziculelor lipozomale propuse in literatura sunt conceptual distincte, niciuna dintre acestea ne fiind utilizata ca o procedura universala.
Principalul obiectiv al acestui studiu a fost investigarea . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . ..
2.1. Materiale și metode
1,2-dipalmitoyl-sn-glycero-3-phosphocholine (DPPC) procurat de la Avanti Polar si medicamentul bortezomib procurat de la Millennium Pharmaceuticals au fost utilizate fara o purificare suplimentara. Pentru masuratorile de fluorescenta, lipozomii SUV au fost marcati cu fluoroforul 1,6 - diphenyl - 1,3,5 - hexatriene (DPH), raportul molar lipid/fluorofor fiind Structura chimica a lipidului DPPC este reprezentata in schema urmatoare.
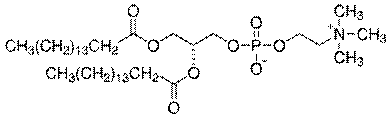
Schema 1. Structura chimica a lipidului DPPC [www.sigmaaldrich.com]
Achizitia si prelucrarea datelor
Experimentele de spectrofluorimetrie au fost realizate cu ajutorul unui spectrometru de fluorescenta Perkin Elmer LS 55 echipat cu un accesoriu biocinetic prevazut cu senzor de temperatura. Rezultatele au fost importate si prelucrate cu ajutorul programului Origin 8. Spectrele de emisie au fost inregistrate atat la lungimea de unda de excitatie a bortezomibului ex = 265 nm) utilizand urmatorii parametrii: fanta de excitatie - 10 nm; fanta de emisie - 15 nm; viteza de scanare 10 nm/minut; cat si la lungimea de unda de excitatie a fluoroforului DPH ( ex = 356 nm), setarile softului fiind: fanta de excitatie - 10 nm; fanta de emisie -5 nm; viteza de scanare 100 nm/minut. Toate experimentele au fost realizate la 47 sC.
Prepararea lipozomilor
Lipozomii au fost preparati utilizand metoda simplei hidratari a filmului lipidic [12, 13], adaptata corespunzator pentru realizarea obiectivelor propuse. Pentru hidratarea filmelor lipidice s-a folosit o solutie de tampon fosfat, pH 7.2, concentratie 60 mM. Pe scurt, fosfolipidele DPPC (concentratie finala 0.3 mM in suspensia de lipozomi) au fost dizolvate in metanol. Solventul a fost apoi evaporat cu ajutorul unui evaporator rotativ Heidolph (~ 30 minute la temperatura T = 47 0C, viteza de rotatie 150 rpm), pentru a forma un film lipidic pe fundul si pe peretii balonului. Dupa aceasta etapa, filmul lipidic a fost hidratat (~ o ora) cu solutia de tampon fosfat si agitat mecanic cu ajutorului unui agitator magnetic. Veziculele unilamelare (SUV) au fost obtinute prin sonicare (30 minute, amplitudine 30 %), utilizand un sonicator Vibra-Cell VCX 750 avand diametrul sondei 0.13 cm. Pentru a obtine o populatie omogena de vezicule unilamelare mici, suspensia a fost centrifugata timp de 30 de minute, 12 000 g.
Pentru a optimiza eficienta incapsularii s-a preparat o suspensie de lipozomi prin crearea unui gradient transmembranar de pH, obtinandu-se o diferenta de pH intre mediul interior al lipozomilor (pH 8.2) si mediul exterior (pH 6) in care lipozomii se afla in suspensie.
Incarcarea medicamentelor in lipozomii
Studiile din literatura de specialitate au aratat faptul ca tehnicile de incarcare activa a agentilor terapeutici au condus la obtinerea unor rezultate mult mai bune privind eficienta de incapsulare, in comparatie cu tehnica de inglobare pasiva, in care medicamentul este incapsulat in lipozomi in timpul procesului de preparare a acestora, mai precis in etapa de hidratare.
Luand in considerare rezultatele din literatura, in cadrul acestui experiment s-a optat pentru incarcarea activa a medicamentului in lipozomi.
Incapsularea moleculelor de bortezomib in veziculele lipozomale s-a realizat prin mixarea solutiei de bortezomib cu suspensia de lipozomi SUV, rapoartele molare bortezomib: lipide DPPC fiind: 1:15; 1:10; 1:7; 1:5. Experimentele au fost realizate la temperatura de 47 0C.
Pentru a inlatura posibilele erori datorate adeziunii lipidelor la suprafata peretilor celulei de masura si pentru obtinerea unui randament de incapsulare cat mai mare, proba a fost agitata riguros pe tot timpul masuratorilor, cu ajutorul sistemului de agitare cu care este prevazut spectrofluorimetrul Perkin Elmer LS 55.
Eficienta de incapsulare a fost calculata raportand cantitatea de medicament incapsulat la cantitatea de medicament total, utilizand urmatoarea ecuatie U. D. Shivhare L. N. Ramana, 2010
![]() (1)
(1)
De asemenea, pe baza modificarilor semnalului de fluorescenta la lungimea de unda corespunzatoare maximului emisiei bortezomibului inglobat in lipozomi, .
3. Studierea interacției dintre lipide și polipeptidul bortezomib
In cadrul acestor studii s-a urmarit cuantificarea si optimizarea procesului de incapsulare a agentului anticancerigen bortezomib in vectorii de transport - lipozomi, prin evaluarea eficientei de incapsulare si a constantei de legare a medicametului de fosfolipidele aflate in compozitia lipozomilor.
Eficienta de incapsulare in lipozomi este guvernata de abilitatea prepararii acestor vezicule in vederea inglobarii intr-un procent cat mai mare si retinerii moleculelor de medicament pe o perioada cat mai lunga de timp.
S-a evaluat influenta raportului molar medicament:lipid asupra eficientei incapsularii prin masurarea intensitatii relative a fluorescentei atat in urma excitarii la λex a medicamentului, cat si la λex a fluoroforului. Diferite cantitati de medicament (de la 20 la 60 M) au fost adaugate in suspensia lipozomala de concentratie 0.3 mM in scopul de a obtine diferite rapoarte molare 1:15, 1:10, 1:7, 1:5.
Medicamentul bortezomib (30 M) in mediu apos, in urma excitarii la lungimea de unda ex = 265 nm, prezinta o emisie fluorescenta slaba la em = 420 nm, fiind caracteristica acidului boronic [..], Figura V.X.
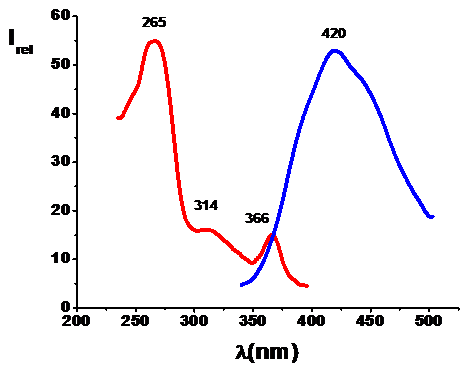
Figura V.X. Spectrul de excitatie si de emisie al bortezomib-ului, 42 μM, tampon fosfat pH 7.2
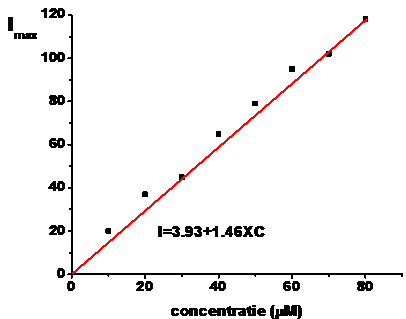
Figura V.X. Dependenta Imax, inregistrata la λem bortezomib, de concentratia bortezomibului
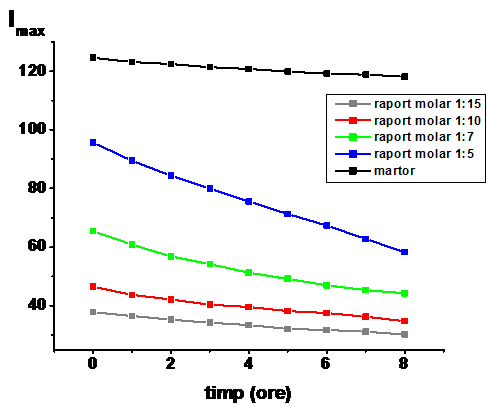
Figura V. X. Evolutia Imax
inregistrat la λem bortezomib in functie de timpul de incubare;
(![]() )
Evolutia in timp a solutiei de bortezomibului de concentratie 80 μM
)
Evolutia in timp a solutiei de bortezomibului de concentratie 80 μM
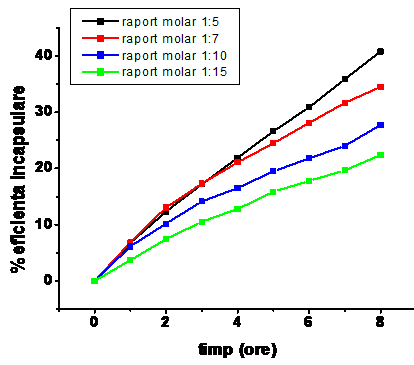
Figura V.X. Eficienta incapsulare in functie de timpul de incubare obtinuta in cazul masuratorilor realizate la lungimea de unda de emisie a bortezomibului
Asa cum se arata in Figures 1. A) and B), eficienta de inglobare a fost redusa in cazul rapoartelor molare 1:15 (30 %) si 1:10 (50 %) bortezomib:lipid. Eficienta maxima de incapsulare (aproximativ 70 %) a medicamentului in lipozomi s-a determinat pentru raportul molar 1:7 medicament:lipid DPPC, complexul fiind incubat la 47 0C timp de 8 ore. In cazul raportului molar 1:5 s-a obtinut o eficienta de incapsulare ceva mai mica (67 %) fata de cazul in care s-a utilizat raportul 1:7.
Rezultatele obtinute privind eficienta de incapsulare a medicamentului in lipozomi indica faptul ca, cresterea concentratiei de fosfolipide (in cazul rapoartelor molare de la 1:7 la 1:15) conduce la scaderea eficientei de incapsulare. Acest lucru se datoreaza faptului ca pentru concentratia de medicament utilizata, moleculele de fosfolipide sunt in exces. In acelasi timp, continutul scazut de fosfolipide (in cazul raportului molar 1:5) furnizeaza capacitate limitata de incapsulare.
In Figura V.X) este prezentata evolutia in timp a intensitatii maxime a fluorescentei fluoroforul DPH cu care lipozomii DPPC au fost marcati. Emisia fluorescenta se datoreaza moleculelor fluoroforului inserate in bistratul lipidic [J. R. Lakowicz, 2006]. Se observa faptul ca dupa aproximativ 30 minute intervine o stabilitate, din acest moment fiind realizate in continuare experimentele. De asemenea timp de 8 ore nu se inregistreaza modificari majore ale emisiei fluorescente a DPH-ului, rezultatele nefiind influentate de o posibila degradare a acestuia.
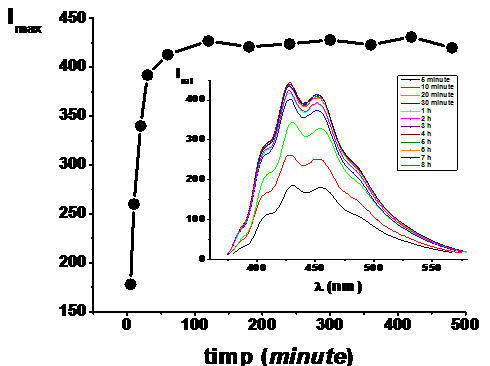
Figura V.X. Evolutia in timp a maximului intensitatii fluorescentei fluoroforului DPH cu care lipozomii DPPC sunt marcati
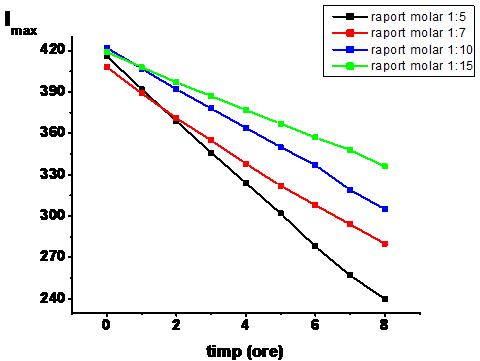
Figura X. Imax functie de timpul de incubare inregistrat la λem DPH
Maximul emisiei fluorescente a DPH-ului in prezenta bortezomibului scade in timp astfel, se poate spune faptul ca polipeptidul actioneaza ca stingator al fluorescentei DPH-ului in lipozomi, stingerea respectand ecuatia Stern - Volmer [Lakowicz..]
![]() (X)
(X)
![]() (X)
(X)
unde, I0 si I reprezinta intensitatile fluorescentei in absenta si respectiv in prezenta stingatorului (bortezomib), KSV reprezinta constanta Stern - Volmer, Kq - constanta bimoleculara de stingere a fluorescentei, τ0 este timpul de viata al fluorescentei DPH-ului in absenta bortezomibului iar [B] reprezinta concentratia bortezomibului.
In figura urmatoare este reprezentata grafica ecuatia Stern-Volmer pentru lipozomi DPPC marcati cu fluoroforul DPH in prezenta bortezomibului aflat in diferite concentratii

Figura X. Reprezentarea grafica a ecuatiei Stern-Volmer pentru lipozomi DPPC marcati cu fluoroforul DPH in prezenta bortezomibului aflat in diferite concentratii
In urma reprezentarii grafice a ecuatiei Stern-Volmer s-a obtinut o dependenta liniara intre raportul intensitatilor fluorescentei in absenta si respectiv in prezenta stingatorului si concentratia bortezomibului. Aceasta liniaritate indica fraptul ca fluoroforul DPH este accesibil stingatorului - bortezomib [.]. Utilizand valorile pantelor dreptelor s-a calculat valoarea constantei Stern - Volmer KSV, Tabel X, pentru fiecare timp de incubare a lipozomilor SUV cu polipeptidul bortezomib. De asemenea s-a calculat valoarea constantei bimoleculare de stingere a fluorescentei Kq pentru fiecare timp de incubare, tinand cont de faptul ca timpul de viata al fluorescentei DPH-ului in absenta bortezomibului este 10 ns [.], Tabel X.
Tabel X. Constanta Stern-Volmer si constanta bimoleculara de stingere a fluorescentei pentru lipozomii DPPC marcati cu fluoroforul DPH
|
Timp (ore) |
Constanta Stern-Volmer Ksv (x 104 M-1) |
Constanta bimoleculara Kq x1012 M-1s |
Conform datelor din literatura stingerea dinamica datorata proceselor de coliziune este caracterizata de o valoare a constantei bimoleculare de stingere a fluorescentei in domeniul 1010 M-1s-1. .
Prin urmare, in urma valorilor obtinute pentru constanta bimoleculara de stingere a fluorescentei pentru lipozomii DPPC marcati cu fluoroforul DPH se pot concluziona urmatoarele:
in intervalul 1 - 5 ore de incubare a solutiei de bortezomib cu lipozomii SUV DPPC stingerea fluorescentei se datoreaza unor procese de ciocnire intre fluorofor si bortezomib
incepand cu a 6-a ora de incubare formarea complexului poate fi responsabila de stingerea fluorescentei.
sau formarii unui complex intre acestia.
Ulterior s-a incercat inglobarea medicamentului in lipozomii preparati prin crearea unui gradient de pH. Incarcarea s-a realizat la raportul molar bortezomib:lipid 1:7, raport la care s-a obtinut cea mai buna eficienta de incapsulare in experimentele anterioare.
Interesant este faptul ca a fost observata o crestere semnificativa a acumularii medicamentului in vectorii de transport, ca raspuns la crearea gradientului de pH. Dupa cum se observa in Figurile X A) si B), scaderea valorii pH-ului in mediul extern conduce la cresterea eficientei de incapsulare a bortezomibului.
In acest caz medicamentul s-a acumulat mult mai rapid in lipozomi, eficienta de incapsulare fiind de 60 % dupa 3 ore de incubare, iar dupa 8 ore - 85 %. Eficienta de incapsulare in final a fost cu 15 % mai mare decat in cazul prepararii lipozomilor prin metoda conventionala.
Tinand cont de structura sa chimica, in mediul apos extern medicamentul este neincarcat electric datorita mediului usor acid. In aceasta stare neincarcata, si datorita gradientului transmembranar de pH, compusul este liber sa difuzeze prin bistratul lipidic, acumulandu-se in compartimentul intern apos al lipozomilor mult mai rapid.
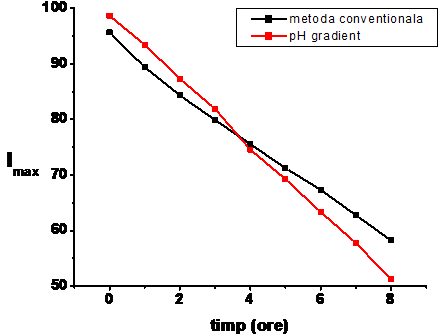
Imax vs incubation time recorded at λem DPH in the case of liposomes prepared by conventional thin-film hydration method and SUV liposomes that presenting a pH gradient across the liposomal membrane
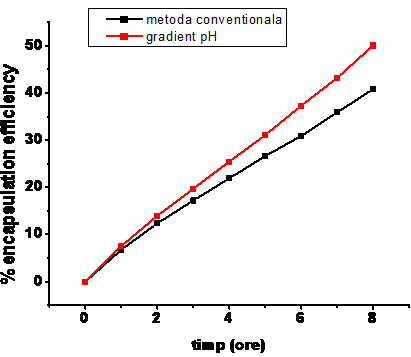
Comparison of encapsulating efficiency for bortezomib encapsulated in liposomes prepared by conventional thin-film hydration method and in SUV liposomes that presenting a pH gradient across the liposomal membrane
Concluzii
Studiile realizate asupra mecanismelor de oxidare și reducere ale agentului anticancerigen bortezomib, furnizeaza informații utile legate de reacțiile redox suferite de aceasta clasa de molecule, conducand la o mai buna intelegere a sistemelor biologice și la creșterea cunostințelor de ansamblu legate de mecanismul fiziologic de acțiune a polipeptidului.
Comportamentul redox al oligopeptidului bortezomib a fost studiat intr-un domeniu mare al pH-ului cu ajutorul tehnicilor: voltametrie ciclica, voltametrie cu puls diferențial și voltametrie cu unda patratica.
S-a aratat faptul ca mecanismele de oxidare și reducere ale agentului anticancerigen sunt independente. Astfel, oxidarea este un proces ireversibil și in soluții de electroliți cu pH < 7.5 implica transferul unui singur electron și a unui singur proton. In medii alcaline, bortezomib sufera deprotonare chimica și procesul sau de oxidare implica doar transferul unui singur electron. Reducerea bortezomibului la suprafața electrodului de lucru este un proces cvasi-reversibil, dependent de pH, și implica transferul a doi electroni și respectiv doi protoni. In cazul soluțiilor alcaline, mecanismul de reducere devine reversibil. De asemenea, au fost stabiliți centrii electroactivi ai bortezomibului și a fost propus mecanismul redox.
The present study demonstrates the influence of the drug:lipid molar ratio and of the transmembrane pH gradient on the encapsulation efficiency of bortezomib anticancer drug into the preformed liposomes. Based on the obtained results, it was found that the anticancer drug bortezomib have been successfully encapsulated into liposomes by using a pH difference between the internal aqueous medium (pH 8.2) and external aqueous medium (pH 6), in which the liposomes are suspended. Also was tested four molar ratio drug:lipid (1:15, 1:10, 1:7, 1:5), determining the maximum of the encapsulation efficiency (~ 70 %) of the bortezomib into liposomes for the molar ratio 1:7 drug:DPPC lipid, the complex being incubated for 8 hours at 47 0C
References
[1] L. Zhang, J. E. Littlejohn, Y. Cui, X. Cao, C. Peddaboina1, W. R. Smythe, Molecular Cancer
[2] C. Lu, R. Gallegos, P. Li, C. Q. Xia, S. Pusalkar, V. Uttamsingh, D. Nix, G. T. Miwa, L. S. Gan, Drug Metabolism And Disposition 34, 4 (2006)
[3]. F. Hsieh, E. Tengstrand, T. Pekol, R. Guerciolini, G. Miwa, Journal of Pharmaceutical and Biomedical Analysis 49, 1 (2009)
[4] A. Mazumder, Community Oncology 5, 9 (2008)
[5] J. Abraham, Community Oncology 6, 2 (2009)
[6] A. Mahindra, T. Hideshima, K. C. Anderson, Blood Reviews 2010
[7] M. Venkataramanna, K. S. Babub, K. A. A. Sulaiman, Journal of Pharmaceutical Sciences 2, 1 (2012)
[8] J. Menashe, Commun Oncol 4, (2007)
[9] S. M. Blaney, M. Bernstein, K. Neville, J. Ginsberg, B. Kitchen, T. Horton, S. L. Berg, M. Krailo, P. C. Adamson, Journal of Clinical Oncology 22, 23 (2004)
[10 P. G.
[11] U. D. Shivhare, D. U. Ambulkar, V. B. Mathur, K. P. Bhusari, M. D. Godbole, Digest Journal of Nanomaterials and Biostructures 4, 4 (2009)
[12] M. R. Mozafari, Cellular & Molecular Biology Letters 10, (2005)
[13] M. Riaz,
[14] L. N. Ramana, S. Sethuraman, U. Ranga, U. M Krishnan, Journal of Biomedical Science 17, 57 (2010)
[15] H. Mojzisova,
[16] A. Kunwar, A. Barik, K. I. Priyadarsini, R. Pandey, Barc Newsletter 285, (2007)
J. R. Lakowicz, Principles of Fluorescence Spectroscopy. Third Edition, Springer (2006)
Referințe
R. Shringarpure, K.J.A. Davies, Protein turnover by the proteasome in aging and disease, Free Radical Bio. Med., 32 (2002) 1084-1089.
[2] J. Adams, The proteasome: structure, function, and role in the cell, Cancer Treat. Rev., 29 (2003) 3-9.
M. Maldonado, J. Wang, Proteosome, In:
Encyclopedia of Stress (Second Edition), Ed. George Fink, Academic Press,
L.J. Crawford, B. Walker, A.E. Irvine, Proteasome inhibitors in cancer therapy, J Cell Commun Signal
A.F. Kisselev, A.F. Goldberg, Proteasome inhibitors: from research tools to drug candidates, Chem Biol, 8 (2001) 739-758.
B. Cvek, Z. Dvorak, The value of proteasome inhibition in cancer: Can the old drug, disulfiram, have a bright new future as a novel proteasome inhibitor?, Drug Discov Today, 13 (2008) 716-722
B. Ruggeri, S. Miknyoczki, B. Dorsey, A. Hui, The Development and Pharmacology of Proteasome Inhibitors for the Management and Treatment of Cancer, Adv Pharmacol
[8] S. Frankland-Searby, S.R. Bhaumik, The 26S proteasome complex: An attractive target for cancer therapy, Biochim Biophys Acta, 1825 (2012) 64-76.
[9] J. Adams, M. Behnke, S. Chen, A. A. Cruickshank, L.R. Dick, L. Grenier, J.M. Klunder, Y.T. Ma, L. Plamondon, R.L. Stein, Potent and selective inhibitors of the proteasome: dipeptidyl boronic acids, Bioorg Med Chem Lett, 8 (1998) 333-338.
[10] M. Groll, K.B. Kim, N. Kairies, R. Huber, C.M. Crews, Crystal structure of epoxomicin:20S proteasome reveals a molecular basis for selectivity of α',β'-epoxyketone proteasome inhibitors, J. Am. Chem. Soc., 122 (2000) 1237-1238.
[11] M. Groll, E.P. Balskus, E.N. Jacobsen, Structural analysis of spiro beta-lactone proteasome inhibitors, J. Am. Chem. Soc., 130 (2008) 14981-14983.
[12] S. M. Blaney, M. Bernstein, K. Neville, J. Ginsberg, B. Kitchen, T. Horton, S. L. Berg, M. Krailo, P. C. Adamson, Phase I Study of the Proteasome Inhibitor Bortezomib in Pediatric Patients With Refractory Solid Tumors: A Children's Oncology Group Study (ADVL0015), J Clin Oncol, 22 (2004) 4804-4809.
P. G. Richardson, T. Hideshima, K. C. Anderson, Bortezomib (PS-341): A Novel, First-in-Class Proteasome Inhibitor for the Treatment of Multiple Myeloma and Other Cancers, Cancer Control, 10 (2003) 361-369.
[14] A. Mazumder, New approaches to multiple myeloma, Community Oncology, 5 (2008).
[15] J. Abraham, Advances in multiple Myeloma treatment: lenalidomide and bortezomib, Community Oncology, 6 (2009) 53 - 58.
[16] C. S. Mitsiades, P. J. Hayden, K. C. Anderson, P. G. Richardson, From the bench to the bedside: emerging new treatments in multiple myeloma, Best Pract Res Cl Ha, 20 (4) (2007) 797-816.
[17] D. P. Schenkein, Preclinical Data with Bortezomib in Lung Cancer, Clin Lung Cancer, 7 (2) (2005) S49-S55.
[18] B. Holkova, S. Grant, Proteasome inhibitors in mantle cell lymphoma, Best Pract Res Cl Ha, In Press (2012).
[19] N. Awasthi, M.A. Schwarz, R.E. Schwarz, Combination Effects of Bortezomib with Gemcitabine and EMAP II in Experimental Pancreatic Cancer, Cancer Biol Ther 10 (1) (2010) 99-107.
[20] G. J. Kubicek, M. Werner-Wasik, M. Machtay, G. Mallon, T. Myers, M. Ramirez, D. Andrews, W.J. Curran Jr., A.P. Dicker, Phase I Trial Using Proteasome Inhibitor Bortezomib and Concurrent Temozolomide and Radiotherapy for Central Nervous System Malignancies, Int J of Radiat Oncol, 74 (2) (2009) 433-439.
[21] S.W. Hung, H.R. Mody, R. Govindarajan, Overcoming nucleoside analog chemoresistance of pancreatic cancer: A therapeutic challenge, Cancer Lett, 320 (2) (2012) 138-149.
[22] K. Venkatakrishnan, M. Rader, R.K. Ramanathan, S. Ramalingam, E. Chen, W. Riordan, W. Trepicchio, M. Cooper, M. Karol, L. von Moltke, R. Neuwirth, M. Egorin, G. Chatta, Effect of the CYP3A inhibitor ketoconazole on the pharmacokinetics and pharmacodynamics of bortezomib in patients with advanced solid tumors: A prospective, multicenter, open-label, randomized, two-way crossover drug-drug interaction study, Clin Ther, 31 (2) (2009) 2444-2458.
[23] A.M. Oliveira-Brett, A.M. Chiorcea Paquim, V.C. Diculescu, J.A.P.Piedade, Electrochemistry of nanoscale DNA surface films on carbon, Med Eng Phys, 28 (10) (2006) 963-970.
[24] V.C. Diculescu, M. Vivan, A.M. Oliveira-Brett, Voltammetric behavior of antileukemia drug glivec. Part III: In situ DNA oxidative damage by the glivec electrochemical metabolite, Electroanal, 18 (19-20) (2006) 1963-1970.
[25] C. M. A. Brett, A. M. Oliveira-Brett, Electrochemistry - Principles, Methods, and Applications, Oxford University Press, 1993.
[26] R.G. Compton, C.E. Banks, Understanding Voltammetry, 2nd edition, Imperial College Press, 2011.
[27] V.C. Diculescu, M. Vivan, A.M. Oliveira-Brett, Voltammetric behavior of antileukemia drug glivec. Part I - Electrochemical study of glivec, Electroanal, 18 (18) (2006) 1800-1807.
[28] A. Adenier, M.M. Chehimi, I. Gallardo, J. Pinson, N. Vila, Electrochemical Oxidation of Aliphatic Amines and Their Attachment to Carbon and Metal Surfaces, Langmuir, 20 (2004) 8243-8253.
[29] J.M.P.J. Garrido, C. Delerue-Matos, F. Borges, T.R.A. Macedo, A.M. Oliveira-Brett, Voltammetric Oxidation of Drugs of Abuse III. Heroin and Metabolites, Electroanal, 16 (18) (2004) 1497-1502.
[30] A.D.R. Pontinha, S.M.A. Jorge, V.C. Diculescu, M. Vivan, A.M. Oliveira-Brett, Antineoplasic Drug Methotrexate Redox Mechanism Using a Glassy Carbon Electrode, Electroanal, 24 (4) (2012) 917-923.
[31] V.C. Diculescu, A. Militaru, A. Shah, R. Qureshi, L. Tugulea, A.M. Oliveira-Brett, Redox mechanism of lumazine at a glassy carbon electrode, J Electroanal Chem, 647 (1) (2010) 1-7.
Copyright © 2025 - Toate drepturile rezervate