 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
Fluidele critice
Studii asupra procesului de dezvoltare
Factorii care au motivat folosirea de dizolvanti critici fluizi in dezvoltarea procesele de separare au fost: cresterea destul de rapida a pretului energiei in anii 1970; cercetarea sporita a dizolvantilor industriali de catre guvern; cresterea preocuparii populatiei referitoare la controlul poluarii si cererile de performanta tot mai crescute bazate pe materiale specializate.
Deficitul energetic timpuriu si de la sfarsitul anilor 1970 a fost in mare masura raspunzator de interesul crescut in extractia fluidelor critice in Statele Unite si a fost motivarea pentru un efort mare in cercetare si dezvoltare, initiat atat in industrie cat si in mediul academic. Un numar mare de cercetatori au cercetat extractia SCF pentru separarea substantelor organice din apa pentru a vedea daca ar putea inlocui metoda traditionala de distilare. In multe circumstante, este teoretic posibil ca separarea substantelor organice mixte prin procesarea cu ajutorul fluidelor critice ar cere mai putina energie decat cea care este ceruta de distilare sau de evaporare. Pentru aceste doua procese, reducerea consumului de energie pentru solventul reciclat si caldura de vaporizare pentru substantele organice ar trebui comparate.
Reducerea cheltuielilor cu energia a devenit o problema nationala in anii 1970. de exemplu, procesul de separare a membranei, cum ar fi ultrafilrarea si osmoza inversa au fost inaintate datorita considerentelor care tineau de consumul energetic. Concentrarea sau separarea unui val de fluid cere mai putina energie in tehnologia cu membrane pentru ca necesitatea reducerii energiei sa invinga fortele ozmozice este mai putin necesara decat energia necesara evaporarii pentru a separa un lichid de sarurile dizolvate in el. In mod similar, extragerea fluidelor critice poate fi mai putin intensiva decat evaporarea (capitolul 6) dar trebuie evaluata pe baza unui caz practic.
Pana la sfarsitul anilor 1970, statisticile au fost acumulate pe baza unor intamplari ale unor extrageri ale unor solventi, in special hidrocarburile clorhidrice. Cresterea folosirii unor solventi traditionali industriali este responsabila de inmultirea unei game variate de programe de cercetare&dezvoltare bazate pe procesele SCF. Cresterea preocuparilor consumatorului asupra potentialelor accidente chimice combinata cu nesiguranta prevederilor viitoare ale actiunilor guvernamentale au motivat o examinare a fluidelor critice, cum ar fi extragerea solventilor pentru mancaruri, bauturi si ingrediente.
In anii '70, opinia publica a devenit constienta de conceptul de "risipa zero". Provocarea risipei zero, desi nu foarte strict prevazuta in legislatie, a condus la cercetarea unor nenumarate procese de distrugere si curatare pentru tratarea materialelor lichide si solide reziduale. De asemenea, o atentie sporita a fost acordata imbunatatirii proceselor traditionale de control al poluarii, cum ar fi incinerarea si absorbtia. Tehnologia SCF si-a gasit adeptii printre cei preocupati de problema risipei si de cateva noi procese SCF pentru realizarea unei game variate de metode de curatare care au fost dezvoltate. Aceste procese SCF sunt descrise in urmatoarele paragrafe si in capitolele urmatoare.
In anii '70, producatorii au pus performanta unei cereri in crestere pe seama diferitelor materiale, cum ar fi chimicalele, polimerii si medicamentele. Ei au observat ca multe procese tehnologice care foloseau metode conventionale nu au putut satisface noile cerinte. Procesarea SCF a fost evaluata in incercarea de a oferi o solutie la aceste probleme. A fost testata pentru inlaturarea solventilor reziduali si monomeri de la polimerii cu structura moleculara complexa; pentru purificarea chimicalelor cu o rezistenta scazuta la temperaturi ridicate si monomeri, cum ar fi monomeri simpli si compusi; pentru despartirea diferitilor polimeri speciali si pentru multe alte scopuri.
In acest capitol o sa analizam un numar de studii de cercetare a procesului pentru demonstrarea principiilor ingineresti si stiintifice care trebuie aplicate atunci cand evaluam potentialele aplicatii ale tehnologiei SCF. Multi dintre cititori vor recunoaste instrumentele pe care le vom folosi in aceasta analiza; ele nu sunt noi, sunt specifice analizei. Aceste instrumente au fost folosite in evaluarea multor intreprinderi industriale la sfarsitul anilor '80 si in continuare. Multe dintre aceste, putine iluzorii aplicatii ale tehnologiei SCF ar fi putut fi evitate, sau cel putin ar trebui sa fie mai putin mediatizate, aplicatiile fiind evaluate folosind principii ingineresti mai vechi, care inainte de timp si bani au fost investite in aplicatii mai degraba nesanatoase.
Regenerarea carbonului activ
Precursoare a recentelor aplicatii ale tehnologiei SCF raportata in SUA este tehnologia SCF de regenerare a carbonului activ, prima data descrisa in anul 1978 in cadrul Conferintei Societatii Americane de Chimie (Modelul lui de Fillipi si Krukonis,1978). Fenomenele de operare din timpul absorbtiei substantelor organice din apele reziduale si cel de evaporare din carbonul activ folosind dioxidul de carbon sunt asemanatoare celor din alte procese de exatractie a fluidelor critice. De aceea, examinam detaliile tehnice aici.
Eventualele avantaje ale regenerarii SCF sunt consumul redus de energie si o pierdere redusa de carbon comparata cu procesul de regenerare termala, inca in aplicatie. Se sugereaza ca din cauza multor componente organice care pot fi dizolvate de solventii fluidelor critice, materialele organice de carbon activ din timpul purificarii apelor reziduale curgatoare pot fi evacuate de catre dioxidul de carbon supercritic in conditii mai putin riguroase decat nivelul de1000 grade Celsius al furnalelor de regenerare industriale.
Pentru procese de marime mai redusa care folosesc carbonul activ la o rata de cateva mii de livre pe zi, evaporatorii pot de asemenea servi si ca vase de absorbtie. Deci, regenerarea carbonului poate fi procesata cand stratul de carbon se foloseste, acesta fiind supraincarcat cu substantele organice absorbite. Procesele care folosesc mai mult carbonul activ si sistemele care necesita vase inalte de absorbtie, cum ar fi acelea de la tratamentul aplicat reziduurilor municipale, carbonul poate fi inlaturat de la absorbanti si transferat evacuatorilor pentru regenerare. Transferul carbonului activ folosit, de la absorbanti la furnalul termal de regenerare este inca o practica intens utilizata. Carbonul folosit este transferat de catre pompele mari, prin valve si inchideri activate de motoare. In paragrafele urmatoare, ne vom concentra pe procese care folosesc mari cantitati de carbon activ.
Figura 8.1. reprezinta o schema a unui sistem de regenerare a carbonului folosind CO2 supercritic. Initial, vasul de evacuare din figura 8.1 este plin cu carbon folosit. Din momentul in care tehnologia actuala a regenerarii carbonului activ foloseste pompe sa transfere carbonul folosit in cuptorul de regenerare, metoda este des folosita in schema sistemului de regenerare SCF. Dupa ce vasul de evacuare este umplut cu carbon activ, apa poate fi drenata in vas si vasul presurizat cu CO2 prin intermediul vaselor comunicante cand presiunea redusa din valve este pusa in miscare. Organismele absorbite sunt dizolvate de CO2, trecand prin stratul de CO2. Curentul de reziduuri organice de CO2 care paraseste vasul extinde la o presiune mai mica pentru a grabi substantele organice si pentru a le colecta in vasul separator care este prezentat in imagine. Solutia de CO2 care paraseste separatorul este recompensata si reciclata in vasul de evacuare si procesul continua pana cand carbonul activ a fost purificat de organismele absorbite.
La sfarsitul etapei de regenerare, fluxul de CO2 este oprit, vasul este deschis pentru a permite CO2 -ului sa se depresurizeze si carbonul activ este inlaturat de pompe. Vasul este apoi reumplut cu carbonul activ folosit, apa drenata si procesul de evaporare repetat. Apropo, CO2-ul ramas in vas la sfarsitul ciclului de regenerare se pierde in acest proces. Desi costul folosirii CO2 este destul de redus, cca. 5-10 centi/livra depinzand de volumul folosit, consumul lui ar trebui luat in considerare in evaluarea viabilitatii procesului, in special daca costul materialului care este extras este redus. CO2-ul care este pierdut reprezinta un dezavantaj economic pentru acest proces, dar o parte din acest tot poate fi recuperata odata cu instalarea unui nou rezervor suplimentar de CO2. Eficienta economica a oricarui proces, nu numai a procesului de extragere a fluidelor critice cere ca utilizarea echipamentului sa fie eficienta deoarece termenul limita este un dezavantaj al investitiei de capital. In prezent, cazul regenerarii carbonului active in functie de modul de dozare umpland si golind portiuni din proces care necesita cantitati specifice de timp care pot fi parti semnificative ale etapelor din intregul proces.
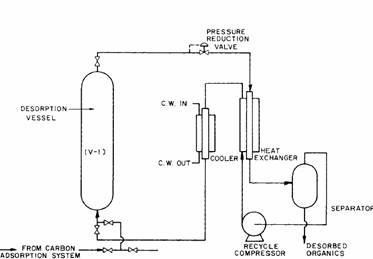
Figura 8.1 Schema unui aparat care se foloseste pentru regenerarea carbonului activ cu un solvent fluid critic
Sa consideram acum ca operatia procesului de regenerare foloseste un al doilea vas de evacuare, care va creste utilizarea aparatului. Vasul adaugat ofera capacitatea de minimizare sau de eliminare, de umplere sau de golire a tot ce a ramas. In operatiunea desfasurata prin cele doua vase prezentata in schema din figura 8.2, in timp ce procesul de regenerare se desfasoara in primul vas, al doilea este umplut cu carbonul active folosit si apa este drenata din vas. La sfarsitul procesului de regenerare (in vasul 1), miscarea CO2 -ului este stopata, vaselor le este permis sa comunice astfel incat jumatate din CO2 este transferat in cel de-al doilea vas. CO2-ul ramas in primul vas este raspandit in atmosfera si in aceasta operatiune in doua vase, o parte din CO2 este salvat. Regenerarea incepe cand CO2-ul trece in cel de al doilea vas; primul vas este golit si umplut in timp ce regenerarea carbonului activ din cel de al doilea vas are loc. Atunci o parte din CO2 este recuperata si aproape jumatate este eliminat prin adaugarea celui de al doilea vas la procesul initial.
Chiar daca procesul descris anterior este optim economic depinde desigur de multi alti factori. Daca sa recuperam CO2, cat sa recuperam, cat sa dureze perioada finala si alte aspecte similare, care sunt functii importante ale cantitatii de carbon activ care poate fi procesat, costul echipamentului si altele? Pentru cazul regenerarii carbonului activ, in recuperarea CO2 pot fi considerate probabil si cheltuielile de capital in plus ale celui de al doilea vas care ar putea fi justificate.
Studiul regenerarii carbonului activ (Filippi si altii, 1980) a fost legat de evaluarea regenerarii carbonului activ folosit in curatarea apelor reziduale care erau deversate de catre uzinele producatoare de pesticide. O gama variata de pesticide precum si diferitele tipuri de carbon activ au fost investigate.
O paleta diversa de temperaturi si presiuni a fost examinata pentru a determina caracteristicile solubile ale pesticidelor inainte de a procesa teste mai evoluate de absorbtie/evacuare. Rezultatele relevante ale testelor sunt descrise in detaliu intr-un raport al lui Arthur D. Little Inc. pentru Agentia de Protectia Mediului a SUA (Filippi si altii, 1980) si sunt prezentate mai amanuntit in paragrafele urmatoare.
Figura 8.3. prezinta structura moleculara a sase pesticide care au fost testate si nivelele lor de solubilitate cu CO2 critic intr-un set de conditii test, respectiv la 275 bari (4 atmosfere) si 100 de grade Celsius. De asemenea este inclusa in figura solubilitatea fenolului care a fost studiata deoarece acesta este o materie prima folosita in productia catorva persticide si atunci poate fi regasit in apele reziduale deversate de uzinele producatoare de pesticide. Solubilitatea acestor componente variaza pe o scara de la 1 la 100 ca si concentratie, dar regenerarea carbonului activ nu este necesar legata de nivelul de solubilitate. In mod specific, o solubilitate ridicata a CO2-ului critic nu asigura ca pesticidele absorbite vor fi inlaturate de catre carbonul activ.
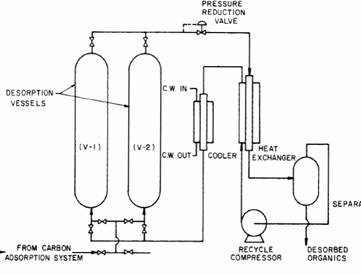
Figura 8.2 Schema variatiei aparatului prezentat in figura 8.1 folosit pentru regenerarea carbonului activ cu un solvent fluid critic
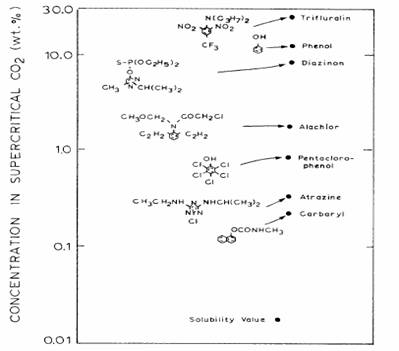
Figura 8.3 Structura moleculara si
solubilitatea dioxidului de carbon
critic asupra a sase pesticide la 100 grade Celsius si 275
Avand ca scop evaluarea eficientei folosirii CO2 -ului critic de a regenera carbonul activ folosit, o serie de experimente de absorbtie si evacuare au loc si capacitatea de recuperare a carbonului activ este masurata. O punte de carbon activ este expusa la un val de ape reziduale sintetice care contin un singur pesticide. Apele reziduale, in majoritatea cazurilor sunt sintetizate la un nivel al concentratiei avand in jur de 80% gradul de saturare.
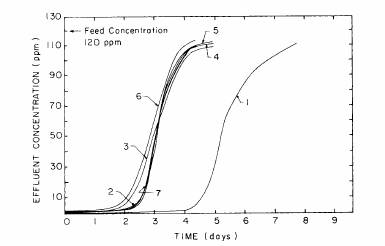
Figura 8.4. Pantele de absorbtie ale clorurilor si carbonului activ; numarul de curbe indica numarul de cicluri
Fluxul de apa de la coloana absorbtiei de carbon este
analizat in direct folosind un spectometru UV. Cu aceasta tehnica este
determinate o panta. Cand pesticidul din coloana cu fluide ajunge la saturatie,
fluxul de apa se opreste, apa iese afara din coloana si CO2 -ul
critic, in mod obisnuit la 275
Solutiile de cloruri sintetice au fost studiate in totalitate din momentul in care clorurile au oferit cel mai bun mod de regenerare. O serie de curbe de absorbtie a clorurilor sunt prezentate in figura 8.4. aria pana la curba de absorbtie este o masura a capacitatii carbonului activ pentru pesticide. Curba 1 reprezinta o schimbare de directie a absorbtiei masurata dupa ce carbonul activ este regenerat cu CO2 critic, s.a.m.d.
Prima capacitate a ciclului de carbon activ pentru cloruri este mai mare decat anterioarele capacitati ale ciclului, dar curbele de la 2 la 7 sunt aproape suprapuse, ceea ce ne indica o capacitate de absorbtie statica care este realizata prin regenerarea CO2 supercritic. In mod accidental, motivele pentru care descresterea in capacitate dupa primul ciclu nu sunt discutate in detaliu aici, dar probabil ca sunt aceleasi raportate de muncitorii care au examinat regenerarea carbonului activ al solventilor lichizi organici.
Este arhicunoscut faptul caci caldura de absorbtie a componentelor variaza odata cu incarcarea acelei componente cu carbon activ. La incarcari mai mici, caldura de absorbtie este foarte ridicata (apropiindu-se de legaturile chimice) in timp ce la incarcarile mari caldura de absorbtie descreste in intensitate. Caldura de reactie este asemanata cu fortele de atractie dintre atomii de carbon activi si componenta organica. Cele mai active pozitii sunt folosite primele si pe masura ce devin mai puternice, starile de absorbtie descresc la nivele care sunt tipice legaturilor fizice de absorbtie. Atunci, am putea concluziona ca anumite parti de carbon sunt mai usor de regenerat decat altele. Abilitatea de a obtine o constanta, dar scazuta capacitate de absorbtie reprezentata prin curbele de la 2 la 7 este probabil o manifestare a unor forte relative reprezentand abilitatea CO2-ului critic de a descompune moleculele mai putin atrase. Primul ciclu de regenerare probabil descompune numai moleculele sustinute de o slaba absorbtie fizica. Atunci, exista o scadere a capacitatii masei de carbon si probabil urmatoarele stadii de absorbtie si regenerare opereaza numai in locul pozitiilor cu energie redusa.
Clorura este unul din pesticidele care este usor de descompus de catre carbonul activ. Unele din alte pesticide nu sunt descompuse de tratamentul cu CO2 critic. Componentele diazina, pentaclorofenol si carbitii prezinta legaturi de atractie foarte puternice care dau in schimb carbonul activ neregenerabil. Deci, capacitatea de atractie a carbonului scade la zero dupa doua-trei cicluri. Desi interactiunile specifice dintre carbonul activ si pesticide care conduc la declinul capacitatii carbonului nu sunt raportate, diferentele nivelului de solvabilitate al pesticidelor bogate in CO2 nu sunt singura explicatie. Figura 8.3 arata ca solubilitatea diazinei este de cinci ori mai mare decat a clorurii, totusi carbonul folosit in cadrul diazinei nu poate fi regenerat. Figura 8.5 prezinta de exemplu trei curbe de atractie cu diazina si cu o comparatie a ariei dintre curbe care arata caci capacitatea carbonului activ a scazut la 10% dupa doua trei cicluri de absorbtie/evacuare. Desi functia primara a acestui studiu a fost folosita la un numar de pesticide si nu pentru a investiga fenomenul de sorbtie este probabil correct sa asemanam incapacitatea CO2 -ului critic de a inlatura aceste componente din carbonul activ cu fortele de sorbtie sau probabil sa aiba loc la suprafata reactii chimice.
Cateva teste de desorbtie vor fi descrise in continuare in detaliu deoarece acestea sunt relevante in studiile asupra extractiei SCF la lichide sau solide inca utilizata la alte laboratoare industriale sau academice. Rezultatele testelor de desorbtie explica anumite fenomene care sunt raportate in alte studii de proces si rezultate reliefeaza anumite limite ale acestor procese. Figura 8.6 reprezinta profilul tipic al desorptiei; in cazul in care concentratia de cloruri, din CO2 -ul care paraseste coloana de carbon activ este ilustrata. Scara de concentratie reprezinta media concentratiei de cloruri din CO2 si lungimea segmentului marcheaza volumul de CO2 care trece prin strat intr-un interval dat a carui concentratie este masurata gravimetric. Reamintind ca solubilitatea clorurii in aceste conditii este de 10 % prezentata in Figura 8.3, dar concentratia din fig. 8.6 este mult mai scazuta. Limitarile transferului in masa, fie de la suprafata carbonului la diferite constante de viteza a reactiei liniare, fie particule de carbon, s.a.m.d. Rezultatele unor asemenea studii sunt prezentate in Figura 8.7. Curbele de regenerare de la aceste teste se suprapun indicand faptul ca regenerarea SCF este independenta de parametrii testate. Concluziile acestor teste sunt ca simplele limitari ale transferului masic nu sunt factori de control in procesul de regenerare a SCF.
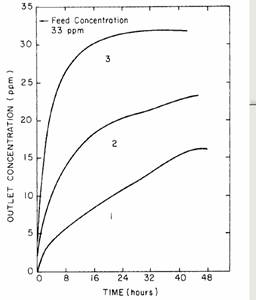
Figura 8.5 Curbele de absorbtie ale diazinei asupra carbonului activ; numarul de curbe indica numarul de cicluri
O alta explicatie pentru forma curbelor de regenerare este aceea de existenta unui echilibru de absorbtie in CO2-ul critic-clorura-sistemul de carbon activ asemanatoare cu echilibrul de absorbtie masurat in sistemul apa-organic-carbon activ. S-a dovedit ca asemanarea cu izoterma de absorbtie in sistemele cu apa reprezinta mecanismul de control pentru procesele de desorptie. Echilibrul de absorbtie pentru cele mai comune sisteme apa-organic-carbon active sunt redate de obicei prin izoterma lui Langmuir si/sau Freundlich, care coreleaza incarcarea organica in carbonul activ cu concentratia organica in faza acvatica. Forma si panta acestor izoterme sunt redate de legatura absorbtiei organicului de catre carbon. Cand izotermele sunt potrivite dupa un model al lui Langmuir si Freundlich, parametrii modelului pot fi determinati. Aceleasi model ear trebui aplicate si pentru CO2 si din valorile parametrilor potriviti, datele din figura 8.7 pot fi explicate.
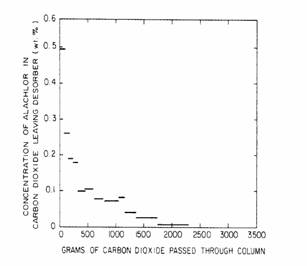 Figura 8.6
Profilul de desorptie al clorurii asupra carbonului activ folosind dioxidul de
carbon critic
Figura 8.6
Profilul de desorptie al clorurii asupra carbonului activ folosind dioxidul de
carbon critic
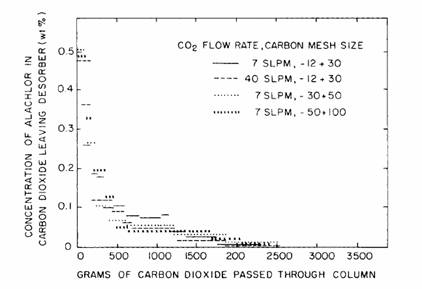
Figura 8.7 Comparatie a efectelor limitarii transferului de masa in desorptia clorurii de carbonul activ folosind dioxidul de carbon critic; teste cu cateva rate fluctuante si cateva site de carbon SLPM= Litrii standard pe minut
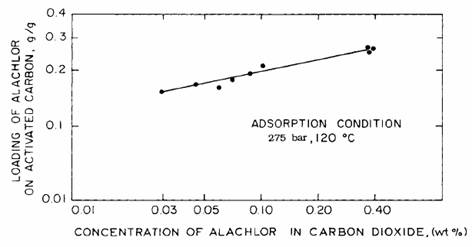
Figura 8.8 Datele pentru sistemul format din dioxidul de carbon critic-clorura-carbon activ potrivit de izoterma Freundlich
Echilibrul dintre pesticidele din faza CO2 ului critic si pesticidele din faza solida a fost masurat. Datele pentru CO2 critic-clorura-carbon activ sunt corelata sub forma izotermei Freundlich prezentata in figura 8.8 (Krukonis, 1977). Suprinzator, chiar si la nivele scazute ale concentratiei clorurii, doua puncte sub nivelul de solubilitate prezentat in figura 8.3, echilibrul de incarcare cu carbon activ este mai mare de 0,2 g/g. Marimea acestor puncte conduce la ipoteza ca limitarile echilibrului de absorbtie nu sunt responsabile de forma curbei de desorptie si ca solubilitatea in CO2-ul critic nu reprezinta pasul limitativ al procesului de regenerare.
Modelul si formele pentru cazul regenerarii guvernat de efectele echilibrului sunt dezbatute in numeroase texte. Tezele lui Sherwood, Pigford si Wilke (1975) vorbesc despre asta. Bilantul material dintre concentratia materialului dizolvat in CO2 si concentratia in carbonul activ solid in timpul desorptiei este data de relatia:
![]() (8.1)
(8.1)
Unde ε este volumul masei, c concentratia speciei in dioxidul de carbon, p densitatea carbonului activ (aproximativ 0,8), q reprezinta concentratia speciei in dioxidul de carbon activ, v reprezinta velocitatea liniara a dioxidului de carbon care trece prin strat. Daca relatia dintre c si q este mai mult cunoscuta analitic, de exemplu ca si izoterma lui Langmuir q=f(c) sau reprezentata precum in figura 8.3, ecuatia poate fi rezolvata pentru a furniza diferite tipuri de concentratie de CO2 si masa ca o functie de timp. Aceasta relatie este cunoscuta ca si modelul teoriei echilibrului.
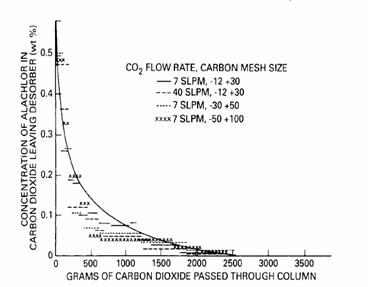
Figura 8.9 Comparatia dintre datele desorptiei calculate si cele experimentale
Cu datele din figura 8.8 si ipoteza echilibrului local putem calcula ca si functie de timp concentratia functiei clorura in CO2 -ul rezidual si profilul concentratiei de clorura din masa carbonului activ. Figura 8.9 arata profilul calculat suprapus peste masurile curbelor de regenerare redate in figura 8.7. Corelatia dintre profilele masurate si cele calculate este destul de buna atat ca forma cat si ca magnitudine; aceasta sustine cu tarie ca teoria echilibrului local explica corect profilul desorptiei masurate (Modell si altii, 1979).
Existenta echilibrului de absorbtie in sistemul format din CO2 - clorura - carbon activ este o limita fundamentala a procesului de regenerare a dioxidului de carbon supercritic. De exemplu, una dintre ramurile echilibrului local este cerinta ca una sau doua pozitii de CO2 sa treaca prin strat pentru a regenera carbon activ decat este previzionat de catre solubilitatea data de combinatia de CO2-clorura. Rezultatele cercetarilor trec peste tema regenerarii carbonului activ si au implicatii dupa cum se pare in extractiile aleatoare ale SCF. Astfel, decofeinizarea SCF a cafelei este un exemplu despre un alt sistem care prezinta un echilibru izotermic remarcabil de apropiat cu izoterma SCF a clorurii prezentata in figura 8.8. De aceea, intelegerea procesului de regenerare a SCF-carbon activ ofera o baza pentru interpretarea altor procese SCF. Vom discuta despre decofeinizarea cafelei in capitolul 10.
Separarea solutiilor organice-apa
Etanol-apa
Consumul redus de energie din anii 1970 a fost un impuls de evaluare a folosirii lichidelor critice pentru separarea organismelor de apa. Un proces care a primit substantiale fonduri guvernamentale si industriale este acela de separare cu ajutorul CO2-ului critic a etanolului de apa (Paulaitis, Gilbert si Nash, 1981; Moses, Goklen si de Filippi, 1982; Jonas, 1981, Kuk si Montagna,1983). Un scop primar al acestor studii este de a desparti azeotropul etanol-apa de 95,5% etanol. Dar daca azeotropul nu poate fi separat, un alt scop este acela de a demonstra un proces de o intensitate mai mica folosind extractia fluidelor critice in concordanta cu distilarea azeotropica. Scopul a fost ca ar putea fi posibil sa se combine extractia fluidelor critice cu distilarea pentru a se reduce costurile procesului de o maniera care combina osmoza si evaporarea, de exemplu.
Procesul de separare a etanolului de apa folosind CO2-ul critic este un concept chimic care este visul oricarui inginer. Nu este necesar a se alimenta solide prin pompe si corespondenta valvelor solenoidale operatia contracurent este in prezent modul normal de operare. O diagrama simplificata a procesului continuu si contracurent a separarii etanolului de apa este prezentata in figura 8.10. Alimentarea amestecului etanol-apa cu amestecul de CO2 supercritic din vas poate fi pompat continuu intr-o coloana. Amestecul transmis catre un separator si substanta rafinata poate fi descarcata din coloana printr-o valva prezentata in figura. Interioarele extractorului pot avea anumite urme sau pot fi impachetate aranjat. Alimentarea se scurge prin coloana din vas in vas impotriva fluxului ascedent de CO2. Exista o limita maxima a presiunii de operare daca procesul are loc cum a fost descris inca din momentul in care la presiuni ridicate densitatea CO2-ului imbogatit se poate apropia sau depasi faza apei-imbogatite. Aceasta conduce intr-o faza de neseparare si o incapacitate de operare a coloanei, desi daca CO2-ul ar fi in faza avansata ar putea fi introdus prin varful coloanei.
In timpul contactului din vas in vas al CO2-ului critic-imbogatit cu solutia de etanol-apa, etanolul este de preferinta extras. Extragerea consta mai mult in CO2, un pic de etanol si apa; pleaca de la varful coloanei. Figura 8.10 arata solutia CO2 imbogatit care este raspandita de presiune prin valva. Aceasta reduce puterea de solvent a CO2-ului si conduce etanolul pentru a se precipita in separator. CO2-ul este apoi recompresat si reciclat prin extractor. Sa consideram ecuatiile care descriu echilibrul de extractie al unui material dintr-o faza in alta. In practica, echilibrul concentratiilor in sistemul in doua faze sunt descrise in termen de coeficient de distributie (uneori numit coeficient de partitie) care descrie echilibrul concentratiilor unei specii in fiecare din cele doua faze. Formulele fizice-chimice, de obicei definesc coeficientul de distributie pentru un sistem ternar in termeni de procent al unei particule; de exemplu, coeficientul de distributie al etanolului in sistemul CO2 -etanol-apa este dat de:
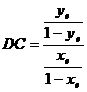
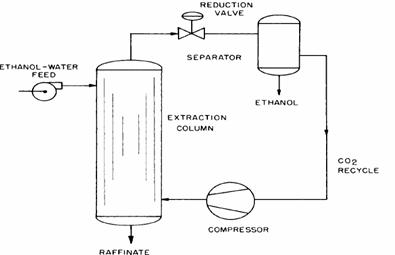
Figura 8.10 Schema unui proces de extractie a etanolului din apa cu ajutorul unui solvent lichid critic
Toate
valorile DC din acest capitol sunt reprezentate in unitati de greutate. Pentru
o concentratie a etanolului mai mica de 10% in oricare din faze, relatia
coeficientului de distributie se simplifica la ![]() (8.3)
(8.3)
Ecuatia simplificata este in general avansata de catre grupurile care studiaza separarea etanol-apa si pe care le vom folosi in discutiile ulterioare.
Un numar de grupuri de cercetare-dezvolatre au publicat date despre sistemul CO2-etanol-apa cu diverse concentratii de etanol, temperature si presiuni diferite (Paulaitis, Gilbert si Nash, 1981; Moses, Golken si de Filippi, 1982; Kuk si Montagna, 1983). Datele din figura 8.11 arata ca conditiile de extractie, daca CO2-ul este un lichid aproape critic sau un fluid critic cu o presiune ridicata nu influenteaza semnificativ extractia, in acest fel, coeficientul de distributie nu este afectat intr-un mod semnificativ. O linie dreapta potriveste datele in figura 8.11 cu o aproximatie de ±30%. Coeficientul de distributie este panta liniei; aproximativ 0,09 (avand greutatea ca baza). Selectarea CO2-ului pentru etanol dintr-un amestec etanol-apa este destul de ridicata. La o concentratie a etanolului in apa de 10%, concentratia etanolului in faza de CO2 imbogatit este de 0,9%. Alte masuratori arata caci concentratia apei care il insoteste este de 0,1% la 25 grade Celsius. De la aceste valori, selectivitatea este calculate ca fiind 81.
In cazul unui coeficient de distributie constant, Treybal (1968) arata ca rata teoretica minima a solventului necesar pentru a extrage toate componentele din amestec este egala cu inversul coeficientului de distributie. Sa ne amintim, totusi ca valoarea teoretica minima a ratei solventului cere coloane infinit de inalte. In practica actuala, o rata mai mare a solventului, in jur de cel putin 1,3-1,5 ori minimum se cere. In continuare vom prezenta cateva proceduri grafice elementare, dar informative pentru a ilustra relatia dintre coeficientul de distributie si operatia procesului de extractie a fluidului critic pentru a separa etanolul de apa.
Sa presupunem caci concentratia etanolului este de 10%, un fenomen produs de procesele de fermentatie. Pentru simplificare sa presupunem mai departe ca CO2-ul reciclat nu contine etanol si ca procentul de alcool recuperat este de 95% din cel din amestec. Figura 8.12 reproduce linia de echilibru prezentata anterior in figura 8.11. In acest caz, rata minima a solventului din amestec este prezentata in figura 8.12 de asa-zisa linie operationala, linia in zig-zag dintre abscisa la 0,55 etanol in apa (specificam ca gradul de recuperare al etanolului din amestec este de 95%) si linia de echilibru la 10% etanol (concentratia amestecului). Rata minima a solventului din amestec in acest caz este de 10,5. Rata solventului din amestec este echivalentul a 105lb CO2/lb etanol din amestec; aceasta este mai degraba o cerinta fundamentala a solventului. Inca de cand linia operationala atinge linia de echilibru, o coloana infinit de inalta este ceruta.
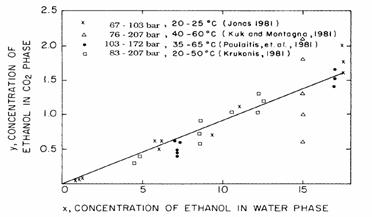
Figura 8.11 Rezultatele experimentelor asupra catorva studii ale sistemului etanol-apa- dioxid de carbon
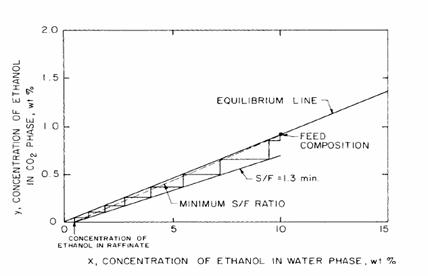
Figura 8.12 Linia de echilibru si cea operationala pentru sistemul format din etanol-apa-dioxid de carbon; in acest caz nu exista etanol in dioxidul de carbon reciclat
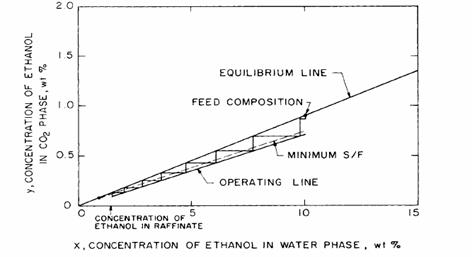
Figura 8.13 Linia de echilibru si cea operationala pentru sistemul format din etanol-apa-dioxid de carbon; in acest caz exista 0,1% etanol in dioxidul de carbon reciclat
Vom folosi o linie operationala cu o rata a solventului de 1,3 ori mai mica decat cea minima (vezi figura 8.12).
O solutie matematica a numarului etapelor de extractie cerute pentru a recupera 95% din etanol prin CO2-ul critic, solutie care este obtinuta printr-o procedura grafica numita gradarea talerelor. Un pic mai mult de sapte talere de echilibru (7.3) sunt necesare pentru aceasta separare folosind constructia grafica din figura 8.2. In locul liniei operationale determinate, a numarului de etape de echilibru din figura 8.12, presupunem ca intrarea de CO2 (reciclat) nu contine etanol; in realitate intrarea de CO2 va contine ceva etanol. Uneori prezenta unei cantitati mici de produs reciclat are un impact major asupra operatiei, costurilor si eficientei procesului. Daca coeficientul de distributie este foarte scazut, cum ar fi pentru separarea etanolului de apa, prezenta produsului reciclat creste dificultatea de obtinere a unei mari recuperari de etanol.
Pentru separarea etanolului de apa, cerinta de inlaturare completa a etanolului din CO2 -ul reciclat reprezinta o provocare tehnica care creste complexitatea si costurile proceselor relative conform diagramei simplificate din figura 8.10. Motivele pentru cresterea complexitatii sunt prezentate in continuare. Figura 8.13 prezinta procesul de extractie a etanolului in momentul in care CO2-ul reciclat are o concentratie a etanolului de 0,1%. La sectorul de rafinare al extractorului, concentratia de etanol in faza apei imbogatite este acum dictata de consideratii de echilibru si de valoarea coeficientului de distributie. Limitarea atribuita echilibrului este indicata de linia operationala din figura 8.13, care are o inclinatie inversa de 13,7 (aceeasi inclinatie ca si linia operationala descarcata din figura 8.12) si intersecteaza dreapata echilibrului in coordonatele x=1,1 y=0,1. Simpla constructie din figura 8.13 arata ca prezenta unei mici cantitati de etanol in amestecul de CO2 reciclat duce la o limita superioara a cantitatii de etanol in locul de rafinare nu poate fi scazuta la mai putin de 1,1%, pentru 0,1% etanol din amestecul reciclat, recuperarea maxima de etanol din amestec, chiar si cu o coloana infinit mai mare este de numai 89%.
Sunt anumite lucruri de luat in considerare pentru a optimiza costurile de recuperare. Cand desenam un proces, inginerul trebuie sa faca anumite concesii asupra procentului de etanol recuperat versus capitalul si costurile operationale ale procesului propus. O linie operationala reala este desenata in figura 8.13 (pentru acest exemplu linia operationala minima este potrivita in asa fel incat numarul de echilibru este din nou 7,3). Amestecul rafinat in acest caz paraseste coloana cu 1,4% etanol, ajungand la o recuperare totala de etanol de 86%. Un desen optim economic depinde de mai multi factori, cum ar fi costul de obtinere a etanolului prin fermentare, legislatia din domeniul controlului local al poluarii care ar putea stabili limite ale etanolului descarcat; si costul tehnologiilor concurente de separare. Vom folosi procesele descrise in figura 8.13 pentru a explica operatia de extractie din coloana care trebuie sa fie investigata cand se ia in considerare daca tehnologia SCF ofera o optiune viabila fata de alte tehnologii.
Nu am descries inca reciclarea totala si recuperarea produsului, dar am presupus caci concentratia de etanol din vas este de 0,1%. Cum s-a ajuns aici? Anumiti cercetatori care prezinta date despre faza de echilibru a sistemului CO2-apa-etanol sugereaza ca reducerea presiunii, cresterea temperaturii sau ambele pot conduce in precipitat la etanol din faza CO2 -ului critic si ca odata cu recompresia CO2-ul poate fi reciclat. Aceste afirmatii sunt incorecte deoarece sunt bazate pe o extrapolare a datelor din cele doua faze: lichida -vapori ale diagramei fara a lua in considerare tipul de comportament al fazei care exista pentru un amestec pseudobinar constand in CO2 si etanol (cu o cantitate mica de apa).
Din figura 8.11 la un nivel al
concentratiei de etanol de 15%, solubilitatea etanolului in CO2 la
75,8
Atunci cand etanolul poate fi separat de CO2 daca reducerea presiunii nu poate realiza sarcina? Exista o intrebare mai generala. Cand un vas din amestec poate fi curatat in cazul extractiei la anumite concentratii scazute ale amestecului sau de la sisteme cu un coeficient scazut de distributie? In principal, reducerea presiunii ar functiona, dar o asemenea schema probabil ar fi scumpa datorita costurilor compresiei de gaze. O schema alternativa de recuperare a etanolului extras si curatarea amestecului din vas este descrisa in U.S. Patent 4,349,415 (de Filippi si Vivian, 1982). In aceasta metoda, o coloana de distilare de presiune ridicata este folosita pentru a distila CO2-ul din amestecul CO2 condensat -etanol. O diagrama schematica a unei extractii totale si procesul de eliminare a CO2 este prezentat in figura 8.14.
Etanolul este extras la 20 grade Celsius si 55,2 bari (800 atm.) cu CO2 lichid si amestecul extras care paraseste partea de sus a extractorului este impinsa incet catre 48,3 bari (700 atm.) pentru a forma o faza lichid si una vapor. Amestecul din doua faze este introdus pentru o scurta distilare in turnul in care vaporii de CO2 initial din etanol sunt separati de faza CO2-etanol. Vaporii de CO2 care parasesc turnul sunt compresati la aproape 62,1 bari (900 atm.). Amestecul de CO2 se incalzeste usor datorita compresiei care a fost facuta de vaporii adaugati de recompresor. Este descarcat din compresor prin partea tubului de schimbare a caldurii boilerului de distilare.
Transferul caldurii sensibile si latente se petrece de la CO2-ul condensat din tuburile de fierbere la solutia fiarta de CO2-etanol. Lichidul CO2 racit este apoi pompat la varful extractorului pentru a completa ciclul si a continua procesul de extractie.
Coeficientii scazuti de distributie, cerinta de reciclare a CO2-ului cu continut foarte scazut de etanol pentru a realiza o foarte buna recuperare a etanolului din amestec si incapacitatea de a realiza separarea etanolului din amestecul extras prin presiunea scazuta a necesitat dezvoltarea procesului SCF extragere-distilare. Diagrama prezentata in figura 8.14 rezuma faptul ca o tehnica veche de distilare poate fi combinata cu noua extractie critica de CO2 pentru a rezolva problema separarii; CO2-ul critic poate extrage etanolul din amestec, distilarea poate separa si regenera solventul pentru vas si compresia vaporilor poate duce la o eficienta a energiei.
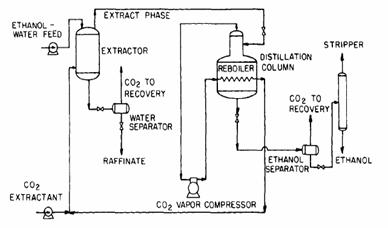
Figura 8.14 Schema unui proces folosind dioxidul de carbon critic pntru extragerea etanolului din apa combinata cu distilarea pentru curatarea dioxidului de carbon
Alte sisteme alcool-apa
Faza despartirea tehnicilor descrisa pentru prima data de Elgin si Weinstock (1959) pentru recuperarea metil etil ketonei din apa folosind etilena critica poate fi de asemenea folosita pentru a separa amestecul de alcool-apa. Sa consideram recuperarea n-propanolului din apa folosind CO2 -ul critic (Kuk si Montagna, 1983). CO2-ul critic poate fi folosit in doua moduri: pentru a desparti amestecurile de n-propanol de apa in proportie de 25% la 75% n-propanol. Recuperarea n-propanolului din apa poate fi realizata fie prin operarea in regiunea in doua faze lichid-lichid (LL) sau in regiunea in trei faze lichid-lichid vapor a diagramei amestecului n-propanol-apa-CO2 prezentata in figura 8.15. Daca se presupune ca procesul are loc in regiunea LLV a diagramei atunci nu exista grade de libertate pentru acest sistem (vezi tabelul 3.1) pentru ca temperatura este fixate la 40 grade Celsius si presiunea este fixata la 104 bari (1,500 atm.).
De aceea, compozitia celor trei faze de echilibru este definita de colturile regiunii triunghiulare LLV cu faza diagramei. Desi sume relative ale celor trei faze de echilibru vor depinde de compozitia amestecului din aceasta regiune, componentele celor trei faze mereu raman fixate la aproximativ 18% n-propanol-72%, apa-10%, CO2 si 12% n-propanol-1%, apa -87% CO2. Atunci, intr-o singura faza a extractorului n-propanol poate fi recuperat prin inlaturarea fie a CO2-ului imbogatit care are o rata de n-propanol in apa de la 12 la 1 sau prin inlaturarea fazei mijlocii a n-propanolului imbogatit care are o rata de n-propanol in apa de 2,25 la 1. Costurile acestui proces vor dicta daca este mai economic sa recuperezi n-propanol din faza de mijloc lichida care are un grad mare de n-propanol dar o scazuta selectivitate a n-propanolului in apa sau CO2-ul din faza imbogatita care are mai putin alcool, dar o rata mai mare de alcool in apa.
Sistemul n-propanol-apa-CO2 este un alt exemplu de sistem care descrie echilibrul LLV in conditii apropiate de temperature critica si presiunea CO2. Acest tip de comportament al fazei este descris in detaliu in capitolul 3. Multe alte sisteme solvent organic-apa- SCF pot fi gasite in lucrarile lui Elgin si ale altor coautori.
Extractia alcoolului din apa folosind fluidele critice a fost descrisa de asemenea in detaliu de Paulaitis si alti coautori (Kaunder si Paulaitis, 1984, Diandreth si Paulaitis, 1984; Paulaitis, Kander si Diandreth, 1984, Paulaitis, Gilbert si Nash, 1981). Acesti cercetatori arata ca atunci cand procesul de separare opereaza in apropierea punctului critic al amestecului (de exemplu punctual de maxim pentru un sistem), schimbari majore in selectivitatea alcoolului si in faza de incarcare cu fluid critic se poate petrece pentru schimbari de temperaturi sau presiuni relative mici. Asemenea schimbari sunt aparente in cele doua seturi de diagrame izopropanol-apa- CO2 prezentate in figurile 8.16 si 8.17. S-a sugerat in lucrarile citate ca cei doi factori de control ai selectivitatii si incarcarea amestecurilor de alcool si apa sunt compresorii solventului SCF si diferentele neideale din faza lichida descrise de amestecurile de alcool binar-SCF si alcool-apa (de exemplu gradul de hidrogen activ din aceste solutii). Acesti doi factori, compresia SCF si amestecurile neideale determina daca amestecul alcool-apa-SCF se va desparti intr-un amestec LLV. Avantajul total ar trebui considerat in procesele de separare alcool-apa-SCF ale diferitelor faze comportamentale care au loc pentru diferite sisteme si care afecteaza selectivitatea si incarcarea solventului SCF.
Apa-acid acetic
Posibilitatea de a obtine un process cu o energie redusa de asemenea a necesitat un effort substantial de a examina extractia fluidelor critice de a separa acidul acetic de apa. Lucrarea se imparte in doua categorii: separarea fermentatiei acidului acetic si separarea acidului acetic de apa din aceasta solutie, acestea formandu-se in timpul productiei celulozei acetate.
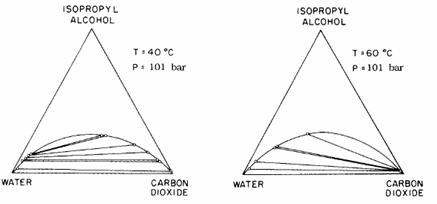
Figura 8.16. Efectul temperaturii asupra selectivitatii si incarcarii izpropanolului in dioxidul de carbon critic
Recuperarea acidului acetic din fermentatie este asemenetor recuperarii etanolului din procesul de fermentatie. In procesul de productie a celulozei acetate, celuloza reactioneaza cu acid acetic inghetat si anhidrida acetica pentru a forma triacetatul celulozic. Apa este apoi adaugata peste solutia formata din triacetatul de celuloza-acidul acetic inghetat care rezulta din inlaturarea unei parti de acetate din celuloza. Apa deasemenea duce la formarea precipitatului de acetat de celuloza si de asemenea dilueaza acidul acetic. Acetatul de celuloza este filtrat, solutia acid acetic-apa este separata prin distilare si acidul acetic inghetat este reciclat in reactorul de cetat de celuloza. Etapa de distilare consuma multa energie si atunci tehnologiile alternative sunt evaluate in continuare pentru separarea celor doua componente.
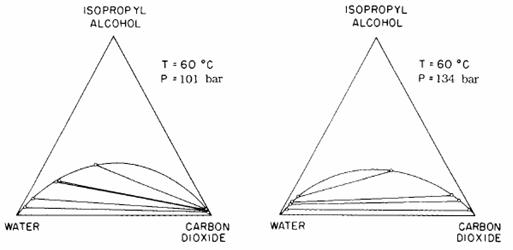
Figura 8.17 Efectul presiunii asupra selectivitatii si incarcarii izopropanolului in dioxidul de carbon critic (Paulaitis, Kander, Diandreth, 1984)
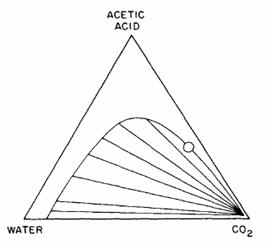
Figura 8.18 Diagrama ternara pentru sistemul format din acid acetic-apa dioxid de carbon la 25 grade Celsius si 64 bari (933 atm.) (Francis, 1954)
Acidul acetic este destul de dificil in a fi extras cu CO2; acest fapt a fost cunoscut inca de acum 30 de ani cand Francis a studiat sistemul CO2-apa-acid acetic (Francis, 1954). O diagrama de echilibru a acestui sistem este prezentat in figura 8.18 si datele de pe linia curbata din diagrama sunt reconfigurate sub forma axelor xy din figura 8.19. Figura 8.19 prezinta ca datele de echilibru nu prezinta o linie dreapta, cum era in cazul sistemului etanol, indicand ca coeficientul de distributie nu e constant. Dar acest lucru in sinea lui nu e important. Ce e important este fluctuatia curbei de echilibru a acidului acetic diluat, punctual de tangenta in aceasta zona determinand rata de dizolvare a solventului. La o fluctuatie a acidului acetic de 0% pana la 15%, coeficientul de edistibutie este in jur de 0,03 (marimea de baza ), vezi in figura 8.19. Atunci rata minima de CO2 necesara pentru a extrage tot acidul acetic este 33 lb CO2 la 1 lb solutie. Pentru comparatie, aceasta valoare este de 3 ori mai mare decat cantitatea de CO2 necesara pentru a extrage etanolul din amestecul etanol-apa. In cazul real, rata solventului de 1,3 ori mai mica este aproximativ 40 lb CO2 la 1 litru solutie, rata considerate a fi destul de ridicata.
Cum coeficientul de distributie scazut nu prezinta destule obstacole, Extractia acidului acetic din procesul de fermentatie este si mai neatractiv datorita PH-ului ridicat al solutiei. Pentru ca procesele sa fie evaluate, acidul acetic va fi produs intr-o solutie cu un PH in jur de 6,0. PH-ul acidului acetic este de 4,8 si atunci la un PH de 6,0, virtual tot acidul acetic produs in solutie exista ca un ion de acetat. Schema recuperarii/extragerii actuale foloseste acidificarea (cu HCl, de exemplu) pentru a converti ionul de acetat in acid acetic liber. Apoi acidul liber poate fi extras cu un solvent organic. Daca CO2-ul este folosit ca un extractant, acidul clorhidric nu este necesar. Acidul carbonic din echilibrul CO2-apa va neutraliza partial, nu total, ionul acetate; aceasta poate fi determinata dintr-o balanta materiala a substantelor din solutie.
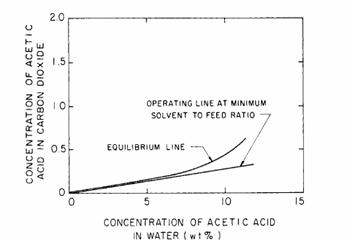
Figura 8.19 Locul de echilibru si liniile operationale pentru sistemul acid acetic-apa-dioxid de carbon la 25 grade Celsius si 57 bari
Un patent care acopera conceptual de extractie al acidului organic din solutiile cu un PH ridicat ofera date din care acest concept poate fi analizat (Shimshick, 1981). Exemplul 6 din patent este reprodus.
Dioxidul de carbon la 2400±200 atm. si 50 grade±2 grade Celsius a fost folosit pentru a extrage acidul acetic din procesul de fermenttie a clostridium thermoaceticum care contine cca. 0,23 M acetat de sodium si 0,03 M acid acetic, PH 5,7. Aproximativ 1% din acidul acetic/acetatul de sodium din procesul de fermentatie a fost recuperate sub forma de acid acetic.
Din datele si din experimental descris in patent
coeficientul de distributie bazat pe un acetat total este calculat ca fiind
0,004. Acesta este un numar foarte mic, care, deasemenea, este o consecinta a
cantitatii mici de acid liber disponibil in solutia cu un
PH ridicat. Alti autori(Yates, 1981; Busche, Shimshick si Yates, 1982) vorbesc
despre problema extractiei incomplete de acid organic din solutia cu un PH
ridicat folosind CO2. Autorii sugereaza ca substanta rafinata din
extractor poate fi reciclata pana la fermentator.
In ultimii ani, mule alte separari ale apei de substantele organice au fost reprezentate prin testele de fezabilitate. Unele au beneficiat de cercetari intense si eforturi de dezvoltare deoarece ele necesita un consum mare de energie pentru separarea prin distilare. O lista partiala cu substantele organice include dioxina, acetone, formaldehidele, N, N-dimetil formaldehide si glicolul de etilena. Multe din aceste componente se dizolva in hidrogenul din apa, ceea ce face mult mai usoara extractia cu CO2.
Formaldehidele si glicolul de etilena sunt doua componente care contin hidrogen. De aceea, ca si apa, este destul de dificil sa extragem aceste componente din apa cu CO2. De exemplu, formaldehidele au un coeficient de distributie scazut de numai 0,001. Un coeficient de distributie asa de scazut sugereaza ca este imposibil sa extragem formaldehide din apa. Ca particularitate, selectivitatea CO2-ului pentru formaldehide este mai mica decat 1,00 ceea ce inseamna ca CO2 -ul extrage apa in special din solutiile formate din formaldehide-apa (Krukonis, 1981b).
Divizarea unui azeotrop
Sistemul format din borat de trimetil si methanol
Asa cum a fost descries in paginile anterioare, valorile selectionate pentru o varietate de solventi SCF pentru etanol pot fi ridicate cam 50-80 la concentratii ale etanolului de cca. 10%, dar coeficientul de distributie al etanolului (y/x) alcool este de numai 0,1 (greutatea ca baza) in aceasta regiune. Cu un asemenea coeficient de distributie scazut, ratele solventului critic in jur de 10 sau mai mari sunt necesare pentru a exrage etanolul din apa. Mai departe, in niciunul din aceste studii nu a fost posibil sa se treaca peste concentratia azeotropica alcool-apa. In acest paragraf, descriem un studiu al lui Unterreiner, McHugh si Krukonis (1991) bazat pe abilitatea metanului critic de a extrage boratul de trimetil (TMB) din metanol si de desparti azeotropul TMB-metanol (70% TMB). Solutia azeotropica TMB-metanol rezulta din procesul sintetic de producere a TMB. Solutia rezultata TMB-metanol trebuie procesata intr-o coloana cu trei pasi de distilare sau de anumite combinatii de extractie si distilare. Sistemul TMB-metanol formeaza un scazut complex acid-baza Lewis, lucru care re loc cand oxigenul din metanol cedeaza o parte din electroni pe orbita incompleta borului (Kreevoy si Kautner, 1977).
Pentru a extrage TMB din amestecurile TMB-metanol este necesar sa se gaseasca un solvent care este relativ solubil in metanol si totusi este insolubil cu TMB in aceleasi conditii. TMB este foarte solubil in benzen, hexan, heptan, nonan si tetraclorura carbonica indicand ca acesta degaja caracteristici lipofilice (Plank si Christopher, 1976; Niswonger, Plank si Laukhuaf, 1965; Munster si altii, 1984). Totusi, TMB ar trebui sa fie solubil in solventi fluizi critici mai comuni cum ar fi etanolul si dioxidul de carbon. Metanolul este divizibil moderat cu xenon, etan, etilena si dioxid de carbon inca de cand o singura faza este obtinuta la presiuni mai mici de 20 bari la temperaturi dintre temperaturile critice respective ale componentelor binare (Brunner, 1985). Pentru a obtine rapid coeficientul de distributie estimate pentru TMB in dioxidul de carbon, etan si etilena, experimente rapide au fost efectuate cu un aparat dinamic la temperaturi pe o raza de la 0 la 55 grade Celsius si la o anumita presiune. Pentru studiul preliminar s-a dovedit ca dioxidul de carbon nu face discriminari intre TMB si metanol, desi la presiuni ridicate le dizolva pe ambele la nivele inalte. Etanul si etilenade asemenea nu pot separa TMB de metanol.
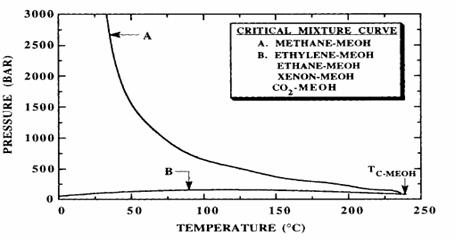
Figura 8.20 Curbele critice ale amestecului metanol cu metan, etan, etilena, xenon si dioxid de carbon (Robinson, Peng si Chung, 1985; Brunner, 1985; Francesconi, Lentz si Franck, 1981). Axele P-T pentru sistemele etan, etilena, xenon si dioxid de carbon nu se disting in aceasta zona din grafic. Dar la aproximativ 50 grade Celsius curbele amestecului etan-metanol cresc abrupt. Neprezentate in acest grafic sunt cele 3 linii ale fazelor relevate de sistemele etilena-metanol si etan-metanol in conditii apropiate de punctele lor critice.
Alte experimente au fost efectuate folosind metanul la garde Celsius si 150 bari cu asteptarea ca metanul nu ar fi la fel de puternic ca solvent critic ca si etanul, etilena sau dioxidul de carbon, pentru ca metanul are o densitate si polarizare scazuta. In aceste texte preliminare metanul a demonstrat o selectivitate ridicata pentru TMB legata de metanol. Acest rezultat nu ar trebui sa fie prea suprinzator, deoarece datele din studii arata ca metanul si metanolul nu sunt prea solubile (Francesconi, Lentz si Franck, 1981; Brunner, 1985). Figura 8.2. prezinta o parte a traseului P-T al curbelor critice ale amestecului pentru sistemul metan-metanol, etan-etanol, etilena-metanol si dioxid de carbon-metanol. Presiunile in exces de peste 2500 bari sunt necesare in camera cu temperatura pentru a obtine o singura faza cu etan, etilena, xenon sau dioxid de carbon (Robinson, Peng si Chung, 1985; Brunner, 1985). Datele P-T prezentate in figura 8.20 sugereaza ca puterea solventului metan-cel mai slab dintre solventii critici- prezentata in aceasta figura poate fi remodelata folosind presiunea, in timp ce alti solventi sunt prea puternici chiar si la temperaturi relativ scazute.
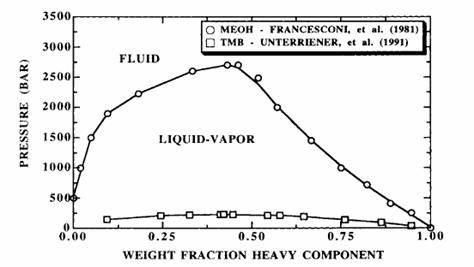
Figura 8.21 Comportamentul P-x al metanolului-metanului (Francesconi, Lentz si Franck, 1981) si sistemul TMB-metanol la 35 grade Celsius (Unterrier, McHugh si Krukonis, 1991)
Evidentele ulterioare referitoare la preferinta metanului pentru TMB legata de metanol este redata in figura 8.21. Presiunile modeste de 225 bari sunt necesare pentru a obtine o singura faza cu sistemul TMB-metan la orice concentratie. Dar, la aceeasi temperatura si concentratie pana la 2500 bari poate fi necesar cu sistemul metanol-metan. Aceasta presiune extrem de ridicata necesara penrtu a dizolva metanolul in metan este probabil rezultatul unei legaturi puternice a hidrogenului intre moleculele de metanol in faza lichida (Prausnitz, 1968; Franck si Deul, 1978). Densitatea metanului la 35 grade Celsius si aproximativ 2500 bari vine ca un factor al celor doua densitati ale metanolului lichid inainte ca dizolvarea completa sa fie obtinuta (Diguet, deul si Franck, 1987). Aceasta sugereaza ca metanul si metanolul trebuie puse aproape simultan pentru a permite fortelor slabe de atractie dintre metan si methanol sa aiba efect. Numai presiunile modeste sunt necesare pentru a solubiliza TMB in metan deoarece TMB interactioneaza pentru inceput prin intermediul fortelor de dispersie. Fortele de dispersie sunt mai putin compatibile cu metanul nonpolar. Diferentele in comportamentul metanului din faza binara cu TMB si cu metanolul sugereaza ca ar fi mai fezabil sa extragem TMB din metanol. Dar este necesar sa se determine informatiile despre comportamnetul din faza ternara, deoarece este cunoscut ca TMB-ul si metanolul formeaza un complex slab donor-acceptor care poate precede extractia eficienta a TMB din aceste amestecuri (Kreevoy si Kantner, 1977).
Figura 8.22 prezinta datele sistemului ternary TMB-metanol-metan la 35 grade Celsius si 152 bari, conditii asemnatatoare celor folosite in studiul prezentat. Cateva caracteristici ale diagramei indica faptul ca metanul este un solvent fluid critic recomandat pentru separarea TMB de metanol. Forma fazelor in doua regiuni si liniile releva faptul ca mai mult de 70% TMB (solvent-baza libera) poate fi obtinut in metanul-faza de extractie imbogatita daca amestecul azeotropic TMB-metanol este extras cu metan.
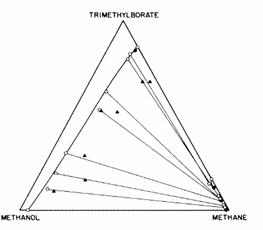
Figura 8.22 Datele procentuale ternare ale trimetil borat-metanol-metan la 35 grade Celsius si 152 bari (Unterreiner, McHugh si Krukonis, 1991). Simbolurile din afara triunghiului sunt exemple analizate, triunghiurile sunt incarcari si cercurile inchise sunt faze ale legaturilor determinate
Nu este numai incarcarea TMB in metanul in faza imbogatita destul de ridicat, aproximativ 12% ci este constant mereu pe masura ce concentratia TMB scade in faza lichida. Metanolul care este atasat la TMB are deasemenea molecule de hidrogen care se lega de alte molecule de metanol. Interactiunile intermoleculare dintre metan si metanol nu sunt destul de puternice pentru a concura cu legatura de hidrogen care are loc intre moleculele de metanol, deci metanolul ramane insolubil la aceasta presiune joasa. Desi cantitati mari de metan dizolvate in metanol abia desfac legatura de hidrogen (Diguet, Deul si Franck, 1987). Este interesant ca prezenta unor cantitati relativ mari de TMB in faza gazoasza a metanului imbogatit au un efect scazut asupra solubilitatii metanolului in aceasta faza, desi metanolul si TMB formeaza un complex slab. Aceasta lipsa de effect este suruprinzatoare.
Inca de cand curbele binodale intersectaeza axa TMB-metan, este posibil sa obtinem TMB pur folosind procesul de extractie contracurent cu reflux. Daca presiunea sistemului ar creste pana la presiunea critica a TMB-metanului la 35 grade Celsius, o faza formata din doua regiuni ar exista si nu ar fi posibil sa obtinem TMB-ul pur cu un proces contracurent.
Figura 8.2 prezinta rezultatele obtinute cand amestecul azeotrop TMB-metanol este extras. De remarcat ca concentratia TMB-ului in faza de extractie ramane constanta pe masura ce extractia continua, in corelatie cu tendintele din datele de echilibru prezentate in figura 8.22.
Diferenta scazuta in conditiile operatiei prezentata in figurile 8.22 si 8.23 nu se astepata sa aiba un effect semnificativ al datelor (Francesconi, Lentz si Franck, 1981). Datele prezentate in aceasta figura nu sunt neaparat datele de echilibru la ratele variabile folosite pentru extractie, desi se estimeaza ca solutia din coloana ajunge la aproximativ 80% din valoarea de echilibru.
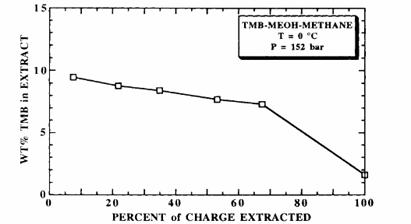
Figura 8.23 Peformanta extractiei dinamice a amestecului azeotropic trimetil borat-metanol folosind metanul critic (Unterrier, McHugh si Krukonis, 1991)
Linia concentratiei releva caracteristicile determinante cand se extrage numai o componenta (de exemplu, masurarea dinamica a solubilitatii unui lichid pur sau solid la o temperatura si presiune fixa, concentratia in extrasul din faza initiala ramane constanta, apoi scade rapid odata ce materialul din coloana devine mai putin). Datele distributiei TMB din tabelul 8.1 arata ca coeficientul de distributie cresc pe masura ce extractia continua. Coeficientul de distributie pentru TMB este deasemenea mai mare decat cel determinat cu etanolul extras din apa folosind solventul lichid critic.
Geometria diagramei din faza ternara ne permite sa aratm ca orice amestec lichid azeotropic poate fi divizat daca sistemul are curbe binodale asemanatoare celor prezentate in sistemul TMB-metanol-metan din figura 8.22. De exemplu, ar fi posibil sa despartim azeotropul etanol-apa cu un fluid critic daca sistemul este produs la o presiune scazuta cum ar fi acea axa etanol-SCF care este intersectata de curbele binodale. Inca de cand micibilitatea mutuala a apei si a hidrocarburilor sau a dioxidului de carbon este relativ insenzitiva la presiune in camera cu temperatura, presiunea de operare pentru procesul critic de extractie ar trebui sa fie mai scazuta decat presiunea necesara pentru a obtine o singura faza cu sistemul binar etanol-SCF. Numai presiunile scazute sunt necesare in camera cu temperatura pentru a obtine o singura faza pentru etanol cu etilena (Paulaitis, Gilbert si Nash, 1981; Ohgaki si altii, 1983), etan (McHugh, Mallett si Kohn, 1983) si dioxidul de carbon (Francis, 1954; Paulaitis, Gilbert si Nash, 1981), de aceea presiunea de extractie folosita in sistemul etanol -apa-SCF ar trebui sa fie foarte scazuta pentru a evita un ciclu in doua faze inchis. Desigur la limite scazute de presiune de operare in aplicatiile practice se foloseste solventul fluid critic pentru a diviza azeotropul etanol-apa inca de cand cantitatea de etanol din faza SCF-ului imbogatit ar fi destul de scazuta.
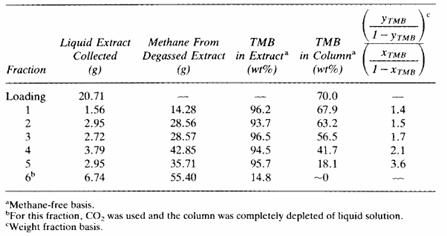
Tabelul 8.1 Datele secventiale ale extractiei pentru sistemul Trimetil Borat (TMB)-Metanol cu metan la 0 grade Celsius si 152 bari folosind o tehnica dinamica variabila (Unterrier, McHugh si Krukonis, 1991). Procentul de TMB din extract este masurat si cantarit procentul de TMB din coloana de extractie este calculat cu o aproximare de ±5% dintr-o masa a balantei
Acest comportament al solubilitatii este in contrast cu sistemul TMB-metanol-metan care are o solubilitate ridicata a TMB la presiuni sub 175 bari mentinand o solubilitate foarte scazuta a metanolului la o presiune scazuta. Desi prezenta unor cantitati ridicate de TMB in faza gazoasa a metanului imbogatit au un efect scazut asupra solubilitatii metanolului in aceasta faza.
Azeotropul TMB-metanol poate fi divizat la concentratia sa azeotropica folosind metanul critic la temperatura si presiuni normale.
Operand contracurent cu reflux este posibil sa se obtina TMB-ul pur, inca de cand curba binodala intersecteaza axa TMB-metan. Relativa legatura intre fortele intermoleculare in operatia din sistemul binar TMB-metanol, TMB-etan si metanol-metan si in sistemul ternar TMB-metanol-metan poate fi interpretat cu informatiile din tipurile de comportamene ale fazelor relevate de fiecare din aceste amestecuri binare si de proprietatile fizico-chimice ale fiecarei componente. TMB o substanta lipofilica se dizolva destul de rapid in metanul nepolar la presiuni scazute. Dar legaturile intermoeculare dintre metan si metanol nu sunt destul de puternice pentru a concura cu legatura de hidrogen din metanolul lichid la 35 grade Celsius pana la densitati ridicate ale metanolului sunt obtinute la presiuni de operare ridicate.
Comportamentul radical diferit al fazei binare a fost demonstrat pentru sistemele metan-TMB si metan-metanol. Aceasta sugereaza ca TMB-ul poate fi extras din metanol. Pentru a verifica aceasta informatie experimentala ce a fost obtinut pe baza sistemului TMB-metanol-metan daca complexul scazut TMB-metanol poate fi separat de metanul nepolar. Interesant, dioxidul de carbon, etanul si etilena, sunt toti solventi critici mai buni decat metanul dizolvati in metanol si TMB la o asemenea mare extindere la care nu sunt selective pentru orice componenta. Dar cu metanul, interactiunile dintre metan si TMB sunt destul de puternice pentru a mentine o concentratie constanta a TMB-ului in faza de extractie pe masura ce TMB-ul este inlaturat din faza metanolului lichid imbogatit. Aceasta inseamna ca coeficientul de distributie pentru TMB creste pe masura ce concentratia din faza lichida scde. Nu s-a mai cunoscut un sistem care sa aiba un asemenea tip de comportament al coeficientului de distributie.
Exempleledin acest capitol reliefeaza multe etape de dezvoltare a proceslor SCF si aplicatiilor pe care trebuie sa le acceseze, inteleaga si rezolve inainte de a obtine rezultatul final. O asemenea procedura este necesara pentru orice proces de separare. Extractia fluidului critic poate reduce costul energiei dar nu inseamna ca rezultatul va fi mai putin costisitor. Frecvent, capitalul si alte costuri operationale pot mai mult sa reduca costurile energiei. Discutiile din capitolele anterioare dezvolta aplicarea solventilor fluizi critici la solutii tehnico binare sau la problemele dificile de separare encomia in care performanta imbunattaita a materialelor procesate poate sprijini costul de procesare.
Copyright © 2025 - Toate drepturile rezervate