 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
Prin difuzie se intelege modificarea pozitiilor atomilor in metale pe distante mari in raport cu distantele interatomice. Difuzia este determinata de agitatia termica a atomilor; la cresterea temperaturii se mareste viteza de difuzie. Se precizeaza faptul ca prin difuzie se intelege nu deplasarea individuala a atomilor ci fluxul macroscopic de atomi determinat de aceste deplasari.
Considerand difuzia unui element chimic in altul este posibil sa se produca numai modificarea compozitiei chimice - caz in care difuzia se numeste atomica. In cazul in care prin difuzie se formeaza noi faze, difuzia se numeste de reactie. Difuzia se poate produce si in lipsa unei diferente de concentratie chimica, cand se deplaseaza atomii aceluiasi element, caz in care se numeste autodifuzie. Difuzia este un proces de mare importanta, ea sta la baza celor mai importante transformari care se produc in metale si aliaje ca: solidificari, transformari de faza, recristalizari, tratamente termice, etc.
Difuzia se realizeaza prin salturi atomice care au ca efect crearea unor fluxuri macroscopice de atomi dintr-o parte a metalului in alta.
In solutii solide de substitutie pot exista mai multe mecanisme pentru realizarea difuziei (fig. ) ca:
schimbarea reciproca a locurilor intre doi atomi vecini;
difuzia prin internoduri;
difuzia prin deplasarea ciclica a unor grupari de atomi;
difuzia prin intermediul vacantelor.
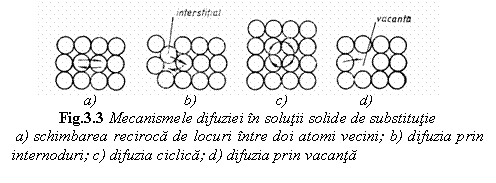
Cel mai probabil mecanism de difuzie in soluti solide este difuzia prin intermediul vacantelor; el consta in trecerea unui atom aflat intr-un nod al retelei cristaline intr-un loc vacant vecin. In nodul din care a plecat se formeaza o noua vacanta care poate fi ocupata de atomul vecin si asa mai departe. In acest fel se realizeaza o deplasare continua a vacantelor, acest mecanism explica valoarea mare a coeficientului de difuzie.
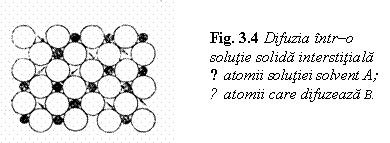
In
solutiile solide interstitiale de atomi B in A, atomii elementului B
care difuzeaza au diametrul atomic foarte mic si ocupa
pozitii interstitiale, putand migra cu usurinta
dintr-o pozitie in alta (fig. 4.). In acest caz difuzia se realizeaza
prin internoduri.
Cauzele difuziei sunt agitatia termica si fluctuatiile termice, ultimele furnizand atomilor energia necesara pentru ca ei sa poata trece prin salturi din pozitii de echilibru in locuri vacante sau din interstitiile pe care le ocupa in interstitii vecine libere. Frecventa salturilor f cu care un atom trece dintr-o pozitie in alta este:
![]()
unde:
![]() - frecventa de vibratie a atomilor;
- frecventa de vibratie a atomilor;
Qa - energia de activare a difuziei.
Difuzia in metalele solide este descrisa matematic cu ajutorul a doua ecuatii diferentiale numite legile lui Fick. Prima lege a difuziei descrie viteza cu care se produce difuzia atomilor aflati la concentratia C intr-un volum de material. Datorita tendintei de egalizare a continutului de atomi B in solvent se creeaza un flux de atomi B a caror concentratie variaza cu distanta x si cu gradientul de concentratie dc/dx. Daca se noteaza cu J fluxul de atomi care strabate unitatea de suprafata in unitatea de timp, pe directia perpendiculara pe axa x, potrivit primei legi a difuziei acest flux este:
![]()
unde: D - coeficient de difuzie egal cu : ![]()
Semnul minus din relatie semnifica faptul ca tendinta de miscare a atomilor este de la concentratii mai mari catre concentratii mai reduse. Coeficientul de difuzie D este egal cu numarul de atomi ce difuzeaza intr-o secunda, printr-o suprafata perpendiculara pe directia fluxului, egala cu unitatea, la o variatie unitara a concentratiei (dc/dx = 1). Ecuatia dimensionala a coeficientului de difuzie este L2T-1 sau cm2 /s. Potrivit primei legi a difuziei fluxul de material este proportional cu gradientul de concentratie. Daca concentratia se exprima in g / cm3, fluxul se noteaza cu m si este egal cu cantitatea de material (in grame) care trece intr-o secunda printr-o sectiune egala cu unitatea. In acest caz prima lege a difuziei se scrie:
![]()
Legea a doua a difuziei deriva din prima lege si exprima dependenta difuziei de timp. Pentru difuzia monodimensionala aceasta lege este data de relatia:
![]()
Pentru cazul tridimensional legea a doua devine:
![]()
Pentru un mediu izotrop Dx = Dy = Dz =D, avem
![]()
unde ![]() este operatorul
Hamilton.
este operatorul
Hamilton.
Valoarea coeficientilor de difuzie este influentata de temperatura, de concentratia in solutie a atomilor care difuzeaza si de prezenta imperfectiunilor in reteaua cristalina. In metale si aliaje solide coeficientii de difuzie au valori de ordinul 10-10 cm2 / sec, in timp ce in metalele lichide valorile sunt de ordinul 10-5 cm2 / sec. Variatia cu temperatura a coeficientilor de difuzie este o exponentiala de tip Arhenius, data de relatia:
![]()
unde:
R - constanta generala a gazelor;
T - temperatura absoluta;
Ea - energia de activare a difuziei;
D0 - factorul de frecventa independent de temperatura care pentru metale si aliaje solide este cuprins intre 0,1 - 10 cm2 / sec.
Energia de activare a difuziei prin dislocatii este egala cu difuzia prin limita de graunte si aproximativ jumatate din difuzia volumica:
Edislc ≈ EL ≈ 1/2Ev
Solutiile particulare ale ecuatiilor de difuzie sunt aplicabile unor cazuri practice de tratamente ale metalelor si aliajelor ca:
Difuzia in regim stationar
Gradientul de concentratie al substantei difuzate este constant in
timp ![]() si in
consecinta:
si in
consecinta:
![]() sau
sau ![]()
Solutia se aplica spre exemplu la difuzia gazelor in metale solide prin aplicarea unei presiuni pe cele doua fete ale unei table;
Difuzia in regim nestationar - sistem infinit
Solutia se aplica de
exemplu la cementarea in mediul gazos a unei piese din otel pentru
carburarea statului superficial, in scopul maririi rezistentei la
uzura. Pentru exemplificare se considera (C - C0) / (Cs
- C0) = , deci o concentratie C situata la jumatatea intervalului
intre concentratia suprafetei Cs si concentratia
initiala a miezului presei C0;
in acest caz utilizand functia eroare se obtine x / 2![]() = 0,52; rezulta x = 1,04
= 0,52; rezulta x = 1,04![]() , relatie valabila pentru orice durata de
difuzie. Generalizand rezulta: x = k
, relatie valabila pentru orice durata de
difuzie. Generalizand rezulta: x = k![]() , deci adancimea de penetratie x variaza parabolic
cu durata de difuzie t.
, deci adancimea de penetratie x variaza parabolic
cu durata de difuzie t.
Coeficientul de difuzie nu este o marime constanta ci depinde de foarte multi factori ca: temperatura, concentratia, impuritatile prezente si marimea de graunte. O influenta deosebit de puternica asupra coeficientului de difuzie exercita temperatura. La fiecare crestere cu 200C a temperaturii difuzia se dubleaza. Cresterea coeficientului de difuzie cu temperatura este exponentiala. Coeficientul de difuzie depinde si de concentratie. In cazul austenitei coeficientul de difuzie variaza cu continutul de carbon conform relatiei lui Mehl:
![]()
Copyright © 2026 - Toate drepturile rezervate