 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
METODA RAPIDA FEULGEN DE COLORARE A NUCLEULUI SI CROMOZOMILOR CU FUXINA BAZICA
Aceasta metoda a fost propusa de R. Feulgen si A. Rosenbeck (1924) si apoi modificata de De Tomasi (1936). In histochimie reactia Feulgen pozitiva este considerata ca un indiciu sigur al prezentei acidului dezoxiribonucleic.
In celulele in diviziune, numai cromozomii se coloreaza electiv in rosu-violaceu cu fuxina, in timp ce in celulele aflate in interfaza, ARN-ul din nucleoli si citoplasma nu se coloreaza.
Colorarea se realizeaza cu o solutie de fuxina bazica decolorata (Reactiv Schiff), care se recoloreaza la nivelul cromatinei sau a cromozomilor. Printr-o usoara hidroliza cu HCl 1N, la 60o C, se elibereaza grupele aldehidice din ADN, dupa care urmeaza o reactie chimica intre grupele aldehidice eliberate si fuxina bazica, din care rezulta o coloratie rosie-violacee a cromozomilor si nucleului interfazic.
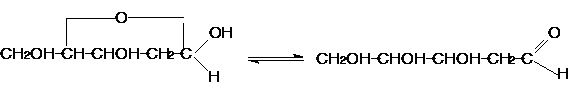
In efectuarea preparatelor dupa aceasta metoda se disting mai multe etape:
Prefixarea, sau tratamentul preliminar al materialului de studiu, are rolul de a inhiba formarea fusului nuclear si de a asigura astfel acumularea de metafaze cu cromozomi contractili. Pentru prefixare se poate folosi o solutie de colchicina 0,01%, timp de 3 ore. Mai recent se foloseste in acelasi scop, o emulsie de α-bromnaftalen. Se pun 2-3 ml emulsie intr-o eprubeta mica, in care se introduc apoi varfuri de radacini, detasate de la boabe germinate si se lasa 4-5 ore.
Fixarea are rolul de a omora celulele si de a asigura coagularea constituientilor celulari, evitand pe cat posibil, modificarea structurii interne a celulelor. Ca fixator, in cazul acestei metode, se foloseste acidul acetic 45%, la temperatura de +2oC. In fiolele cu radacini, dupa indepartarea emulsiei de α-bromnaftalen, se introduc 2-3 ml de acid acetic 45% si se introduc in frigider pentru 12 ore.
Hidroliza, are rolul de a asigura macerarea tesuturilor prin dizolvarea partiala a substantelor pectice, astfel sa faciliteze procesul de colorare si apoi de etalare a celulelor pe lama. Se foloseste HCl 1N, la temperatura de 60oC, in termostat, unde se pastreaza exact 12 minute in cazul radacinilor de grau si secara. Hidroliza se poate face in aceleasi fiole de sticla, dupa ce a fost indepartat fixatorul.
Colorarea se efectueaza cu o solutie de fuxina bazica decolorata (Reactiv Schiff). La sfarsitul hidrolizei se indeparteaza HCl din fiole si se adauga 2-3 ml colorant. Dupa 10-15 min se poate observa colorarea in rosu-violaceu a regiunii meristematice din varful radacinii. Pentru intensificarea colorarii se lasa radacinile in solutie 30 min.
Efectuarea preparatului microscopic, se realizeaza prin etalarea materialului dupa metoda "squash" (zdrobire), pe o lama, intr-un strat subtire, pe cat posibil intr-un singur rand de celule. Pe o lama degresata cu alcool se pune o picatura mare de acid acetic 45%, in care se aseaza numai portiunea colorata din varful radacinii, apoi peste radacina se aplica o lamela care a fost obdusa cu o pelicula fina de albumina glicerinata si trecuta usor prin flacara unui bec de gaz, pentru coagularea albuminei. Cu un bat de lemn (varf de creion) se loveste sistematic in lamela, pana cand se realizeaza o etalare cat mai buna. Se inveleste apoi degetul mare sau cel aratator al mainii, in hartie de filtru si se apasa uniform si puternic pe lamela. Preparatul astfel obtinut se examineaza la microscop, iar pentru marirea contrastului se poate utiliza un filtru verde.
Un preparat bine realizat trebuie sa prezinte nucleii si cromozomii colorati intens in rosu-violaceu, citoplasma incolora, celulele sa fie bine etalate, cromozomii sa fie dispersati si individualizati. Preparatul astfel obtinut poate fi pastrat in frigider, timp de 1-3 zile si examinat treptat la microscop.
De asemenea radacinile pot fi pastrate cateva zile in fixator si efectuarea preparatelor se poate face treptat.
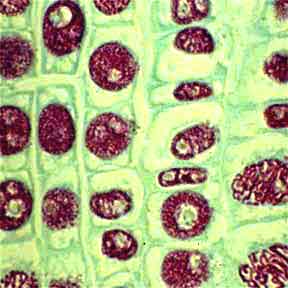
Testul Feulgen in lumina verde
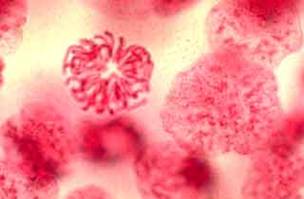
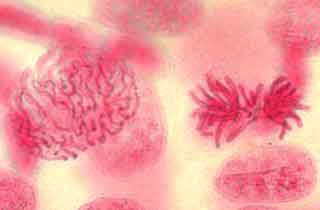
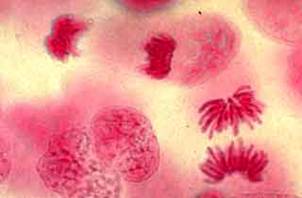
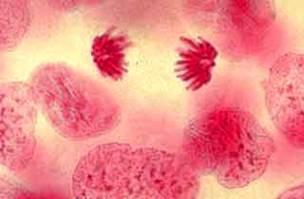
Testul Feulgen: diferite faze ale diviziunii mitotice
TESTUL BRACHET PENTRU LOCALIZAREA IN CELULA
A ADN SI ARN
Dintre diferitele metode utilizate pentru detectarea microhistochimica a celor doua tipuri de acizi nucleici din interiorul celulei, metoda preconizata de Brachet, da cele mai bune rezultate.
In acest scop se foloseste un amestec de coloranti format din verde de metil si pironina. Verdele de metil va colora ADN-ul in verde iar pironina va colora ARN-ul in rosu.
Se folosesc sectiuni in parafina efectuate la microtom din meristemul radicular de grau sau usturoi, dupa tehnica descrisa la lucrarea 1 si 2. Dupa ce sectiunile au fost etalate pe lama si uscate, se deparafineaza si apoi se hidrateaza, apoi se mentin 10-15 min in amestecul de verde de metil-pironina. Se spala apoi excesul de colorant prin trecerea succesiva a lamei prin apa, dilutiile de alcool absolut si toluen, un timp foarte scurt, spre a evita dizolvarea si eluarea din preparat a verdelui de metil. Urmeaza apoi includerea in balsam de Canada si efectuarea preparatului fix.
Dupa montarea preparatului la microscop se va face observarea cu ob. 40x si O.I. 90x. Se vor putea observa atat celulele cu nuclei interfazici cat si celulele cu nuclei in diviziune. Nucleul apare colorat in albastru-verzui, cu exceptia nucleolului care se coloreaza in rosu. In citoplasma vom putea observa numeroase granulatii fine, ce reprezinta ribozomii si care se coloreaza in rosu-deschis.
In cazul celulelor aflate in diviziune, cromozomii apar colorati in albastru-verzui, iar citoplasma cu granulatii rosii.
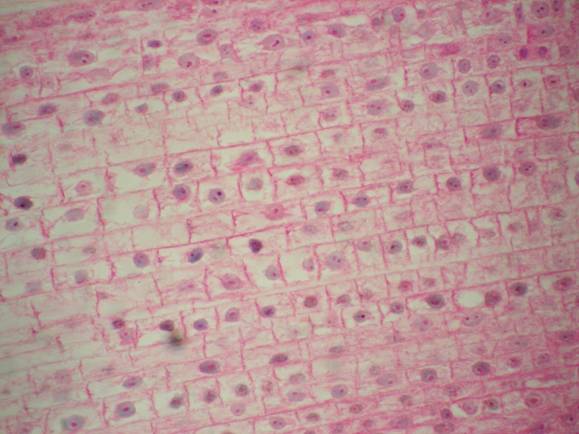
Reactivi:
α-brom-naftalen: se agita puternic, cateva minute, intr-o sticla cu dop rodat, un amestec de 75 ml apa distilata si 25 ml α-brom-naftalen. Se lasa apoi sa se depuna excesul de bromnaftalen pe fundul sticlei. Prentru prefixare se va folosi faza superioara.
Acid acetic 45%: 45 ml acid acetic glacial se dilueaza cu 55 ml apa.
Reactiv Schiff: peste 1 g fuxina pudra se toarna 200 ml apa distilata incalzita la 100oC, se agita si se lasa sa se raceasca la 50oC. Se filtreaza si se adauga 30 ml HCl 1N si 3 g metabisulfit de K (K2S2O5) cristale si se lasa solutia 24 ore intr-o sticla bine inchisa, la intuneric si rece, dupa care solutia capata o culoare galbuie. Pentru decolorare se mai adauga 0,5 g carbune vegetal, se lasa 1 min si se filtreaza repede, printr-o hartie de filtru grosiera. Solutia se pastreaza in sticle brune la intuneric si rece.
Intrebari:
R. Feulgen se desfasoara in conditii controlate. Care sunt acestea?
Care este rolul hidrolizei acide?
Enumerati etapele care se parcurg pentru realizarea preparatului in cadrul testului Brachet.
Copyright © 2025 - Toate drepturile rezervate