 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
Fenomene capilare
1. Interfata solid - lichid
Fenomenele superficiale au loc si la contactul dintre solid si lichid. In acest caz trebuie sa se tina cont atat de fortele de coeziune FC dintre moleculele lichidului, cat si de fortele de adeziune FA dintre moleculele solidului si ale lichidului. Aceste forte au un rol important in forma suprafetelor libere a lichidelor in regiunea de contact cu solidul.
Suprafata libera a lichidului dintr-un vas cu sectiune mare
poate fi plana, cand rezultanta ![]() a fortelor de
coeziune si adeziune este indreptata in lungul peretelui vasului, sau
sub forma de menisc. Meniscul este concav cand
a fortelor de
coeziune si adeziune este indreptata in lungul peretelui vasului, sau
sub forma de menisc. Meniscul este concav cand ![]() este orientata
spre exteriorul vasului, in acest caz lichidul uda solidul. Daca
este orientata
spre exteriorul vasului, in acest caz lichidul uda solidul. Daca ![]() este indreptata
spre interior, meniscul este convex si lichidul nu uda solidul.
Rezultanta este perpendiculara pe tangenta dusa la suprafata
libera in unghiul de racord q. Suprafata de la mijlocul vasului este orizontala, deoarece in
aceasta zona actioneaza numai fortele de coeziune.
este indreptata
spre interior, meniscul este convex si lichidul nu uda solidul.
Rezultanta este perpendiculara pe tangenta dusa la suprafata
libera in unghiul de racord q. Suprafata de la mijlocul vasului este orizontala, deoarece in
aceasta zona actioneaza numai fortele de coeziune.
Un solid in raport cu lichidele (Fig.5.3) poate fi:
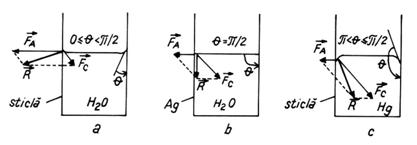
Fig.5.3. Forma suprafetelor libere a lichidelor la contactul cu diferite solide: a) menisc concav (solid liofil); b) suprafata orizontala (solid indiferent); c) menisc convex (solid liofob).
a) solid liofil (hidrofil in cazul
apei) cand ![]() >
> ![]() si 0 < q < p/2,
menisc concav, fiind udat de lichid;
si 0 < q < p/2,
menisc concav, fiind udat de lichid;
b) solid indiferent cu q p/2, suprafata libera a lichidului fiind orizontala;
c) solid liofob (hidrofob) cand ![]() <
< ![]() , p < q < p/2,
menisc convex, lichidul nu uda solidul.
, p < q < p/2,
menisc convex, lichidul nu uda solidul.
2. Capilaritatea
Consideratiile prevazute in paragraful anterior se regasesc si in cazul tuburilor cu diametre mici (10-6 < d <10-3), numite tuburi capilare. Cu ajutorul lor se pune in evidenta fenomenul cunoscut sub numele de capilaritate, care consta in urcarea sau coborarea lichidului in tub in raport cu nivelul lichidului din vas.
In cazul suprafetelor curbe din tuburile capilare, fortele de tensiune superficiala, care actioneaza tangent in fiecare punct al meniscului, au o componenta indreptata in lungul tubului. Rezultanta acestor componente se numeste forta Laplace si este orientata spre exteriorul lichidului pentru meniscul concav, respectiv spre interior in cazul meniscului convex (Fig.5.4.). Forta Laplace va determina aparitia unei presiuni suplimentare capilare, ps, de forma:
ps = 2s / r (5.4)
unde r este raza capilarului.
Deci, sub actiunea fortelor de tensiune superficiala la nivelul meniscului are loc un salt de presiune Dp, expresia pentru meniscul ideal fiind:
Dp = pext - pint = 2s / r (5.5)
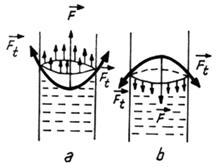
Fig. 5.4. Forta Laplace; a) menisc concav si b) menisc convex.
Datorita acestui salt presiunea de-a lungul capilarului variaza astfel: sub meniscul concav este p0 - 2s/r, deci mai mica decat presiunea atmosferica (p0), si creste spre baza tubului capilar ajungand la nivelul lichidului din vas egala cu p0. Deci, in tot capilarul presiunea este mai mica decat cea atmosferica, si lichidul urca in tub. In cazul lichidului care nu uda peretii capilarului, fenomenele se petrec invers, are loc o depresiune capilara, respectiv o scadere a presiunii in tubul capilar de la valoarea p0 + 2s/r la nivelul meniscului convex pana la p0, la baza tubului capilar.
In cazul lichidelor reale, in expresia presiunii suplimentare trebuie sa se tina cont si de contributia unghiului de racord dintre suprafata libera si peretii tubului.
Ascensiunea pentru tuburile capilare liofile si depresiunea capilara pentru tuburile capilare liofobe este data de legea lui Jurin:
![]() (5.6)
(5.6)
unde s - coeficientul de tensiune superficiala, r - densitatea lichidului, g - acceleratia gravitationala, r - raza capilarului si q -unghiul de racord.
Capilaritatea este un fenomen foarte des intalnit in lumea vie, dar este produs si pe cale artificiala. Astfel, sta la baza ascensiunii sevei in tulpinile si frunzele plantelor, contribuie la circulatia sangvina in capilarele organismelor vii, la mentinerea umiditatii solului. Utilizarea hartiei de filtru, a buretelui si vopsirea fibrelor se bazeaza tot pe fenomene capilare.
5.3. Adsorbtia
La nivelul interfetelor dintre doua faze pot aparea modificari de concentratie ale substantelor aflate in contact. Astfel, substantele liofobe se aglomereaza la suprafata lichidului, concentratia superficiala fiind mult mai mare decat cea din volumul de lichid, determinand scaderea tensiunii superficiale. Deci, apare o repartitie inegala a substantelor intre fazele sistemului heterogen.
Adsorbtia este fenomenul de acumulare si fixare a moleculelor unei substante pe suprafata unui suport lichid sau solid. Faza care retine moleculele se numeste adsorbant, iar substanta care se fixeaza se numeste adsorbit.
Observatie Adsorbtia este un fenomen de suprafata, spre deoserbire de absorbtie care este un fenomen de volum.
Fenomenul de adsorbtia se poate clasifica dupa mai multe criterii.
Din punct de vedere al interfetelor exista:
adsorbtie gaz-lichid;
adsorbtie gaz-solid
adsorbtie lichid-lichid;
adsorbtie lichid-solid.
Pentru biologie, importanta deosebita prezinta ultimele doua interfete.
In functie de tipul de interactiune de la suprafata de separare:
adsorbtie fizica - permite formarea pe suprafata adsorbantului a unui strat, de regula monoatomic, sub actiunea fortelor van der Waals.
adsorbtie chimica (chemisorbtie) - adsorbantul formeaza un complex molecular nou cu adsorbitul prin diferite tipuri de legaturi chimice.
3. In functie de marimea fortelor dintre moleculelor adsorbantului, F0 , si a fortelor dintre moleculele de adsorbant si adsorbit, F,:
adsorbtie pozitiva - cand F0 > F, atunci moleculele adsorbitului sunt " impinse" spre patura superficiala, unde creste concentratia lor. Acest tip de adsorbtie se intalneste la substantele tensioactive.
adsorbtie negativa - cand F0 < F, atunci moleculele adsorbitului se acumuleaza in volumul lichidului, si de fapt, practic este absorbtie. Se intalneste la solutiile de electrolit.
Adsorbtia este un proces in mare masura reversibil, fenomenul invers se numeste desorbtie. Cele doua procese au un anumit grad de selectivitate si, din acest motiv, au o larga aplicabilitate in cromatografie, pentru separarea prin elutie a componentelor unui amestec fixat pe un suport.
TEME:
Ce reprezinta interfata. Exemple.
Cum se defineste coeficientul de tensiune superficiala.
Fenomenul de capilaritate.
Ce este adsorbtia.
Copyright © 2026 - Toate drepturile rezervate