 | Alimentatie | Asistenta sociala | Frumusete | Medicina | Medicina veterinara | Retete |
Metabolismul nucleotidelor pirimidinice si purinice
In functie de natura bazelor azotate din structura lor, nucleotidele se clasifica in purinice si pirimidinice. Prin numeroasele utilizari ale lor cea mai studiata este incorporarea in acizii nucleici ADN (replicarea) si ARN (transcriptia).
Nucleotidele purinice servesc ca sursa de energie libera (ADP + Pi → ATP), mesageri secunzi ai semnalelor reglatoare (AMPc, GMPc), sunt componente ale unor metaboliti cu rol detoxifiant ca 3'-fosfoadenozil fosfosulfat (PAPS) sau donori de grupe metil (S-adenozilmetionina). Nucleotidele pirimidinice servesc la sinteza altor compusi macroergici, donori de glucide in sinteza glicogenului (UDP-glucoza) sau pentru sinteza glicoproteinelor (UDP-galactoza). Analogii sinte-tici ai nucleotidelor naturale sau ale componen-telor lor (derivati de nucleobaze, nucleozide) constituie un important grup al farmacopeei oncologice. Ei sunt folositi in chemoterapia cancerului pentru inhibarea proliferarii tumorilor canceroase sau distrugerea unor virusi deoarece pentru ca o celula sa se divida, ADN-ul propriu trebuie sa sufere replicarea si acest proces nece-sita nucleotide purinice si pirimidinice normale. Un analog sintetic in care este modificata fie structura bazei azotate (nucleobaza), fie a partii glucidice (riboza sau deoxiriboza) induce efecte toxice atunci cand este incorporat in acizii nucleici sau alti constituenti celulari. Aceste efecte sunt de doua feluri:
(i) inhibitia enzimelor implicate in sinte-za acizilor nucleici si
(ii) incorporarea analogilor insisi, datorita asemanarii lor structurale cu nucleotidele natura-le, in componenta acizilor nucleici, ceea ce alte-reaza imperecherea bazelor pe principiul comple-mentaritatii lor (Watson-Crick) si, prin urmare produce alterarea transferului de informatii ge-netice.
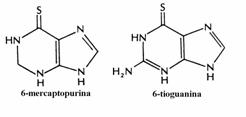
Exemple sunt 5-fluoro-uracilul si 5-bromo-uracilul, analogii sintetici ai bazei timina. Simi-lar, 6-tioguanina si 6-mercaptopurina sunt ana-logi ai guaninei respectiv inozinei. Compusii din grupa aza, ca 6-azauridina si 6-azacitidina, sunt analogi ai nucleozidelor uridina si citidina iar citarabina (arabinozil-citozina) este analog al ci-tidinei.
1. Biosinteza de novo a nucleotidelor piri-midinice
Experimente cu markeri radioactivi au aratat ca atomii N(1), C(4), C(5) si C(6) ai ciclului pirimidinic provin din scheletul acidului aspartic, atomul (C) provine din CO2 si atomul N(3) este preluat de la glutamina.
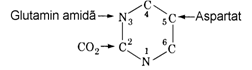
1. Sinteza carbamoil fosfatului este prima reactie a biosintezei pirimidinelor, enzima fiind carba-moil fosfat sintetaza II existenta in citosol. Una din cele doua molecule de ATP care se consuma in reactie furnizeaza o grupare fosfat iar cealalta contribuie cu energia necesara la carboxilarea azotului aminic, fara implicarea biotinei, coen-zima tipica angajata in reactiile de carboxilare la atomul de carbon. Am vazut la ciclul ureogenetic ca enzima similara, carbamoil fosfat sintetaza I, catalizeaza carboxilarea si fosforilarea unui atom de azot din amoniac si este localizata in mitocon-drie. La procariote exista o singura sintetaza care catalizeaza ambele cai metabolice (pirimidinoge-neza si ureogeneza).
2. Sinteza carbamoil aspartatului este catalizata de aspartat transcarbamoilaza (ATC).
Formarea dihidroorotatului are loc prin inchi-derea ciclului catalizata de dihidoorotaza. Primele 3 enzime, sintetaza II, ATC si dihidroorotaza fac parte dintr-o singura proteina trifunctionala la eucariote. Aceasta proteina numita CAD, consta din 3 catene polipeptidice identice avand mase moleculare de 230 kDa, fiecare continand cei 3 centri activi ai enzimelor aratate. Integrarea acestor enzime intr-un complex multienzimatic este de asteptat datorita caracterului relativ dezor-ganizat al citosolului.
4. Oxidarea dihidroorotatului este o reactie reversibila catalizata de dihidroorotat dehidro-genaza, enzima eucariotica continand FMN si fer neheminic fiind asociata la membrana interna mitocondriala. Chinone intermediaza transferul atomilor de hidrogen. Aceasta dehidrogenaza este singura enzima mitocondriala toate celelalte enzime ale pirimidinogenezei fiind citosolare.
Plasarea dihidroorotatului pe fosforiboza are loc cu implicarea compusului macroergic 5-fosforibosil-pirofosfat (PRPP) rezultand orotidin-5'-monofosfat (OMP). Reactia este catalizata de orotat fosforil transferaza care poate actiona si ca "enzima de salvare" pentru baze pirimidinice ca uracilul si citozina pe care le transforma in nucleotidele monofosforice corespunzatoare.
Figura 28. Biosinteza de novo a UMP. Inelul pirimidinic este sintetizat inaintea atasarii la inelul ribozic.
6. Formarea UMP are loc prin decarboxilarea OMP de catre OMP decarboxilaza. La animale reactiile 5 si 6 sunt catalizate de o singura catena polipeptidica ceea ce releva integrarea in com-plexe multienzimatice a urmatoarelor enzime citosolare (reactia 4 este catalizata de o enzima mitocondriala). Integrarea reactiilor 1,2,3,5 si 6 creeaza conditiile canalizarii intermediarilor pen-tru a parcurge succesiunea de reactii cu viteza mare, protejati fata de actiunea degradatoare a altor enzime celulare.
7.si 8. Sinteza UDP si UTP are loc prin actiunea secventiala a nucleozid monofosfat kinazei si nucleozid difosfat kinazei:
UMP+ATP↔UDP+ADP UDP+ATP↔UTP+ADP
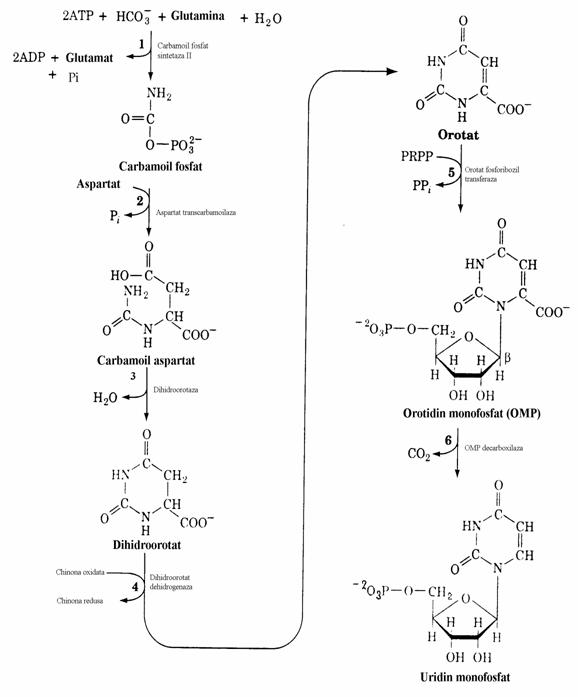
Conversia UTP in CTP are loc sub actiunea CTP sintetazei.
Figura 29. Sinteza CTP din UTP.
 1.2. Reglarea biosintezei nucleotidelor
pi-rimidinice
1.2. Reglarea biosintezei nucleotidelor
pi-rimidinice
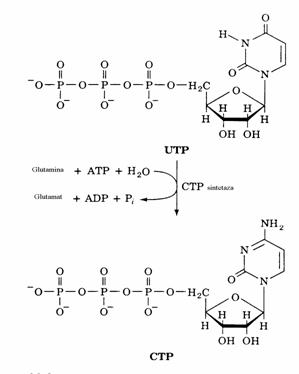
Aspartat transcarbamoilaza (ATC) este principala enzima reglatoare la bacterii (fig. 30)
Asocierea moleculelor substraturilor carbamoil-fosfatul si aspartatul este cooperativa, ceea ce determina forma sigmoidala a curbei viteza-con-centratia. CTP inhiba enzima prin micsorarea afi-nitatii acesteia fata de substrat, fara sa afecteze numarul de turnover (viteza maxima). Inhibitia poate atinge 90%.
ATP este un activator al ATC. Acesta mareste afinitatea enzimei fata de substrat fara sa afecteze vmax. In plus, legarea CTP si ATP la centrul alosteric este competitiva (un singur centru alosteric pentru ATP si CTP). Concentratii mari de ATP deplaseaza CTP de pe enzima care nu-si mai poate exercita efectul inhibitor. Semni-ficatia activitatii ATC-azei de ATP este dubla:
a) Sunt egalizate vitezele de formare ale nucleotidelor purinice si pirimidinice ceea ce satisface necesarul in raportul 1:1.
b) Sunt puse de acord vitezele reactiilor consu-matoare de ATP(sinteza carbamoil-P, fosfori-larea UMP si UDP) cu rezerva de ATP. Deci daca ATP creste, creste sinteza precursorilor reactiilor consumatoare de ATP. La animale ATC nu este enzima reglatoare. Biosinteza pirimidi-nelor este controlata si la nivelul carbamoil fosfat sintetazei II (fig. 30). Aceasta este inhibata de UDP si UTP si este activata de ATP si PRPP.
Figura 30. Controlul biosintezei pirimidinelor la E. coli (a) si la animale (b). Inhibitia retroactiva are loc la nivelul enzimelor indicate cu octogon. Activarea este indicata cu patrate pline.
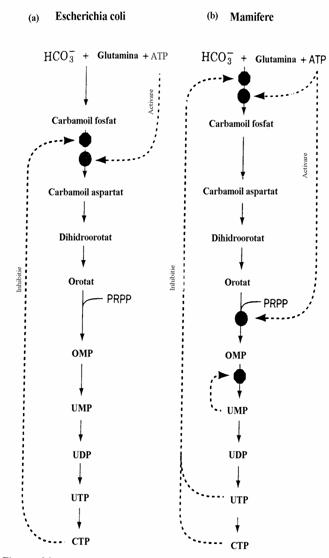
La animale ATC-aza nu este enzima reglatore. Biosinteza pirimidinelor este controlata la nivelul carbamoil fosfat sintetazei II (fig. 30). Aceasta este inhibata de UDP si UTP si este activata de ATP si PRPP. Al doilea nivel de reglare a caii la mamifere este OMP decarboxi-laza care este inhibata competitiv de UMP. La toate organismele productia de OMP variaza cu nivelul precursorului PRPP.
Aciduria orotica ereditara este caracte-rizata prin tulburari de crestere, anemie megalo-blastica severa, excretia unor mari cantitati de acid orotic (cristalurie orotica). Baza biochimica a excretiei de acid orotic este absenta orotat fos-foribozil transferazei si/sau orotidilat decar-boxilazei.
Cu toate ca boala este rara, intelegerea bazei me-tabolice a ei a permis aplicarea unui tratament adecvat si confirmarea etapei reglatoare a biosin-tezei pirimidin nucleotidelor.
Cand acesti pacienti sunt alimentati (per oral) cu citidina sau uridina ei prezinta o evidenta ame-liorare a manifestarilor hematologice precum si o descrestere a excretiei de acid orotic. Explicatia consta in faptul ca aceste nucleozide adminis-trate sunt transformate in nucleotide, astfel fiind ocolit blocajul de la nivelul celor doua enzime. Scheletele lor intra in procesele de crestere celulara ca de exemplu in procesul eritropoietic care sunt intense in sintezele de ARN si ADN. Prin urmare este eliminata anemia. In plus, for-marea CTP si a UTP din aceste nucleozide, prin feed-back negativ, inhiba aspartat transcarba-moilaza si carbamoil-fosfat sintetaza II, enzime precursoare sintezei de acid orotic, ceea ce reduce excretia de acid orotic.
Deoxiribonucleotidele
pirimidinice si purinice sunt sintetizate din ribonucleotidele
corespunzatoare prin reducerea atomului de carbon C(2΄) al acestora
din urma, nu prin sinteza de novo din precursori care
contin deoxiriboza. 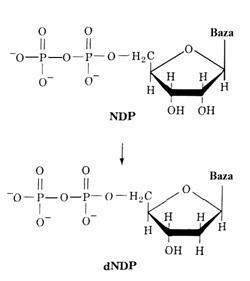
Enzimele care catalizeaza aceasta transformare se numesc ribonucleotid reductaze. Se cunosc 3 tipuri de reductaze de acest fel:
Figura 31. Reciclarea ribonucleotid reductazelor prin reducere cu tioredoxina redusa.
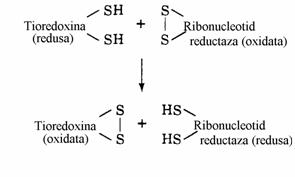
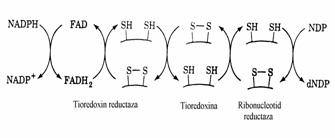
Figura 32. Sistemul de transfer electronic prin care puterea reducatoare reduce un ribonucleotid.
 1.4. Formarea timinei
1.4. Formarea timinei
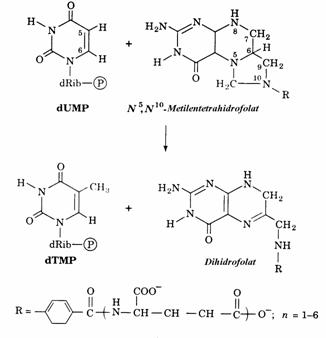
dTMP, component al ADN, se formeaza prin metilarea dUMP de catre un donor de grupa-re metil, sub actiunea timidilat sintazei(fig. 33).
Figura 3 Sinteza dTMP din dUMP. Enzima catali-zatoare este timidilat sintaza.
1.5. Agenti anticancerosi
Reciclarea acidului dihidrofolic(DHF) pentru sinteza N5,N10-metilentetrahidrofolatului are loc prin parcurgerea unei secvente de 2 reactii (fig. 34) cu participarea enzimelor dihidrofolat reductaza si serin hidroximetil transferaza.
Figura 34. Sistemul enzimelor timidilat sintaza-DHF reductaza-serin hidroximetil transferaza catalizeaza
un ciclu metabolic prin care dUMP este convertit in dTMP cu participare puterii reducatoare si a serinei.
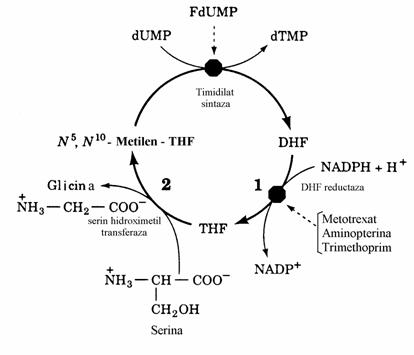
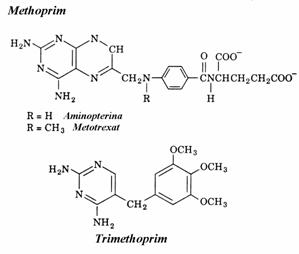
Antifolatii, antimetaboliti ai sintezei timin nu-cleotidelor, sunt analogi ai DHF care se leaga competitiv, aproape ireversibil, la DHF reduc-taza. Blocarea acestei enzime impiedica sinteza dTMP. Exemple de antifolati sunt methoprim, metotrexat, trimethoprim.
2. Catabolismul nucleotidelor pirimidinice
Sediul catabolismului pirimidinelor este ficatul. Produsii acestui catabolism sunt gaze usor solubile in apa(NH3, CO2) precum si compusi usor metabolizabili. Celulele animalelor degra-deaza nucleotidele pirimidinice pana la starea de baza (uracil, timina). Aceste transformari au loc prin reactii de defosforilare(hidroliza) sub actiu-
nea nucleotidazelor si deaminare si clivaj a legaturii N-glicozidice sub actiunea unei fosfori-laze. Nucleobazele sunt reduse in hepatocite iar dihidronucleobazele sunt deciclizate si hidroli-zate rezultand δ-Ala sau β-aminoizobutirat alaturi de NH3 si CO2. Prin urmare, spre deosebire de catabolismul purin-nucleotidelor, produsii finali ai pirimidin-nucleotidelor sunt substante usor solubile in apa. Astfel, in conditiile unei supra- productii de pirimidine nu vor apare semne clinice deoarece produsii de degradare ai acestora nu se acumuleaza ca acidul uric si uratii. Hiperproductia de PRPP determina cresterea acestor compusi. Aminoacizii rezultati sunt procesati prin succesiuni de reactii similare cu cele intalnite la degradarea aminoacizilor cu catene ramificate.
Figura 35. Catabolismul pirimidin nucleotidelor la animale. Aminoacizii rezultati prin reactii specifice sunt preluati de alte procese metabolice cum ar fi catabolizarea aminoacizilor. UMP si dTMP sunt de-gradati de aceleasi enzime.
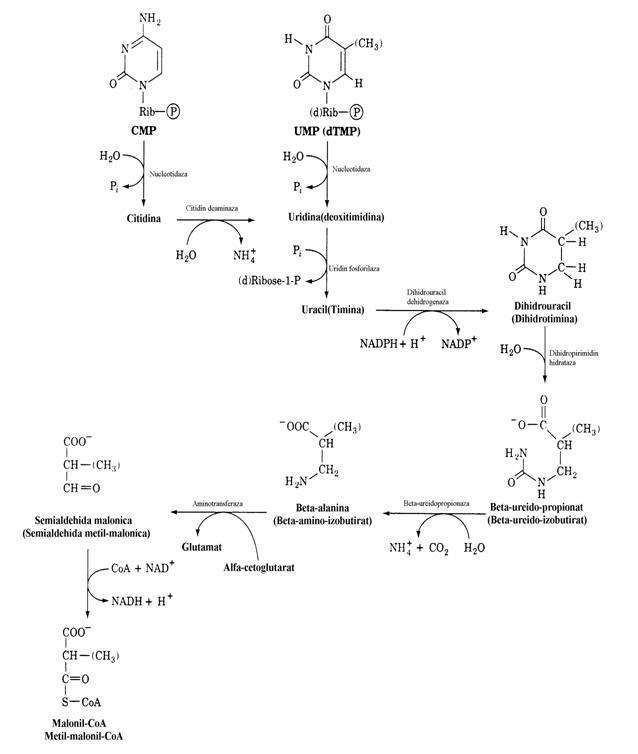
Excretia de b-amino-izobutirat creste in ira-dierea cu raze X, leucemie. Ea se explica prin faptul ca in iradierea cu raze X exista o distrugere de celule crescuta si deci distrugerea ADN din care rezulta nucleotide pirimidinice.
Biosinteza de novo a nucleotidelor pu-rinice. 1. Mecanismul chimic
Spre deosebire de pirimidin-nucleotide la care sinteza nucleobazei se realizeaza inaintea formarii legaturii N-glicozidice, la biosinteza purin-nucleotidelor construirea scheletului puri-nic se face pe restul fosfoglucidic(fig. 36, 37).
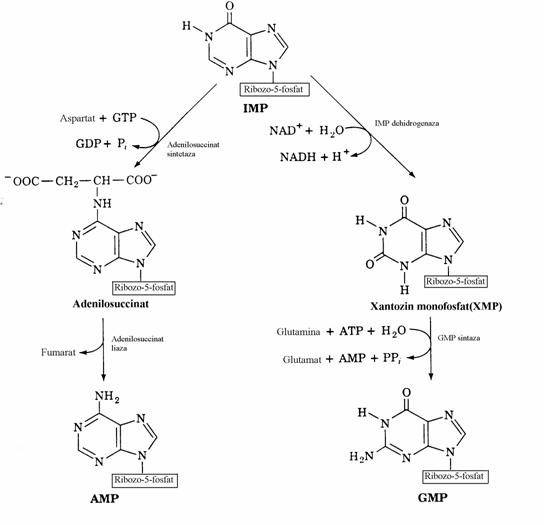
Figura 36. Biosinteza de novo a nucleotidelor monofosforice purinice pana la inozin monofosfat.
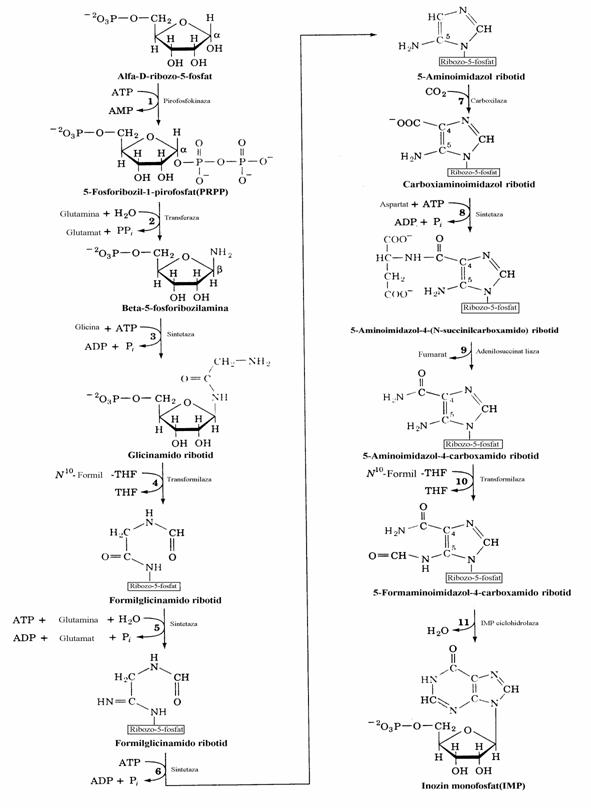
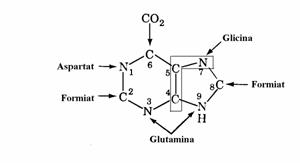
Global, nucleul purinic rezulta din contri-butia a 2 aminoacizi(Gly si Gln), a unor subuni-tati C1 activate de acidul tetrahidrofolic si a CO2, asa cum se vede mai jos.
Figura 37. Biosinteza AMP si GMP pornind de la inozin monofosfat.
2. Ciclul purin nucleotidelor
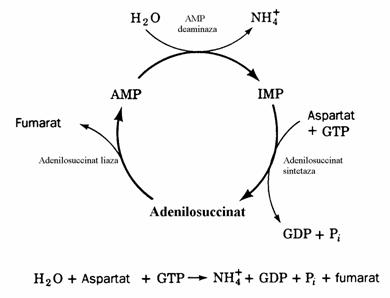
Atunci cand dezaminarea AMP sub actiu-nea AMP deaminazei, cu formare de IMP, este combinata cu sinteza AMP din IMP(fig. 36, 37) global are loc dezaminarea neoxidativa a acidului aspartic prin care resulta acidul fumaric(ne amin-tim ca dezaminarea neoxidativa a histidinei produce acid urocanic). Aceasta combinatie se numeste ciclul purin nucleotidelor(fig. 38). Acesta are un important rol in metabolismul mus-chiului scheletic. Intensificarea activitatii muscu-lare impune intensificarea ciclului citric care are loc prin anapleroza. Totusi, miocitele muschiului scheletic sunt mai sarace in enzime anaplerotice decat celulele altor tesuturi. Miocitele isi 'rein-carca' ciclul citric mai degraba cu fumaratul generat de ciclul purin nucleotidelor. Importanta ciclului purin nucleotidelor in muschi este dove-dita de observatia ca cele 3 enzime implicate in ciclul purin nucleotidelor sunt mult mai active in acest tesut decat in altele. Indivizii cu deficit inascut de AMP deaminaza obosesc usor si sufera de crampe musculare dupa efortul fizic.
Figura 38. Ciclul purin nucleotidelor. In efort fizic acest ciclu incarca ciclul citric furnizandu-i fumarat. Jos este prezentata reactia globala a ciclului.
Reglarea biosintezei nucleotidelor puri-nice
Cel mai important reglator al biosintezei "de novo" a purinelor este concentratia intrace-lulara a PRPP. Pe de alta parte viteza de sinteza a PRPP depinde de activitatea PRPP sintetazei. Activitatea PRPP sintetazei depinde de efectele alosterice ale purin si pirimidin nucleotidelor.
Figura 39. Controlul biosintezei de novo a purin-nucleotidelor. Octogoanele pline indica punctele de control. Inhibitia prin feed-back si activarea prin feed-forward sunt reprezentate prin linii intrerupte.
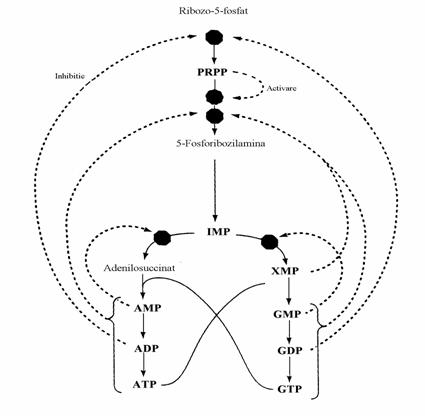
Viteza de utilizare a PRPP depinde in special de consumul lui pe caile de salvare a bazelor purinice (in mai mica masura de viteza biosintezei "de novo"). Prin urmare orice deficit enzimatic aparut pe aceste cai determina o cres-tere marcata a PRPP si deci o intensificare a biosintezei de novo. Pe de alta parte, amido-transferaza, prima enzima implicata in sinteza specifica a purinelor, este obiectul a doua efecte opuse:
- efectul inhibitor al IMP si nucleotidelor finale
- efectul activator al PRPP ca substrat, competitiv cu cel inhibitor al IMP.
Schema arata ca in afara reglarii procesului global de biosinteza este reglat si echilibrul dintre AMP si GMP.
4. Medicamente inhibitoare ale sintezei purin nucleotidelor
6-mercaptopurina si 6-tioguanina sunt convertite in ribonucleotidele de catre hipoxan-tin-guanin fosforibozil transferaza (HGPRT), enzima de salvare a nucleobazelor indicate in denumire. 6-tio-IMP rezultat inhiba conversia IMP in AMP, respectiv 6-tio-GMP inhiba con-versia IMP in GMP. In plus, cele doua ribonu-cleotide tiolice inhiba prin feed-back negativ etapa cheie a sintezei de novo a purin nucleo-tidelor, reactia PRPP cu glutamina.
5. 'Salvarea' bazelor purinice - cale de sinteza a nucleotidelor purinice
Mamiferele si multe vertebrate inferioare sunt capabile sa sintetizeze "de novo" nucleotide purinice si pirimidinice. Prin urmare supravie-tuirea lor nu depinde de prezenta acestor nucleo-tide in alimentatie. Totusi, dieta acestor organis-me contine nucleoproteide (complexe formate din acizi nucleici si proteine). Enzimele proteolitice ale tractului intestinal elibereaza acizii nucleici din nucleoproteine. Sucul pancreatic contine nucleaze care degradeaza acizii nucleici in nu-cleotidele componente: ribonucleazele actionea-za asupra ARN si deoxiribonucleazele actio-neaza asupra ADN.
Nucleotidazele hidrolizeaza mononucleotidele in nucleozide si H3PO4. Aceste nucleozide libere pot fi absorbite in intestin sau degradate pana la sta-rea de baze libere sub actiunea fosforilazei intes-tinale:
Adenozina+ATP Adenina+Rib-1-P
Nucleazele, nucleotidazele si fosforilazele in-tracelulare au aceleasi functii cu ale celor intestinale.
Bazele purinice (spre deosebire de bazele pirimi-dinice), pot servi la resinteza nucleotidelor purinice pe o cale "de salvare" care este mult mai simpla si cu un cost energetic mult mai mic decat calea biosintezei "de novo". Exista doua "enzime de slavare" a bazelor purinice: (i) adenin fosfo-ribozil transferaza (APRT). (ii) guanin-hipoxan-tin fosforibozil transferaza (GHPRT). Schema reactiilor catalizate de aceste enzime este prezen-tata in figura 40.
Figura 40. Biosinteza salvatorie a purin-nucleotide-lor.
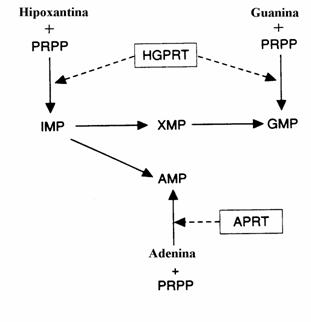
Enzima adenozin kinaza catalizeaza sinteza AMP si dAMP prin 'salvarea' adenozinei si deoxiadenozinei.
In functie de specia organismului puri-nele sunt degradate diferit, pana la acid uric, sau pana la alantoina sau uree si acid glioxilic. Omul degradeaza purinele pana la acid uric.
4.1. Mecanismul chimic
Calea urmata pentru conversia purinelor in acid uric implica reactii de dezaminare, fosfo-roliza si oxidare(fig. 41).
Figura 41. Principalele cai de catabolizare a purin nucleotidelor la mamifere. Produsul final este acidul uric.
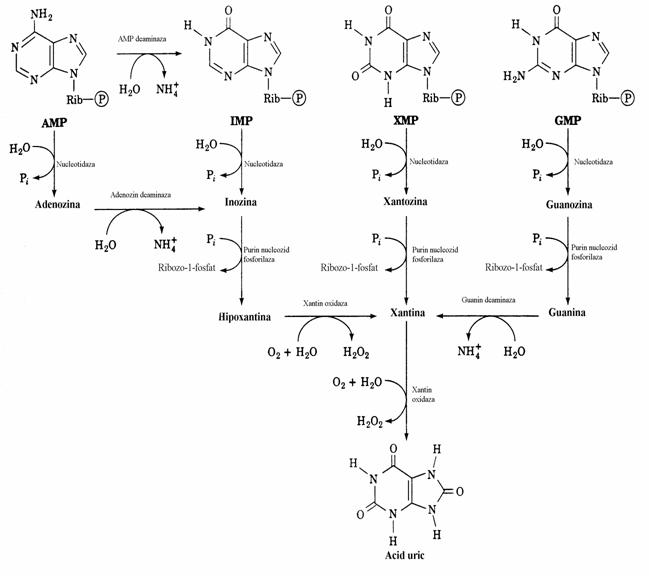
Acele organisme, pasari, reptile, la care principa-la forma de eliminare a azotului aminic este acidul uric se numesc uricotelice. La acestea, biosinteza purin nucleotidelor are o mai mare in-tensitate decat la ureotelice avand in vedere ca, prin intermediul lor, azotul din: Asp, Gly, Glu-NH2 este excretat sub forma de acid uric. Este si un mijloc de conservare a apei datorita solubili-tatii mici a uratului.
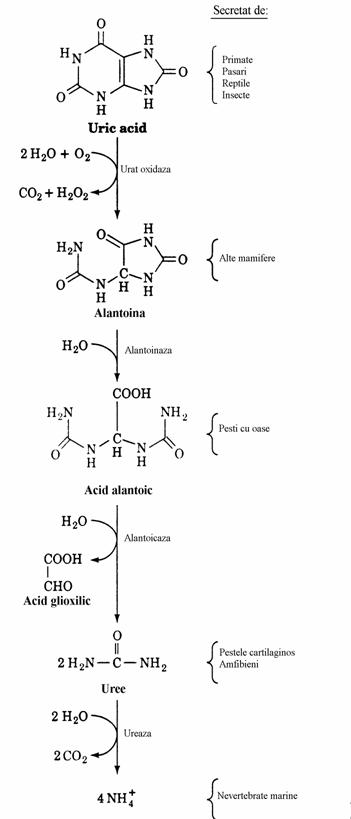
La oameni se pare ca acidul uric joaca un rol care il depaseste pe cel de produs final. El poate servi ca antioxidant prin transformarea neenzimatica in alantoina. Alantoina are proprietati asemana-toare acidului ascorbic. Alte mamifere, inferioare primatelor, secreta alantoina ca produs final de degradare a nucleotidelor purinice datorita existentei in celulele lor a uricazei (urat oxida-zei), enzima care catalizeaza formarea alantoinei.
Probabil ca la un anumit nivel in scara filogenetica, au existat la stamosii primatelor atat gulonolacton oxidaza cat si uricaza. Pierderea gulonolacton oxidazei si deci incapacitatea de sinteza a acidului ascorbic, a fost compensata ulterior prin pierderea uricazei, deci conservarea acidului uric ca reducator. La unii pesti alantoina este degradata pana la uree si acid glioxilic.
Figura 42. Conversia acidului uric in amoniac. Procesul este intrerupt in diferite stadii la speciile indicate in acolade.
4.2. Tulburari ale metabolismului purinelor. Hiperuricemia
Structura acidului uric depinde de pH. In figura 43 sunt prezentate formele tautomere ale acidului uric si echilibrul de ionizare a formei enol.
Figura 4 Acidul uric
in diferite forme tautomere. 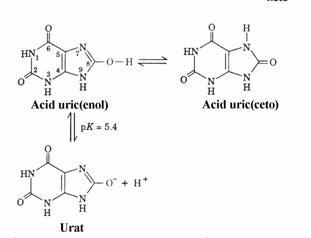
In conditii fiziologice exista un amestec urat/acid uric, predominand uratul de sodiu. Atunci cand concentratia ionilor acestuia depa-seste produsul de solubilitate a uratului de sodiu, serul devine suprasaturat si in el pot precipita cristale de urat. In ser la 37 C, solubilitatea uratului este 7 mg%. Cristalele se depoziteaza in special in incheieturi. In urina solubilitatea aci-dului uric este mai mare decat in ser, limita de solubilitate fiind 15 mg%. Acidifierea urinei primare are loc in tubul distal si ductul colector ale nefronului. Prin acidifiere raportul urat/acid uric scade si totodata scade si solubilitatea siste-mului urat deoarece acidul uric este de 17 ori mai putin solubil decat uratul de sodiu. Precipi-tarea cristalelor de acid uric (piatra la rinichi) poate fi prevenita prin alcalinizarea urinei. Boala, numita artrita hiperuricemica (guta, podagra) este cauzata de formarea cristalelor de urat de sodiu in incheieturi si rinichi.
Una din cauzele metabolice ale bolii este lipsa unui control alosteric a PRPP-sintetazei. O alta este lipsa activitatii guanin-hipoxantin fosforibozil transferazei (GHPRT), enzima de salvare a bazelor purinice (guaninei). Ambele cauze determina cresterea concentratiei de PRPP si supraproductia de acid uric pe calea de novo. Aceste cristale precipita atunci cand nivelul seric al uratului depaseste limita sa de solubilitate. Cristalele aciforme de urat de sodiu sunt anizo-trope din punct de vedere optic prezentand bire-fringenta negativa, ceea ce permite sa fie deosebite la microscopicopul cu polarizare de alte cristale. Daca leucocitele polimorfonucleare din fluidul sinovial contin cristale de urat de sodiu diagnosticul este guta. Inflamatia si eroda-rea incheieturilor apar atunci cand leucocitele incorporeaza cristalele de acid uric care deter-mina ruptura celuleor si eliberarea enzimelor lizozomiale. Aceste cristale, daca sunt prezente in tractul urinar, altereaza functia renala. Guta se trateaza prin dieta si medicamente. Alimentele bogate in acizii nucleici ca ficatul sunt excluse din dieta, la fel cafeaua si ceaiul care contin cafe-ina si teobromina.
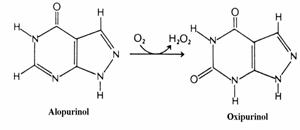
Ca medicament se foloseste alopurino-lul, analog al hipoxantinei. Xantin oxidaza catali-zeaza oxidarea alopurinolului cu formare de oxi-purinol(fig. 44). Acesta din urma se asociaza strans la centrul activ al enzimei si o impiedica sa oxideze xantina sau hipoxantina pentru a forma acid uric. Acesta este un exemplu tipic de inhibi-tie prin "sinucidere"(suicide inhibition). Pentru tratamentul gutei in timpul puseului acut se utilizeaza colchicina, un medicament(alcaloid) antiinflamator care inhiba miscarea leucocitelor prin inhibarea microtubulilor.
Figura 44. Oxidarea alopurinolului.
Sindromul Lesch-Nyhan are la baza lipsa aproape totala a activitatii GHPRT, defect inascut. Din aceasta cauza guanina si hipoxantina nu sunt 'salvate' ceea ce determina scaderea nivelelor GMP si IMP si cresterea nivelului PRPP. In consecinta este accelerata sinteza de novo a purinelor si a acidului uric. Copiii cu aceasta boala incep sa se manifeste la 2 ani prin a-si musca buzele si degetele. Tendinta la auto-mutilare este atat de mare incat este necesara protejarea acestor pacienti prin invelirea mainilor in tifon. Ei sunt agresivi si fata de ceilalti. Sunt deficienti mintal, au miscari necoordonate si fac hiperuricemie si piatra la rinichi foarte timpuriu. Tratamentul cu alopurinol reduce formarea acidului uric insa nu amelioreaza simptomele neurologice. In ciuda faptului ca celulele acestor pacienti au putut fi "vindecate" in vitro prin inginerie genetica, foarte putin s-a putut face pentru insanatosirea in situ a lor.
Deficienta de adenozin deaminaza de-termina nivele crescute ale adenozinei si deoxi-adenozinei care sunt convertite prin 'salvare' in nucleotidele corespunzatoare in leucocite. Nive-lurile mari ale dATP inhiba ribonucleotid reduc-tazele adica reduce productia de deoxinucleotide si deci inhiba sinteza ADN. Din aceasta cauza leucocitele nu pot prolifera (imunodeficienta). Alterarea severa a functiunilor limfocitelor T si B determina aparitia la varsta de 6 luni a unor infectii si tulburari de crestere. Decesul poate surveni la varsta de 18 luni. Tratamentul consta in transplantul de maduva osoasa.
Copyright © 2024 - Toate drepturile rezervate