 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
Proprietatile unui aliaj sunt determinate nu numai de compozitia sa chimica ci mai ales de constitutia fizico - chimica, adica de natura si proportia fazelor care alcatuiesc aliajul. Limitele de stabilitate ale fazelor intr-un sistem de aliaje sunt reprezentate grafic in functie de temperatura si compozitie prin diagrama de echilibru fazic a sistemului respectiv.
Pentru reprezentarea diagramei de echilibru fazic sunt necesare un numar de axe de coordonate egal cu numarul n de componenti ai sistemului si anume 1 axa pentru temperatura si n -1 axa pentru valorile independente ale concentratiei componentilor. Rezulta ca diagramele de echilibru fazic ale sistemelor binare (n = 2) se reprezinta grafic in plan; diagramele de echilibru fazic ale sistemelor ternare (n = 3) se construiesc in spatiu pe modele; pentru sisteme complexe (n > 3) nu se pot face decat reprezentari simplificate ale diagramelor de echilibru fazic.
Concentratia componentilor in diagrama de echilibru fazic este exprimata in procente de greutate (% W) sau in procente atomice (% at). Transformarea procentelor de greutate in procente atomice se face pe baza greutatilor atomice A, utilizand relatia:

Domeniile de stabilitate a fazelor pe diagrama de echilibru sunt separate prin linii de transformare fazica (in diagramele binare) si prin suprafete de transformare fazica (in diagramele sistemelor multicomponente).
Construirea diagramei de echilibru fazic consta in stabilirea tuturor liniilor de transformare din sistemul dat, cu precizarea pozitiilor acestora in coordonate temperatura - compozitie. Limitele de transformare fazica se refera atat la transformarea la solidificare cat si la transformarile in stare solida determinate de transformari alotropice, variatii de solubilitate si formarea compusilor intermetalici.
Stabilirea liniilor de transformare fazica se executa experimental prin urmarirea transformarilor la incalzire - racire in conditii de echilibru. Temperaturile transformarilor sunt puse in evidenta prin inflexiuni pe curbele de variatie cu temperatura a proprietatilor aliajelor prin diverse metode ca: analiza termica (metoda curbelor de racire, analiza termodiferentiala), analiza dilatotermica, analiza magnetica, etc.
Solubilitatea completa sau nelimitata a componentilor sistemului in stare lichida si solida se realizeaza cand toti factorii de solubilitate (geometric, electrochimic, de concentratie electronica) sunt favorabili si componentii sunt izomorfi (au aceeasi retea cristalina). In acest caz componentii formeaza la diverse compozitii o serie continua de solutii izomorfe. Astfel de diagrame prezinta sistemele binare: Cu - Ni, Ag - Pb, Co - Mo, Ag - Au, Pt - Cu, Mo - Ti, Mo - W, Ti - Nb, Ti - W, etc.
Fie o diagrama binara alcatuita din doi componenti A si B complet solubili in stare lichida si solida (fig. 3.5) si aliajul c0 care se raceste incet.
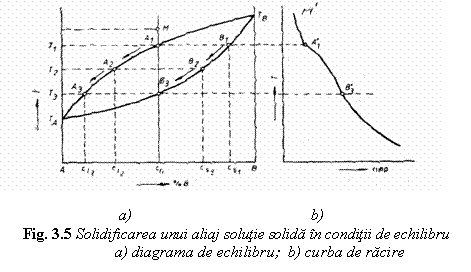
Starea aliajului se reprezinta printr-un punct M situat la intersectia dintre verticala de compozitie si orizontala de temperatura; deoarece aliajul este topit punctul M se afla deasupra curbei lichidus. Prin racire temperatura aliajului va scadea, deci M va cobori pe verticala de compozitie. Deoarece pana in A1 in aliaj nu are loc nici o transformare, curba de racire va descrie segmentul M'A'1 de forma exponentiala. In intervalul de temperatura MA1 variatia sistemului este egala cu 2, conform legii fazelor, cele doua grade de libertate a sistemului fiind temperatura si concentratia.
In punctul A1 care se gaseste la intersectia dintre verticala compozitiei si curba lichidus, incepe formarea primelor cristale de solutie solida. Compozitia acestor cristale este data de intersectia dintre orizontala de temperatura T1 care trece prin A1 si curba solidus; notand aceasta intersectie cu B1 compozitia cristalelor este cs1. In punctul A1 varianta sistemului este egala cu 1, fiind prezente doua faze: topitura si cristalele de solutie solida (v =n + 2 - f = 1 + 2 - 2 = 1).
Ca urmare solidificarea are loc intr-un interval de temperatura; in punctul A1, in urma pierderii caldurii latente de solidificare, curba de racire incepe sa se abata de forma exponentiala . Pentru ca solidificarea sa aiba loc temperatura trebuie sa scada continuu, la fiecare temperatura stabilindu-se un echilibru, atat lichidul cat si solidul avand compozitii omogene. De exemplu, la temperatura T2 se afla in echilibru lichidul A2 de compozitie cl2 si solidul B2 de compozitie cs2. Solidul format la temperaturi mai mari decat T2 si-a schimbat, prin difuzie intre lichid si solid, compozitia, ajungand la concentratia cs2. Rezulta in acest fel ca in cursul solidificarii compozitia lichidului s-a deplasat pe curba lichidus de la A1 spre A2, iar compozitia solidului pe curba solidus de la B1 spre B2, solidificarea se termina la temperatura T3 care corespunde intersectiei dintre verticala de compozitie si curba solidus; ultimele cantitati de lichid care se solidifica au compozitia cl3, iar solidul compozitia initiala c0 a lichidului. La temperatura T3 curba de racire isi reia aspectul exponential.
Structura care se obtine ca rezultat al solidificarii in conditii de echilibru este o solutie solida omogena cu graunti omogeni, cu contur geometric neregulat (fig. 3.6).
In conditii practice de solidificare nu se poate realiza starea de echilibru pentru omogenizarea prin difuzie a compozitiei si deci cristalele de solutie solida vor fi la inceputul solidificarii mai bogate in componentul B care are temperatura de topire mai ridicata.
Structura cristalului de solidificare are un aspect dendritic (fig. 3.7) care se poate corecta prin tratament termic de recoacere de omogenizare.

Din aceasta categorie de diagrame fac parte trei grupe de aliaje:
sisteme cu transformare eutectica;
sisteme cu transformare peritectica;
sistem fara transformare eutectica sau peritectica.
Dintre sistemele de aliaje care apartin acestei grupe se
nominalizeaza sistemele: Ag -Cu; Al- Si; Cr - Ni; Pt - Cr; etc. In figura
3.8. se prezinta diagrama de echilibru fazic pentru asemenea aliaje, 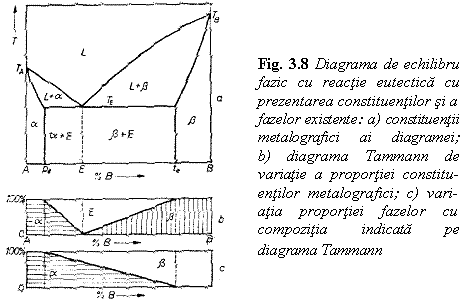
unde compozitia E
reprezinta compozitia eutectica avand semnificatia
lichidului cu cea mai joasa temperatura de solidificare (respectiv de
topire) din sistem. Lichidul eutectic solidifica la temperatura
eutectica TE conform reactiei zero variante:
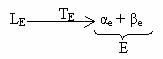
In cursul cristalizarii eutectice temperatura ramane constanta, sistemul neavand nici un grad de libertate; la sfarsitul cristalizarii faza lichida dispare si sistemul isi dobandeste un grad de libertate. Morfologia constituentului eutectic poate fi lamelara (lamele alternante ale fazelor a si b), in baghete, globulara sau o morfologie neregulata. Proprietatile eutecticului reprezinta media proprietatilor fazelor constitutive; proprietatile mecanice depind de finetea cristalelor fazelor.
In fig 3.8.a. sunt indicati constituentii metalografici ai aliajelor solidificate din acest sistem de aliaje. Aliajele cu compozitia din domeniul A - pe si te - B sunt monofazice, respectiv solutii solide a si b. Aliajele din domeniul pe - E sunt constituite din eutectic si cristale a proeutectice - denumite hipoeutectice. Aliajele cu compozitia din domeniul E - te sunt constituite din eutectic si cristale b proeutectice - denumite hipereutectice.
 Proportia constituentilor in diverse aliaje din sistem, la
temperatura ambianta, este redata in fig. 3.8.b, prin diagrama
Tammann; cantitatile constituentilor variaza liniar cu
compozitia conform regulii segmentelor inverse. In fig.3.8.c se
prezinta intr-o diagrama Tammann proportia fazelor in aliajele sistemului la temperatura ambianta; se constata in aliajele bifazice
(in gama de compozitii pe - te) ca fazele se
prezinta partial sub forma libera de cristale proeutectice
si partial sunt incluse in structura eutecticului.
Proportia constituentilor in diverse aliaje din sistem, la
temperatura ambianta, este redata in fig. 3.8.b, prin diagrama
Tammann; cantitatile constituentilor variaza liniar cu
compozitia conform regulii segmentelor inverse. In fig.3.8.c se
prezinta intr-o diagrama Tammann proportia fazelor in aliajele sistemului la temperatura ambianta; se constata in aliajele bifazice
(in gama de compozitii pe - te) ca fazele se
prezinta partial sub forma libera de cristale proeutectice
si partial sunt incluse in structura eutecticului.
Diagramele de echilibru fazic ale unui sistem ce prezinta transformare eutectica pot lua aspectele prezentate mai jos:
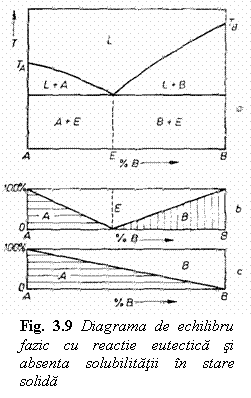
Diagrama de echilibru fazic cu reactie eutectica cu lipsa totala a solubilitatii componentilor in stare solida (fig. 3.9); toate aliajele sistemului sunt bifazice si contin eutectic in structura alaturi de componentii puri A si B;
Diagrama de echilibru fazic cu transformare eutectica cu variatie de solubilitate in stare solida. In majoritatea sistemelor de aliaje din aceasta categorie, la racire se constata o scadere a solubilitatii in solutiile solide din sistem. Fenomenul se explica prin scaderea entropiei la temperaturi joase. In aceste conditii linia de delimitare a domeniului solutiei solide nu mai este reprezentata de o verticala pe diagrama de echilibru fazic, ci printr-o curba numita curba solvus; care exprima variatia cu temperatura a limitei de solubilitate in solutia solida.
In fig. 3. 10. Se prezinta aspectul diagramei cu variatia solubilitatii in stare solida, asa cum este cazul sistemului Ag - Cu.
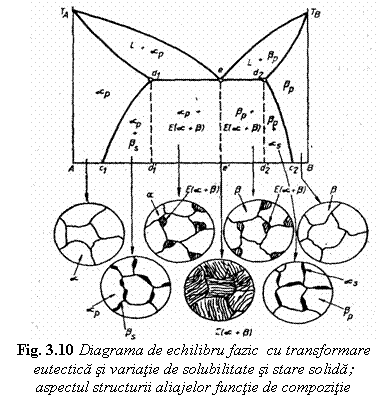
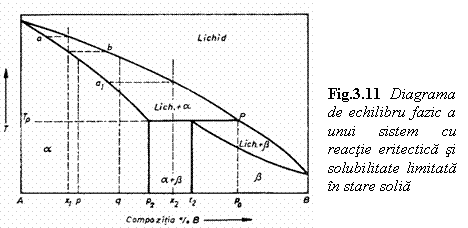
Diagrama de echilibru fazic a unui sistem binar cu solubilitate limitata in stare solida si reactie peritectica este prezentata in fig. 3.11. In aceasta diagrama p0 reprezinta compozitia peritectica avand semnificatia lichidului care se consuma prin reactie peritectica zero varianta si care se produce la temperatura constanta. Din acest sistem fac parte aliajele: Co-Os, Co-Re, In-Ti etc.
Transformarea peritectica este descrisa de reactia:
![]()
Faza β rezultata prin reactia peritectica apare sub forma unei pelicule la limita intre fazele existente anterior (lichid + α); aceasta pelicula β se ingroasa pe masura ce reactia progreseaza, formand un perete ce desparte fazele reactante, de unde rezulta si denumirea reactiei. Transformarea peritectica este o reactie lenta intrucat implica difuzia prin peretele de faza solida β.
In numeroase sisteme de aliaje apar, in anumite domenii de compozitii, una sau mai multe faze intermediare AB cu structura cristalina diferita fata de solutiile solide terminale. In diagrama de echilibru fazic al acestui sistem (fig.3.12) se constata prezenta a doua reactii eutectice:

Daca componentii AB sunt total solubili in stare lichida si partial solubili in stare solida se formeaza un compus AB cu topire congruenta, cu variatii de solubilitate in stare solida.

Diagramele de echilibru fazic reprezinta baza studierii rationale a aliajelor. Fiind data compozitia unui aliaj, diagrama de echilibru fazic indica, pentru orice temperatura, constitutia fizico - chimica a aliajului, adica natura fazelor care il alcatuiesc, compozitia acestor faze si proportia lor. In cazul cand diagrama de echilibru fazic a sistemului contine amestecuri mecanice de cristale si faze diferite (eutectice si eutectoide) notiunile de faza si constituent devin distincte. In acest caz pozitia compozitiei aliajului pe diagrama de echilibru fazic a sistemului permite determinarea naturii si proportiei constituentilor aliajului. Constitutia aliajului stabilita pe baza diagramei de echilibru permite o serie de deductii privind proprietatile acestuia. In privinta proprietatilor mecanice diagramele de echilibru dau numeroase indicatii:
a) in cazul aliajelor alcatuite dintr-un singur constituent:
metalele pure prezinta rezistenta la tractiune relativ scazuta, dar o plasticitate ridicata;
compusii definiti si solutiile solide corespunzatoare unui maxim pe curba lichidus sunt caracterizati prin duritate si fragilitate ridicate;
eutecticul si eutectoidul au proprietati speciale dependente de proprietatile fazelor constitutive cat si de morfologia si finetea amestecului;
b) in cazul aliajelor alcatuite din doi constituenti:
proprietatile aliajului sunt reprezentate prin media ponderata a proprietatilor constituentilor;
diagramele de echilibru fazic indica temperaturile la care se produc modificarile de constitutie sau transformarile de faza care stau la baza tratamentelor termice; Proprietatile fizico - mecanice depind de compozitia chimica in acelasi mod ca si energia libera: in timp ce in domeniile omogene ale diagramelor de echilibru conductibilitatea electrica si termica, alungirea si gatuirea variaza cu compozitia dupa o curba convexa, iar rezistivitatea electrica, duritatea, limita de curgere, etc. dupa o curba concava in domeniile eterogene ale diagramelor de echilibru, aceste proprietati variaza cu compozitia liniar. Legile de variatie ale proprietatilor fizico - chimice - mecanice cu compozitia sunt cunoscute sub numele de legile lui Kurnakov, iar pentru rezistivitatea electrica sunt prezentate in figura 3.13.

Fig. 3.13 Variatia rezistivitatii electrice cu compozitia:
a) sistem de aliaje cu componenti complet solubili in stare lichida si solida; b) sistem de aliaje cu componenti total insolubili si in stare solida; c) sistem de aliaje cu componenti partial solubili in stare solida; d) sis-teme de aliaje cu compusi intermetalici
Sistemele de aliaje prezentate se regasesc ca utilizare si in domeniul biomaterialelor sub forma de proteze ortopedice si diverse dispozitive medicale.
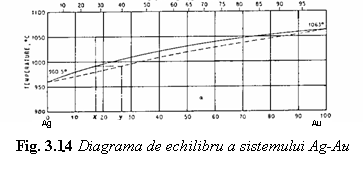
Sisteme de aliaje binare cu solubilitate totala a componentilor in stare lichida si solida sunt reprezentate de catre aliajele Ag - Au si Cr - Mo (fig. 3.14 si 3.15).
Diagrama Ag - Au (fig.3.14) pune in evidenta un domeniu ingust intre curbele solidus si lichidus, ceea ce inseamna ca aceste aliaje au fluiditate buna in stare topita; ele se utilizeaza mai ales in tehnica dentara.
In figura 3.15. este prezentata
diagrama binara Cr - Mo de asemenea cu solubilitatea totala a
componentilor in stare lichida si solida .
![]()
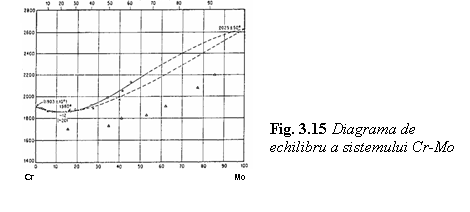
Diagrama deriva din sistemul ternar de aliaje Co - Cr - Mo care a castigat mare utilizare in domeniile chirurgiei ortopedice si al implantologiei dentare. Sunt puse in evidenta cele doua verticale de temperatura ale metalelor pure (Cr, Mo) respectiv 19030 C pentru Cr si 20250 C pentru Mo, precum si domeniul foarte ingust al intervalului de topire pentru aliajele binare care contin pana la 20% Mo. Acest sistem de aliaje se caracterizeaza prin foarte bune proprietati de turnare determinate de domeniul ingust solidus - lichidus.
Sistemul de aliaje binare cu transformare eutectica si solubilitate partiala in stare solida este reprezentat aici de diagrama de echilibru Co - Mo (fig. 3.16).
La temperatura de 13400C se formeaza din cele doua metale lichide eutecticul solid care contine 37% Mo. In diagrama binara se pun in evidenta doi. compusi intermetalici:
Fig. 3.16 Diagrama
de echilibru
a sistemului binar Co-Mo.
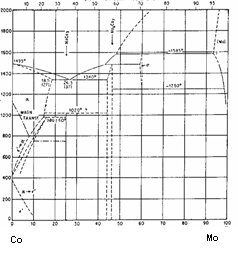
compusul Mo6Co7 format direct din lichid prin reactie peritectica la 1585 0C care este stabil pana la temperatura camerei, precum si compusul MoCo3 format prin reactie peritectoida la 1020 0C din fazele de solutie solida. Coa si compusul Mo6Co7, stabile de asemenea pana la temperatura ambianta.
Sistemul de aliaje binare cu transformare peritectica si formare de compusi intermetalici este reprezentat de diagrama Ti - Al. In acest sistem de aliaje se constata formarea a doi compusi intermetalici prin reactie peritectica (fig. 3.17).
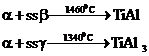

Ambii compusi au stabilitate in stare solida pana la temperatura ambianta. Aliajele dinspre titan din domeniul s.s.α se
utilizeaza ca implanturi ortopedice pana la o concentratie de cca. 6% Al.
Diagrama de echilibru a aliajelor Fe -C prezinta interes practic pentru gama de oteluri inoxidabile utilizate ca biomateriale in ortopedie si chirurgie. Diagrama de echilibru este prezentata in fig. 3.18 de unde rezulta ca ea contine mai multe transformari, faze si constituenti dupa cum urmeaza:
trei solutii solide: a - ferita, g - austenita si d stabila numai la temperaturi inalte cuprinse intre 14000C si 15360C - temperatura de topire a fierului pur;
transformare eutectica - pe linia ECF, eutecticul se numeste ledeburita (in domeniul fontelor);
transformare eutectoida - pe linia PSK; eutectoidul se numeste perlita;
un compus definit cementita corespunzator verticalei DL;
linia lichidus este ABCD, iar linia solidus este AHJECF.
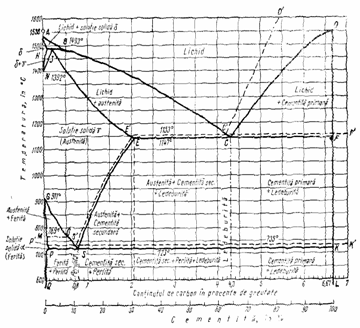
Fig.3.18 Diagrama de echilibru termic Fe-C
Liniile continui reprezinta diagrama metastabila Fe-cementita. Liniile disconti-nui reprezinta diagrama stabila Fe-C
Diagrama de echilibru Fe - C simplificata se prezinta in figura 3.19 fiind caracterizata prin urmatoarele domenii si zone cu fazele si constituentii specifici otelurilor:
domeniul I, in lungul liniei AC, in care se separa solutia solida de carbon in fier g denumita austenita. Acest domeniu este alcatuit din doua faze: lichid si austenita;
domeniul II cuprinde o singura faza austenita cu compozitia chimica, variabila cu temperatura, intre 0 si 2,11%C;
domeniul III cuprinde doua faze: austenita si cementita secundara (care se separa in stare solida de-a lungul liniei ES
domeniul IV delimitat de linia GS ca urmare a transformarii alotropice a fierului g in fier a, din austenita se separa ferita cu continut foarte redus de carbon.
eutectoidul corespunzator punctului S (0,8%C) se numeste perlita, acesta rezulta in urma descompunerii austenitei conform reactiei:
![]() austenita ferita + cementita
austenita ferita + cementita
perlita
domeniul V situat sub linia PSK in care se afla in echilibru doua faze: ferita si perlita. Zonele acestui domeniu din stanga verticalei eutectoide numita zona otelurilor hipoeutectoide (C < 0,80%) avand drept constituenti perlita si ferita; in dreapta verticalei eutectoide se afla in zona otelurilor hipereutectoide (C = 0,8 - 2,11%) avand constituenti sub forma de cementita secundara si perlita.
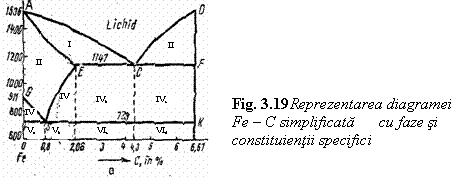
Diagrama de echilibru, asa cum a fost prezentata, nu corespunde starii reale cand aliajele sunt in afara echilibrului si nu furnizeaza date privind structura aliajelor. Notarea punctelor si liniilor de transformare corespunzatoare otelurilor se prezinta in fig.3.20 si au urmatoarele semnificatii:
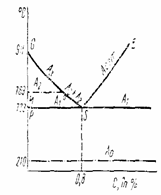
Fig. 3.20 Punctele si liniile de transformare din domeniul otelurilor
A0 - transformarea magnetica a cementitei (2100C);
A1 - transformarea perlitica (7230C);
A2 - transformarea magnetica a feritei (7690C);
A3 - transformarea austenita - ferita (linia G - S);
Acem - separarea cementitei secundare (linia SE).
In sistemul de aliaje Fe - C exista o diferenta intre temperatura punctelor de transformare determinate la incalzire si racire, deci notatiile se vor completa cu literele c respectiv r ca de exemplu Ac1, Arcem, Ar3. etc.
Copyright © 2025 - Toate drepturile rezervate