 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
Metalul este definit ca fiind un element chimic cu luciu caracteristic, opac, bun conductor de caldura si electricitate , maleabil si ductil. Atomii metalelor pierd usor electroni, formand ioni pozitivi, iar oxizii si hidroxizii lor sunt bazici.
Proprietatea specifica starii metalice este coeficientul de temperatura al rezistivitatii electrice, care este pozitiv, adica rezistivitatea electrica creste cu temperatura, spre deosebire de nemetale la care acest coeficient este negativ.
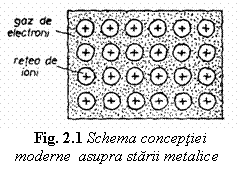
Teoria moderna a starii metalice porneste de la ideea ca distributia electronilor este diferita de cea a atomilor liberi, la care electroni sunt repartizati pe nivele si subnivele de energie, pe orbite bine determinate. La metalele solide numai nivelele energetice mai apropiate de nucleu sunt distincte, in timp ce nivelele si subnivelele exterioare se contopesc in benzi energetice care contin nivele cu energii foarte apropiate. Aceste nivele energetice nu apartin atomilor individuali ci intregului agregat atomic. In acest fel, electronii stratului exterior - electroni de valenta - apartin intregului ansamblu atomic formand un gaz sau nor electronic, in care sunt scufundati ionii pozitivi (atomii fara electroni de valenta), asa cum se constata in fig. 1.
In esenta, teoria electronica a metalelor considera materialul metalic (metal sau aliaj) ca fiind constituit din ioni pozitivi printre care circula electronii de valenta sub forma unui gaz de electroni liberi.
 Formarea in metale si aliaje a unor
legaturi interatomice metalice,
bazate pe existenta gazului de electroni liberi, este o consecinta a
structurii electronice a atomilor metalici, care se ionizeaza usor
eliberand electroni exteriori slab legati, aflati de regula in
substraturile cuantice - s. Caracterul nesaturat al
legaturii interatomice din metale conduce la o densitate a electronilor
intre atomi mult mai scazuta decat cea permisa de principiul
excluderii a lui Pauli. Aceasta permite electronilor de valenta din metale
sa se deplaseze aproape liber de la
un punct la altul, fara o crestere semnificativa a energiei
lor, ceea ce explica valorile mari ale conductibilitatii
electrice si termice specifice metalelor. Pe de alta parte densitatea
mai redusa a sarcinii electrice negative in legatura metalica,
face ca aceasta legatura sa fie nedirectionata si slaba, ceea ce da
posibilitatea cristalelor metalice sa se deformeze fara rupere (deformare plastica).
Legatura interatomica este prezenta nu numai in metale, ci
si in cristalele de solutie solida cu solvent metalic care
alcatuiesc majoritatea sistemelor de aliaje, proprietate care asigura
aliajelor caracteristici tipic metalice.
Formarea in metale si aliaje a unor
legaturi interatomice metalice,
bazate pe existenta gazului de electroni liberi, este o consecinta a
structurii electronice a atomilor metalici, care se ionizeaza usor
eliberand electroni exteriori slab legati, aflati de regula in
substraturile cuantice - s. Caracterul nesaturat al
legaturii interatomice din metale conduce la o densitate a electronilor
intre atomi mult mai scazuta decat cea permisa de principiul
excluderii a lui Pauli. Aceasta permite electronilor de valenta din metale
sa se deplaseze aproape liber de la
un punct la altul, fara o crestere semnificativa a energiei
lor, ceea ce explica valorile mari ale conductibilitatii
electrice si termice specifice metalelor. Pe de alta parte densitatea
mai redusa a sarcinii electrice negative in legatura metalica,
face ca aceasta legatura sa fie nedirectionata si slaba, ceea ce da
posibilitatea cristalelor metalice sa se deformeze fara rupere (deformare plastica).
Legatura interatomica este prezenta nu numai in metale, ci
si in cristalele de solutie solida cu solvent metalic care
alcatuiesc majoritatea sistemelor de aliaje, proprietate care asigura
aliajelor caracteristici tipic metalice.
Coeziunea cristalelor si proprietatile derivate din ea (elasticitate, dilatare termica, punct de topire) sunt asigurate de fortele de legatura interatomica, care pot fi de atractie sau de respingere dintre atomi, asa cum rezulta din figura
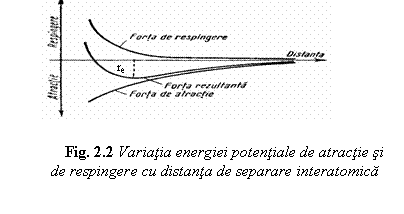
La apropierea atomilor, intre ei apar forte de respingere daca spinii electronilor sunt paraleli, sau forte de atractie daca spinii sunt antiparaleli. In acest din urma caz energia potentiala are un minim la distanta de separare de echilibru re.
Din graficul prezentat in figura 2 se constata ca ambele forte cresc odata cu micsorarea distantei dintre atomi. Totusi exista o diferenta intre modul de variatie al celor doua forte cu distanta, diferenta concretizata prin valori mai mari ale fortei de respingere la distante mici si valori mai mari ale fortei de atractie la distante mai mari. Datorita fortei rezultante atomii vor ocupa unii fata de altii pozitii bine determinate.
In acest fel fiecare atom este atras de catre toti atomii imediat vecini prin intermediul electronilor liberi care circula printre ei. Rezulta prin urmare, pentru fiecare atom, o tendinta de a se inconjura de un numar cat mai mare de atomi vecini. Se ajunge astfel la o aranjare ordonata a atomilor in spatiu, cu formarea unor figuri geometrice spatiale, numite retele cristaline.
Energia de coeziune Ec a
cristalului metalic, dedusa din modelul Wigner - Seitz, are expresia:
![]()
in care:
3/5 E0 = energia cinetica medie a electronilor liberi
V0 = energia potentiala a electronului in campul ionului pozitiv
V1 = primul potential de ionizare
Energia de coeziune se masoara experimental prin caldura latenta de sublimare, adica de trecere a metalului din stare solida in stare gazoasa (tabelul 1).
Energia DE corespunzatoare distantei interatomice de echilibru re, (figura 2), reprezinta in cazul cristalelor metalice, lucrul mecanic necesar pentru a transforma metalul intr-un gaz de ioni pozitivi.
Energia de coeziune poate fi calculata si cu ajutorul relatiei empirice: Ec ≈ 0,025 Tev , unde Tev este temperatura de evaporare a metalului in grade Kelvin.
Energia de coeziune, caracterizand stabilitatea corpurilor cristaline, poate fi definita si ca diferenta dintre energia unui atom liber si energia aceluiasi atom cand face parte dintr-un cristal.
Tabelul 1 Energia de coeziune a unor metale exprimata prin caldura de sublimare
|
Metalul |
Caldura de sublimare [kJ/mol] |
|
Argint | |
|
Aluminiu | |
|
Aur | |
|
Crom | |
|
Fier | |
|
Magneziu | |
|
Molibden | |
|
Nichel | |
|
Titan | |
|
Vanadiu |
Metalele si aliajele sunt corpuri solide cristaline. Ele difera de solidele amorfe, in care atomii sunt dispusi dezordonat, prin faptul ca distributia este ordonata prezentand o periodicitate in cele trei directii spatiale la o distanta mare.
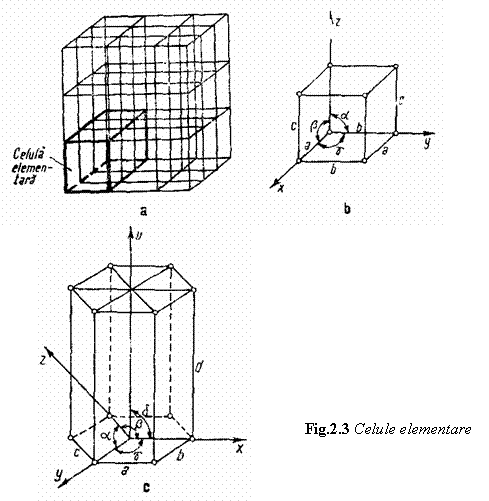
Fiecare cristal metalic este format dintr-un aranjament regulat de ioni pozitivi, care pot fi asimilati cu niste sfere tangente, aranjamentul de ioni poate fi divizat in paralelipipede elementare in contact si egale intre ele. Laturile paralelipipedelor formeaza un sistem de drepte paralele in trei directii necoplanare (ortogonale sau nu). Ansamblul acestor paralelipipede sau celule elementare formeaza reteaua cristalina ale carei noduri sunt punctele de intersectie ale laturilor paralelipipedelor (figura 3).
Un sistem cristalin este definit prin parametrii celulei elementare, adica prin laturile si unghiurile paralelipipedului elementar. In functie de valoarea unghiurilor a b g si de relatiile intre parametri retelei a, b, c, retelele cristaline se impart in sapte sisteme cristaline (cubic, tetragonal, ortorombic, romboidal, hexagonal, monoclinic si triclinic), din care pentru metale sunt caracteristice doua: cubic si hexagonal, ale caror parametri sunt prezentati in tabelul 2 .
Intr-un cristal metalic centrele de oscilatie ale ionilor coincid cu nodurile retelei cristaline, dar ionii pot fi plasati si in afara nodurilor, in pozitii precise in raport cu acestea. Dupa densitatea de umplere cu atomi a celulei elementare, retelele cristaline pot fi:
simple (primitive), cu un singur atom in celula elementara, atomii fiind plasati in colturile celulei (ex. CVC);
compuse, cu mai multi atomi in celula elementara, care sunt amplasati in centrul celulei sau in centrele fetelor (ex. CFC).
Tabelul 2 Sisteme cristaline metalice
|
Sistemul cristalin |
Parametrii retelei |
Metale |
|
Cubic cu volum centrat - CVC |
a b g=90o |
Li, Na, K, Rb, Cs, Ba, Zr, V, Nb, Ta, Cr, Mo, W, Mn, Fea |
|
Cubic cu fete centrate - CFC |
idem |
Cu, Ag, Au, Ca, Sr, Al, Tl, La, Ce, Pb, Th, U, Ni, Rh, Ir, Pt, Feg |
|
Hexagonal compact - HC |
a=b c a b=90o g=120o |
Be, Mg, Zn,Cd, Sc, Y, Ti, Hf, Co, Os |
Un punct al retelei din interiorul celulei i apartine complet celulei, un punct de pe centrul fetei f este comun la doua celule, iar un punct din coltul celulei c este comun la opt celule astfel numarul de atomi al unei celule elementare este dat de relatia:
![]()
Ansamblul spatial al celulelor elementare, in care exista o aranjare ordonata a atomilor, constituie reteaua cristalina. Compactitatea unei retele cristaline se caracterizeaza prin doi parametri: numarul de coordinatie C si gradul de compactitate φ, care se definesc astfel:
numarul de coordinatie reprezinta numarul de vecini care inconjoara un atom al cristalului la distanta minima de acesta;
gradul de compactitate reprezinta, conform modelului sferelor rigide, raportul dintre volumul efectiv ocupat de atomii celulei elementare si volumul celulei.
Spatiile libere dintre atomi in contact reprezinta interstitiile retelei cristaline, care sunt importante la alierea metalelor, cand atomii unor elemente de aliere se asaza in interstitiile metalului de baza. Metalele cristalizeaza intr-un numar limitat de retele cristaline care sunt prezentate in continuare.
In aceasta retea
cristalizeaza cincisprezece metale printre care cele mai utilizate sunt: V,
Nb, Cr, Mo, W, Mn, Fea. Majoritatea metalelor din aceasta
grupa sunt caracterizate prin rezistenta mecanica
ridicata si plasticitate moderata. Conform relatiei de mai
sus, celula elementara a retelei contine doi atomi
determinati astfel: N = 1 + 8 8 = 2 atomi. Utilizand modelul de sfere rigide pentru redarea
amplasa-mentului atomilor in metal, se observa din fig.4. ca in celula
elementara CVC tangenta atomilor are loc dupa diagonala
spatiala a 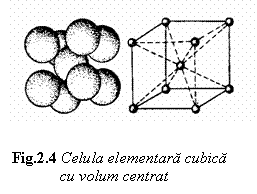 cubului.
cubului.
In baza unor relatii geometrice
simple se obtine corelatia dintre raza atomica r si
parametrul retelei a, si anume: ![]() , de unde rezulta ca unui atom ii revine un
spatiu egal cu 6,16.r3.
, de unde rezulta ca unui atom ii revine un
spatiu egal cu 6,16.r3.
Numarul de coordinatie al acestei retele este 8(C8), ceea ce se poate observa considerand atomul central sau un atom echivalent din colturile cubului.
Gradul de compactitate se calculeaza tinand seama de raza atomica si de faptul ca celula unitara contine doi atomi:
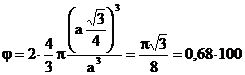 , deci 68%
, deci 68%
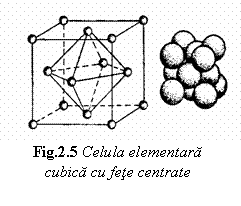 Metalele care cristali-zeaza in
aceasta retea (fig. 5) se caracterizeaza prin ductilitate
si maleabilitate ridicate, printre cele mai uzuale sunt: Cu, Au, Ag, Al,
Ni, Feg, etc.
Metalele care cristali-zeaza in
aceasta retea (fig. 5) se caracterizeaza prin ductilitate
si maleabilitate ridicate, printre cele mai uzuale sunt: Cu, Au, Ag, Al,
Ni, Feg, etc.
Conform relatiei mentionate mai sus celula elementara a retelei contine patru atomi.
Caracteristicile principale ale retelei cubice cu fete centrate sunt:
spatiul ce revine unui atom in celula elementara este egal cu 5,66.r3;
numarul de coordinatie este 12 (C 12);
gradul de compactitate, calculat tinand seama de expresia razei atomice si de faptul ca celula elementara contine patru atomi, este:
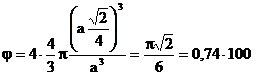 , deci 74%
, deci 74%
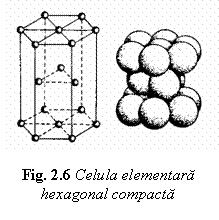 Retea cristalina hexagonal
compacta - HC
Retea cristalina hexagonal
compacta - HC Aceasta retea cuprinde unele metale de mare utilitate practica cum sunt: Be, Mg, In, Ti, Co. Metalele cristalizate in acest sistem se caracterizeaza prin plasticitate redusa , dar sunt excelente elemente de aliere, cu influenta hotaratoare asupra caracteristicilor metalului de baza. Particularitatile geometrice si structurale pentru aceasta retea sunt:
corelatia dintre raza atomica si parametrul retelei este: r=a
numarul de coordinatie este 12 (C12);
numarul de atomi in celula elementara N, asa cum rezulta din fig.6, este 6 (trei atomi in pozitii interne, un atom in centrul fetei bazale si doi atomi in colturile prismei hexagonale): N=12x1 6+2x1
gradul de compactitate, calculat tinand seama de expresia razei atomice si de cei sase atomi ai celulei elementare, este:
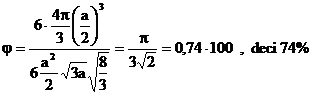
Desi au aceeasi compactitate, intre metalele cristalizate in reteaua CFC, respectiv HC, exista o mare diferenta de comportare la solicitari mecanice legate de cele doua retele. Astfel, in timp ce la reteaua CFC exista patru serii de straturi atomice cu impachetare compacta (normale la cele patru diagonale ale cubului), in reteaua HC exista doar o singura serie de straturi atomice cu impachetare compacta (stratul bazal al prismei). Aceasta particularitate cristalografica explica plasticitatea redusa a metalelor din reteaua HC.
Parametrul retelei si tipul retelei cristaline se determina prin tehnici de difractie (cu raze X sau electronic). Pentru majoritatea metalelor de interes tehnic razele ionilor se afla intr-o gama stransa de valori cuprinsa intre 1,2 -1,45Å .
Examinarea structurii cristaline a metalelor scoate in evidenta faptul ca ele se pot prezenta, in stare solida cristalizata, in mai multe tipuri de retele. Acest fenomen se numeste alotropie sau polimorfism; diversele forme alotropice ale aceluiasi metal sunt stabile in intervale de temperatura bine determinate.
Majoritatea metalelor care prezinta transformari alotropice apartin grupelor secundare ale sistemului periodic ca metale de tranzitie, lantanide, actinide: Ti, Zr, Ag, W, Mn, Fe, Co, Ni, Rh, La, Ce, Th, U, etc. In tabelul 3. sunt prezentate starile alotropice si intervalele de temperatura pentru o serie de metale de importanta tehnica.
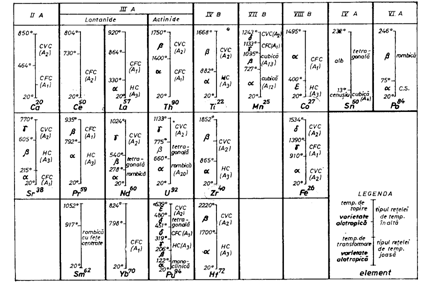
Tabel
3 Varietatile alotropice ale unor metale si intervalele
de stabilitate termica
Aliajele metalelor care prezinta transformari alotropice sunt susceptibile la tratamente termice mai variate datorita posibilitatii de a pastra la temperaturi relativ joase, printr-o racire rapida, starea alotropica de temperatura inalta sau continutul de elemente de aliere existent in starea alotropica de temperatura inalta. Intr-o asemenea stare aliajul este din punct de vedere al constitutiei fazice, in afara de echilibru si poate prezenta proprietati interesante in practica. Astfel la calirea otelurilor densitatea variaza cu cca. 5% prin transformarea fierului g cu reteaua CFC in fier a cu reteaua CVC. In cazul staniului transformarea b in staniu a se face cu o crestere de volum de 26%, ceea ce provoaca faramitarea staniului cenusiu.
Intre formele alotropice diferite ale aceluiasi metal exista diferente de dimensiuni ale interstitiilor retelei, ceea ce are drept consecinta o capacitate diferita ale celor doua forme alotropice de a dizolva atomi straini interstitiali.
Astfel dimensiunea relativ mare a interstitiilor octoedrice din reteaua CFC a fierului g permite dizolvarea carbonului in proportie mai mare decat a fierului a caracterizata prin interstitii mai numeroase, dar mai mici.
Orice produs metalic se obtine, ca regula generala, prin solidificarea unei topituri. La trecerea din starea lichida in starea solida, procesul aranjarii ordonate a atomilor incepe in diferite puncte ale topiturii, care se raceste in jurul unor germeni (centri) de cristalizare (fig.7.a). Fiecare formatie solida va prezenta o aranjare ordonata a atomilor, conform retelei spatiale specifice metalului respectiv, dar orientarea retelelor diverselor formatii va fi intamplatoare (fig.7.b).

a) b) c) d)
Fig. 7 Formarea structurii policristaline
Fiecare formatie cristalina creste in jurul germenului, pana cand cristalele incep sa se incomodeze reciproc in crestere (fig.7.c). In continuare cresterea se produce pe directiile libere pana la consumarea ultimelor cantitati de metal lichid. Se vor obtine in final cristale de forma exterioara neregulata, poliedrice (fig. 7.d) avand marimea de ordinul zecimilor sau sutimilor de milimetri.
Uneori cristalele pot fi obtinute si la dimensiuni mai mari, astfel incat pot fi usor observate cu ochiul liber intr-o zona de rupere a metalului. Aceste cristale de forma neregulata si de marimi diferite se numesc graunti cristalini sau cristalite. Rezulta ca structura unui metal nu este alcatuita dintr-un singur cristal de dimensiuni mari (monocristal), ci dintr-un numar mare de cristale, fapt pentru care ea se numeste structura policristalina.
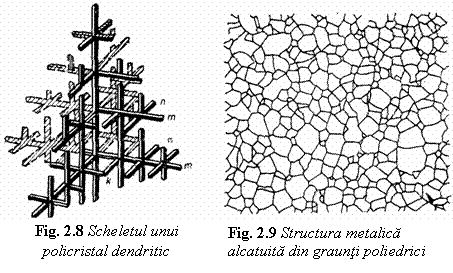
Cristalele metalice (de metal pur sau solutie solida) sunt cristale alotriomorfe ale caror forma exterioara nu prezinta caractere geometrice definite, corelabile cu structura aranjamentului ordonat din reteaua cristalina. In forma lor de utilizare metalele si aliajele sunt materiale policristaline, adica agregate compacte de cristale microscopice in contact. Aceste policristale au forme oarecare, impuse de constrangerile exterioare care au loc in cursul solidificarii sau in procesele de prelucrare la cald (deformare plastica, tratamente termice, etc.). Forma obisnuita a cristalelor materialului metalic policristalin este dendrita, in materialele turnate (fig.8.) si forma de poliedre neregulate in materialele deformate la cald (fig.9.).
Forma dendritica sau arborescenta a cristalelor metalice solidificate din topitura este o consecinta a caracterului nedirectionat al legaturii interatomice de tip metalic. Forma dendritica a cristalelor metalice rezultata la solidificare se transforma in procesul de deformare plastica la cald sau la reincalzire (recoacere), in poliedre neregulate asa cum se prezinta in fig.9.
Pentru a-si micsora energia superficiala un material policristalin tinde sa -si reduca aria limitei de graunte, lucru posibil cand metalul este mentinut la temperatura ridicata, prin deplasari ale atomilor din reteaua cristalina prin procese de difuzie. Tendinta de reducere a ariei limitei de graunte determina o serie de caracteristici ale structuri metalelor cum ar fi: globulizarea, cresterea grauntilor la recoacere, schimbarea formei dendritice in forme poliedrice, etc.
Structura de solidificare prezinta importanta practica pentru trei categorii de aplicatii tehnice ale procesului de cristalizare:
producerea lingourilor metalice destinate prelucrarii prin deformare plastica;
producerea pieselor turnate metalice;
producerea de piese metalice prin alte procedee ca: sudare, lipire, sinterizare, topire zonala, etc.
Procesul de solidificare exercita o influenta decisiva asupra structurii si calitatii materialului metalic turnat, prin aspectele fizice prezentate in continuare.
Formarea cristalelor la solidificare este rezultatul a doua procese elementare :
a) formarea in topitura a germenilor de cristalizare;
b) cresterea germenilor formati.
Deoarece mersul solidificarii este determinat de vitezele cu care se desfasoara nasterea germenilor si cresterea lor, parametrii de baza ai cristalizarii sunt : viteza de aparitie a germenilor cristalini numita si viteza de germinare si viteza de crestere a acestor germeni.
Procesul de germinare poate avea loc in conditii de topitura omogena (metal pur) si eterogena (in prezenta unor incluziuni preexistente in topitura). Formarea germenilor prin germinare omogena presupune existenta unei subraciri DT a topiturii sub temperatura de solidificare Ts. Cand topitura este subracita sub Ts, in diverse puncte ale lichidului apar simultan germeni de cristalizare. Stabilitatea unui germene cristalin este determinata de doi factori:
modificarea energiei libere F la tranzitia lichid-solid;
aparitia unei energii superficiale in suprafata de separare interfazica dintre germene si topitura. Luand in considerare ambii factori la formarea din topitura a unui embrion sferic de raza r, energia libera a sistemului se modifica cu D F:
DF= - 4/3pr3DFv +4pr2s unde:
DFv-reprezinta modificarea energiei libere pe unitatea de volum la cristalizare;
s - energia superficiala la formarea unitatii de suprafata.
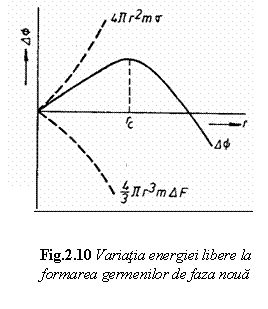 Reprezentarea grafica a ecuatiei
de mai sus este data in figura 10. de unde rezulta ca sunt stabile
si vor creste numai particulele de faza solida pentru care
r rc deoarece cresterea acestor particule este insotita de micsorarea
energiei libere
Reprezentarea grafica a ecuatiei
de mai sus este data in figura 10. de unde rezulta ca sunt stabile
si vor creste numai particulele de faza solida pentru care
r rc deoarece cresterea acestor particule este insotita de micsorarea
energiei libere
Raza critica rezulta din prima derivata a relatiei de mai sus este : rc=2s/ΔFv
Rezulta astfel ca o crestere a razei critice la germinare este insotita de micsorarea energiei libere specifice si de cresterea tensiunii superficiale s. Dar in procesul de cristalizare sunt necesare structuri cu granulatie fina pentru a obtine proprietati superioare in metalul solidificat, si deci trebuie micsorata tensiunea superficiala, lucru ce se poate realiza prin introducerea in topitura a unor impuritati solubile in cantitati mici (de ordinul zecimilor sau sutimilor de procente).
Aceste elemente fiind superficial active se concentreaza prin adsorbtie pe suprafetele de separare dintre faza solida si lichida, micsorand tensiunea superficiala pe de o parte si constituind insasi ele germeni de cristalizare, pe de alta parte.
O astfel de germinare se numeste eterogena cand germenii cristalini se formeaza pe suprafete preexistente in topitura. Cantitatea de particule insolubile active in procesul de germinare eterogena poate fi crescuta prin introducerea unor adaosuri insolubile sau care formeaza cu componentii topiturii compusii greu fuzibili. Asemenea substante se numesc modificatori si permit reglarea procesului de cristalizare si finisarea grauntilor din piesele turnate.
Cresterea germenilor cristalini se produce ca rezultat al trecerii atomilor din lichidul subracit in nucleele cristaline produse la germinare. Cresterea incepe mai intai prin formarea in topitura a unor mici grupari de atomi de grosime monoatomica, numite germeni bidimensionali, stabile din punct de vedere termodinamic. Cresterea cristalelor continua prin formarea de noi germeni bidimensionali si dezvoltarea lor in structuri atomice.
Formarea germenilor bidimensionali necesita subraciri relativ mari, in multe cazuri insa cresterea cristalelor se face la subraciri mici, in conditii in care germenii bidimensionali nu se pot forma. Acest mecanism, mai convenabil din punct de vedere energetic, se realizeaza prin intermediul dislocatiilor elicoidale care se formeaza in trepte pe suprafata cristalului initial.
Mersul solidificarii este determinat de viteza de germinare n si de capacitatea de crestere a germenilor c. Experimental si teoretic s-a demonstrat ca volumul v al materialului solidificat variaza cu timpul dupa o curba reprezentata cu linie continua in fig.11.
Marimea vitezei de solidificare
dv/dt este determinata de numarul efectiv de atomi care trec in
unitatea de timp in faza solida. Viteza de solidificare atinge
valoarea maxima cand topitura s-a solidificat 50%.
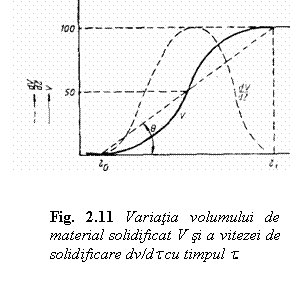 Din curba de variatie a vitezei de
solidificare si a volumului de material solidificat se constata
ca procesul nu incepe imediat ci dupa trecerea unui timp t numit perioada de incubare, durata
transformarii fiind t t
Din curba de variatie a vitezei de
solidificare si a volumului de material solidificat se constata
ca procesul nu incepe imediat ci dupa trecerea unui timp t numit perioada de incubare, durata
transformarii fiind t t
Marimea cristalelor care se formeaza la solidificare depinde de raportul n/c; cu cat viteza de germinare n este mai mare si viteza de crestere c este mai mica, cu atat vor fi mai mici graunti care se obtin, deci cu atat va fi mai mare numarul lor. Numarul de graunti N in unitatea de volum este egal cu:
![]() ; a- constanta
adimensionala.
; a- constanta
adimensionala.
O metoda frecvent folosita pentru obtinerea unor graunti fini consta in cresterea vitezei de racire care conduce la cresterea vitezei de germinare. Obtinerea unor graunti mici se poate realiza, asa cum s-a mai aratat, prin utilizarea modificatorilor, adica a unei substante introduse in topitura care actioneaza ca drept catalizator ai germinarii.
Cristalele care cresc liber isi dezvolta liber formele exterioare, caracterizate prin cea mai mica energie superficiala data de relatia care satisface starea de echilibru a cristalelor:
SσiSi = minim,
unde :
σi - tensiunea superficiala a fetei cristalului
Si - suprafata fetei cristaline.
Relatia de mai sus este cunoscuta sub numele de legea Curie - Wolff si arata ca viteza de crestere a unui cristal este anizotropa, cristalul crescand cu cea mai mare viteza de-a lungul directiei perpendiculare pe fata cu cea mai mare tensiune superficiala (planul cu cea mai mica densitate in atomi).
Solidificarea se produce de regula in afara conditiilor de echilibru, cand interfata lichid-solid nu este perfect neteda ci contine o serie de denivelari care se formeaza ca urmare a modului de crestere a fazei solide. Intr-o astfel de interfata varful denivelarii se afla intr-un lichid subracit mai puternic decat masa de lichid din vecinatatea interfetei. Varful denivelarii creste cu o viteza mult mai mare decat deplasarea interfetei in conditii de subracire. Se dezvolta in acest fel pe interfata solid-lichid ramuri cristaline foarte lungi numite axe principale .
Acest proces se produce si la interfetele dintre axele principale si topitura; ca urmare denivelarile de pe axa principala-topitura vor creste foarte repede formand o alta familie de axe numite secundare. In mod asemanator din axele secundare se vor dezvolta axe tertiare si asa mai departe. Se formeaza astfel un schelet arborescent numit dendrita (fig.12).

Cresterea unei dendrite are loc pana la intalnirea ei cu dendritele vecine, moment in care cresterea axelor primare se opreste, solidificarea continua prin formarea ramificatiilor de ordin superior pana cand tot spatiul dintre ramificatii se umple cu metal solid. Ca urmare aspectul dendritic dispare si intreaga masa solidificata este formata dintr-un conglomerat de graunti cristalini poliedrici, fiecare dendrita transformandu-se intr-un graunte cristalin (fig.13).
Grauntii
cristalini variaza ca forma, marime si orientare; fetele
lor nu sunt fete cristalite regulate deoarece fiecare graunte este
impiedicat in cresterea sa de
grauntii vecini. In structura grauntilor se pot forma
si pune in evidenta dendrite libere datorita contractiei de 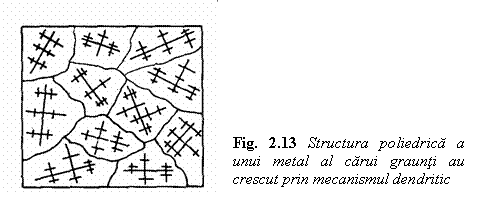
volum a metalului la solidificare.
Structura de solidificare este determinata de compozitia chimica a topiturii si de viteza de solidificare. Microstructura se refera la forma si marimea grauntilor si modelul de asociere a fazelor constitutive. Macrostructura se caracterizeaza prin variatia caracteristicilor microstructurale in volumul materialului.
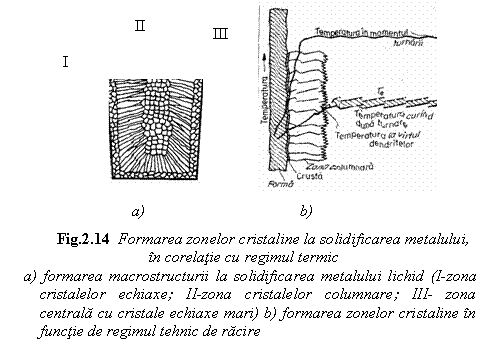
Tipul obisnuit de macrostructura (fig. 14) cuprinde trei zone distincte:
I - crusta sau zona exterioara a metalului solidificat cu cristale echiaxe mici;
II - zona cristalelor columnare;
III - zona centrala cu cristale echiaxe mari.
Crusta sau zona exterioara se formeaza prin germinare eterogena pe peretele formei de turnare , asa cum se poate constata si din fig. 14.
Cristalizarea la grade mari de subracire a topiturii, asa cum se produce la contactul lichidului cu peretele formei, produce o viteza mare de germinare a cristalelor din topitura, ceea ce asigura in zona cresterii o granulatie foarte fina.

Cristalele dendritice din aceasta zona au orientare cristalina intamplatoare fiind provenite dintr-un mare numar de germeni diferiti.
In zona II, dintr-un numar de graunti cu orientare intamplatoare prezenti in crusta, isi continua cresterea doar un numar redus care are axul dendritei in directia fluxului termic, deci pe directia perpendiculara peretelui formei. Datorita micsorarii gradului de subracire a topiturii din zona II, viteza de crestere a acestor cristale se mareste si dendritele se dezvolta rapid in directia axului lor principal, capatand o forma columnara, care da materialului solidificat o pronuntata anizotropie a proprietatilor, aceasta fiind utila in anumite aplicatii speciale.
Zona III se formeaza printr-o noua germinare in lichidul care are grad mic de subracire in zona centrala a lingoului; dezvoltarea cristalelor din zona centrala opreste cresterea cristalelor columnare. Gradientul termic fiind foarte mic, dezvoltarea cristalelor se face relativ uniform in toate directiile, rezultand graunti echiacsi. In zona centrala subracirea necesara pentru germinare este de natura constitutionala, produsa de impuritatile acumulate in aceasta zona si de fragmentele de dendrite rupte din ramurile cristalelor datorita curentilor de convectie din lichid.
Intinderea relativa a zonei columnare si a zonei centrale depinde de caracteristicile aliajului si de regimul de racire. Lungimea dendritelor este determinata de intervalul de solidificare a aliajului: Ts = (Tlichidus-Tsolidus) si de gradientul termic mediu Gm in zona bifazica constituita din dendrite in crestere si lichidul interdendritic.
![]()
Exista si alti factori legati de conditiile de turnare care actioneaza in sensul largirii zonei cristalelor echiaxe si anume:
supraincalzirea mica a topiturii;
turnarea in forme de amestec in locul cohilelor;
amestecarea topiturii prin vibratii mecanice sau ultrasonice cu fragmentarea dendritelor si disiparea caldurii in masa de metal.
In majoritatea cazurilor se urmareste obtinerea unei granulatii fine in metalul turnat, lucru care se realizeaza practic prin turnarea in cohile, care asigura un grad mare de subracire si prin introducerea de modificatori in topitura.
Tensiunile reziduale sunt prezente in piesele turnate datorita diferentelor de masivitate a sectiunii lor. Pe parcursul solidificarii portiunile cu sectiune mare din piesa se afla inca in stare lichida, in timp ce portiunile cu sectiune subtire sunt solidificate si racite. Cand se solidifica si portiunile masive contractia lor solicita la intindere sau comprimare portiunile solidificate anterior.
Portiunile subtiri ale piesei aflate la temperatura mai scazuta nu se pot deforma plastic si actiunea provocata de contractia portiunilor groase se mentine sub forma de tensiuni interne sau tensiuni reziduale in material. Cand aceste tensiuni sunt mari ele pot provoca ruperea piesei la jonctiunea intre doua portiuni de sectiune diferita.
Porozitatea este un aspect fizic important al micro si macrostructurii materialelor metalice turnate determinata de prezenta discontinuitatilor sau golurilor. Asemenea defecte pot sa apara ca efect al micsorarii de volum care insoteste solidificarea, sau ca efect al degajarii gazelor dizolvate in topitura ori ca efect combinat al ambelor cauze.
Toate metalele cu structura cristalina compacta (CVC, CFC si HC) se contracta la solidificare. Contractia totala la turnare este egala cu diferenta de volum intre lichidul la temperatura de turnare (Tl) si materialul solidificat la temperatura camerei (Ts).
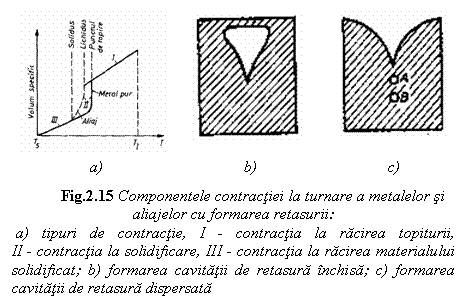
Contractia totala (fig. 15) cuprinde contractia lichidului pana la temperatura de inceput de solidificare (I), contractia in intervalul de solidificare (II) si contractia solidului de la temperatura de sfarsit de solidificare (III) pana la temperatura ambianta.
Cea mai mare parte a contractiei de turnare apare sub forma cavitatii de retasura. Aparitia si formarea cavitatii de retasura este determinata de caracterul concav al frontului de cristalizare izoterm. La randul sau concavitatea este determinata de cantitatile relative de caldura eliminate in directia verticala, respectiv in directiile orizontale (fig. 15.a). Daca solidificarea se produce nu numai la baza si la peretii formei ci si la suprafata superioara libera a topiturii se formeaza o retasura inchisa (fig.15.b). Lichidul din zonele de solidificare ramane izolat de restul masei de lichid si apar cavitati inchise sub forma de porozitati (fig.15.c). Rezulta concluzia importanta ca orice portiune de topitura careia i se intrerupe alimentarea cu lichid in timpul solidificarii, formeaza o cavitate inchisa (o porozitate) in momentul in care se solidifica.
Dificultatile de alimentare cu lichid a canalelor interdendritice conduc la aparitia unor goluri de contractie de dimensiuni microscopice care constituie microporozitatea. Dimensiunile tipice ale porilor sunt intre 5 si 10 μm in zona cristalelor columnare si de aproximativ 25 μm in zona cristalelor echiaxe.
Gazele care se degaja la solidificare formeaza sufluri in materialul turnat. Originea degajarii de gaze de la solidificare o reprezinta fie anumite reactii chimice in topitura metalica, fie scaderea drastica a solubilitatii gazelor in metalul solid. Gazele rejectate din topitura se acumuleaza in lichidul din fata frontului de solidificare pana ce ating o concentratie suficienta pentru a provoca germinarea de bule. Comportarea ulterioara a bulelor depinde de viteza de deplasare a frontului de cristalizare, astfel:
daca frontul de solidificare se deplaseaza rapid bulele de gaz sunt inchise in materialul solid sub forma de sufluri sferice;
daca frontul de cristalizare se deplaseaza mai lent in acelasi timp cu cresterea bulelor, prin difuzia gazelor din topitura, bulele dau nastere la sufluri cilindrice cu axul perpendicular pe frontul de solidificare;
daca viteza de deplasare a frontului de cristalizare este mai mica decat viteza de difuzie a gazelor din topitura, bulele de gaz cresc suficient pentru a se desprinde si a se ridica la suprafata libera a topiturii unde se elimina in atmosfera.
Microporozitatea poate fi redusa prin turnare sub presiune sau prin degazare in vid, ultimul procedeu este frecvent utilizat la turnarea metalului lichid in lingouri sau piese.
In structura pieselor turnate se gasesc anumite cantitati de incluziuni nemetalice sub forma de particule de oxizi, sulfuri, silicati, etc. Proprietatile de utilizare a materialelor metalice sunt afectate negativ de prezenta incluziunilor, care constituie intreruperi in continuitatea masei metalice. Incluziunile pot fi de origine exogena (resturi de materiale refractate, particule de zgura) sau de origine endogena (ca urmare a reactiilor chimice rezultate din procesul de elaborare: oxizi, sulfuri, etc.).
In procesul de solidificare se produc neuniformitati in distributia elementelor chimice numite segregatii. La interfata solid - lichid de forma dendritica elementele de aliere sau impuritatile cu coeficient de distributie subunitar sunt rejectate in lichid. Transportul de masa longitudinal este de lunga distanta, care da nastere macrosegregatiei in directia de avans a frontului.
Transportul de masa lateral este un transport de scurta distanta, care da nastere unei microsegregatii la nivel de cristal. In tabelul 4. este prezentat gradul de segregare a unor elemente in oteluri aliate.
Tabelul 4 Segregatia elementelor de aliere in otel
|
Material |
Distanta de la peretele lingotierei, in mm |
Gradul de segregare, (GS) |
|
Ni in otelul 40 Mo CN 15 | ||
|
Ni in aliajul FeNi 10 | ||
|
Cr in otel de rulmenti |
Structura de solidificare sau structura primara influenteaza proprietatile de utilizare a materialelor metalice indiferent de prelucrarile ulterioare.
Metalul turnat poate fi utilizat in urmatoarele stari:
in stare brut turnata;
tratat termic dupa turnare;
deformat plastic dupa turnare;
deformat si tratat termic.
Principalii parametri ai structurii primare care influenteaza proprietatile mecanice ale materialelor metalice sunt: porozitatea, distanta interdendritica, prezenta fazelor secundare, marimea de graunte.
Porozitatea influenteaza negativ proprietatile mecanice pe doua cai: porii actioneaza ca niste concentratori de tensiuni, precum si prin reducerea sectiunii efective a piesei metalice. Influenta porozitatii este maxima in cazul pieselor turnate utilizate ca atare. Aceasta influenta se reduce prin efectuarea unei deformari plastice, cand porii se sudeaza partial sau total.
Micsorarea distantei intre ramurile dendritelor mareste ductilitatea si rezistenta la rupere la tractiune, efectul fiind datorat unei omogenizari mai bune pe seama reducerii microsegregatiilor.
Prezenta fazelor secundare in aliaje (compusi intermetalici si solutii solide secundare) maresc susceptibilitatea la tratamente termice si contribuie la imbunatatirea tuturor proprietatilor mecanice.
Marimea grauntelui cristalin influenteaza rezistenta mecanica a metalelor, in sensul ca aceasta creste cu gradul de finisare a grauntilor conform relatiei:
![]()
unde:
d - diametrul mediu al grauntilor;
σ- limita de curgere;
σ o si K - constante de material.
Un material metalic in stare de lingou, semifabricat sau piesa contine in volumul sau numeroase abateri de la ordinea perfecta a atomilor in reteaua cristalina. Aceste abateri de la aranjamentul ordonat al atomilor constituie imperfectiuni sau defecte care provoaca modificari esentiale ale unor proprietati ale metalului. Astfel se estimeaza ca rezistenta la rupere a unui monocristal metalic ideal este de 100 pana la 1000 de ori mai mare decat in materialul real.
Ca proportie, in volumul materialului cristalin, imperfectiunile de retea reprezinta o mica fractiune. De exemplu, chiar in metalele puternic deformate proportia atomilor aflati in afara pozitiilor de echilibru este mai mica de 1 la 1000, deci predominant ramane aranjamentul ordonat care caracterizeaza reteaua cristalina. Cu toate acestea, influenta exercitata de imperfectiunile de retea asupra unor proprietati importante, cum sunt proprietatile mecanice de rezistenta si de plasticitate ale metalelor, este considerabila. Ca urmare, proprietatile metalelor si aliajelor pot fi impartite in doua categorii:
proprietati independente sau putin dependente de structura de fond determinata de natura metalului sau aliajului; nefiind afectate de prezenta si cantitatea imperfectiunilor de retea. Printre acestea se numara: cateva proprietati mecanice (constante elastice, densitatea), termice (temperatura de topire, caldura specifica, conductibilitatea termica, dilatarea), electrice si optice.
proprietati dependente de structura, care isi schimba valoarea in limite largi in functie de natura si cantitatea imperfectiunilor de retea introduse in diversele faze ale procesului de prelucrare. Proprietatile sensibile la structura includ proprietati mecanice de rezistenta si plasticitate, ca si unele proprietati magnetice si electrice.
De remarcat este faptul ca proprietatile care stau la baza utilizarii materialelor metalice sunt proprietatile mecanice sensibile la structura.
Pe langa imperfectiuni, reteaua cristalina poate prezenta si distorsiuni elastice sau tensiuni interne. Din aceasta cauza parametrii retelei se abat in zonele tensionate de la valorile ideale cu diferente in plus sau in minus cu valori de cca. 1%. Printre proprietatile metalelor si aliajelor puternic afectate de prezenta tensiunilor interne se numara rezistivitatea electrica si susceptibilitatea la coroziune.
Defectele retelelor cristaline pot fi din punct de vedere geometric: punctiforme, liniare si de suprafata.
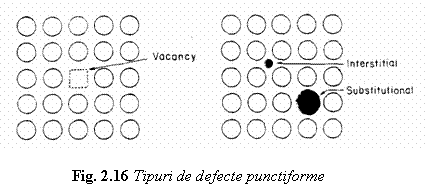
Acest tip de defecte apare in celula cristalina sub trei forme, asa cum se prezinta schematic in fig. 16:
vacante sau pozitii neocupate in nodurile retelei;
atomi interstitiali stranii patrunsi printre atomii ordonati ai retelei;
atomi de substitutie stranii care inlocuiesc atomii proprii din nodurile retelei cristaline.
Vacantele pot fi create prin racirea rapida a metalului din starea lichida, in timpul deformarii plastice si prin expunere la sarcini ciclice a materialului metalic. Existenta vacantelor in cristale face posibila autodifuzia atomilor la temperaturi joase. De asemenea difuzia atomilor in stare solida ar fi imposibila fara prezenta in retea a vacantelor.
Atomii de substitutie cat si cei de interstitie pot provoca deranjamente ale retelei cristaline, manifestate prin deformarea geometrica a acesteia si cresterea gradului de compactitate al retelei.
Defectele liniare constau din anomalii de dispunere a unor plane cristaline, ele sunt denumite dislocatii. Se disting doua tipuri mai importante de dislocatii: dislocatia pana si dislocatia elicoidala.
Dislocatia pana consta dintr-un sir de atomi, fiecare atom al sirului avand un numar de vecini deficitar (un vecin in minus) fata de numarul normal din structura cristalina perfecta. O asemenea dislocatie este indicata in fig. 17 prin simbolul linia de dislocatie fiind perpendiculara pe planul figurii.


Dislocatia pana poate fi considerata drept limita a unui semiplan atomic suplimentar existent in portiunea superioara a cristalului. In fig. 18 linia de dislocatie MN prezentata in perspectiva intr-un cristal, indica prezenta sirului atomic cu numar incorect de vecini, care se extinde intr-o regiune cilindrica cu axa DD' si raza de 3 - 4 diametre atomice.
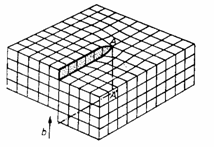
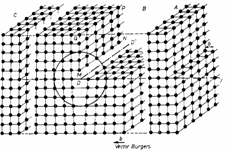
Fig. 18 Sectiune intr-o retea Fig. 19 Reprezentarea unui cubica simpla care contine o cristal care contine o dislocatie dislocatie pana elicoidala AA'
Zona dislocatiei este o regiune de dezordine atomica, in care sferele atomice se afla in stare de compresie (in partea superioara a planului xy) si in stare de dilatare sau intindere (in portiunea de sub planul xy al dislocatiei).
Vectorul de alunecare ![]() numit vector Burgers
este continut in planul de alunecare xy care este in acest caz
perpendicular pe linia de dislocatie, aspect ce caracterizeaza
dislocatia tip pana.
numit vector Burgers
este continut in planul de alunecare xy care este in acest caz
perpendicular pe linia de dislocatie, aspect ce caracterizeaza
dislocatia tip pana.
Dislocatia elicoidala (fig.19) rezulta printr-o forfecare a cristalului in plan vertical, linia de dislocatie AA' delimiteaza zona planului de forfecare, in care s-a produs deja alunecarea fata de zona nedeformata a cristalului.
Deplasarea masurata prin vectorul Burgers ![]() , este in acest caz paralela cu linia de
dislocatie. Planele cristaline, care inaintea forfecarii erau
orizontale, au forma unei suprafete elicoidale care se
infasoara in jurul liniei de dislocatie AA'.
, este in acest caz paralela cu linia de
dislocatie. Planele cristaline, care inaintea forfecarii erau
orizontale, au forma unei suprafete elicoidale care se
infasoara in jurul liniei de dislocatie AA'.
Se remarca faptul ca o dislocatie elicoidala fiind paralela cu vectorul Burgers este de regula rectilinie. Dislocatia pana fiind perpendiculara pe vectorul Burgers poate lua o alta directie in planul normal la acest vector.
In cristalele reale dislocatiile sunt mixte, fiecare segment al dislocatiei avand o componenta tip pana si o componenta de tip elicoidal. Conturul unei dislocatii mixte are o forma spatiala complexa, acesta este tipul cel mai general de dislocatii.
O linie de dislocatie nu se poate opri decat la intersectia cu suprafata limitei de graunte, cu suprafata libera a cristalului sau la intersectia cu o alta dislocatie sau la o intalnire cu un alt atom strain. Intr-un cristal nedeformat liniile de dislocatie sunt legate intre ele in puncte numite noduri de dislocatie, alcatuind o retea tridimensionala numita retea Frank. Lungimea medie a unui segment de dislocatie din reteaua Frank este cuprinsa intre 10-2 -10-4 cm.
Densitatea dislocatiilor, exprimate ca lungime totala a
dislocatiilor din unitatea de volum a materialului sau ca numar de
dislocatii ce intersecteaza unitatea de suprafata, variaza
intre 105-106/cm2 in metalele recoapte. O
alta exprimare mai sugestiva arata ca densitatea
dislocatiilor intr-un metal recopt este de 1km/cm3 si
atinge in metalele deformate la rece valoarea de 107km/cm3.
Se admite ca dislocatiile se formeaza la solidificarea metalului
pe baza disparitiei excesului de vacante existent in lichid.
Dislocatiile se multiplica mai ales prin deformare plastica,
fenomenul fiind insotit de o marire a energiei libere. Energia
acumulata intr-o dislocatie este proportionala cu lungimea
ei. Aceasta energie acumulata in unitatea de lungime - numita si tensiune liniara a
dislocatiei este aproximativ egala cu Gb2 (G - modulul de elasticitate transversal al
materialului, ![]() este vectorul Burgers
al dislocatiei), ceea ce conduce la o valoare de cca. 3 eV pe lungimea de
dislocatie, cuprinsa intre doua plane cristaline.
este vectorul Burgers
al dislocatiei), ceea ce conduce la o valoare de cca. 3 eV pe lungimea de
dislocatie, cuprinsa intre doua plane cristaline.
Viteza de deplasare a dislocatiilor in cursul deformarii plastice a metalelor este de ordinul 0,1 mm/secunda . In deplasarea lor, dislocatiile pot juca rol de surse de vacante cat si rol de zone de anihilare a vacantelor, contribuind la stabilirea echilibrului termic al vacantelor.
Principalele defecte de suprafata in metale sunt: limitele de graunte, limitele de subgraunte, structura de blocuri mozaic si defectele de impachetare.
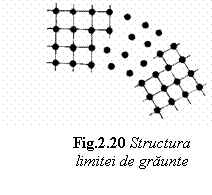
Limitele de graunte reprezinta suprafetele de separare intre grauntii cristalini din metal. Tranzitia de la un graunte la altul se face printr-o zona cu grosime de cateva diametre atomice, numita limita de graunte. In aceasta zona aranjamentul atomic nu corespunde cu cel al cristalelor vecine, ci este un aranjament de tranzitie (fig.20), cu un grad pronuntat de dezordine, in care este prezenta o retea complicata de dislocatii si vacante.
Limitele de graunte au o reactivitate chimica sporita din cauza concentrarii de defecte de retea si de impuritati. Aceasta poate fi observata prin microscopie optica pe o proba atacata cu un reactiv chimic corespunzator.
 Energia superficiala a limitei de
graunte este superioara celei corespunzatoare altor defecte; de
exemplu in cupru ea are valoarea de 500 ergi/cm Datorita surplusului de
energie si a concentratiei sporite de atomi stranii, limitele de
graunte constituie sediul de initiere a transformarilor in stare
solida din metale.
Energia superficiala a limitei de
graunte este superioara celei corespunzatoare altor defecte; de
exemplu in cupru ea are valoarea de 500 ergi/cm Datorita surplusului de
energie si a concentratiei sporite de atomi stranii, limitele de
graunte constituie sediul de initiere a transformarilor in stare
solida din metale.
Suprafetele interfazice reprezinta limitele de separare intre grauntii din faze diferite. Structura acestor suprafete este mai complexa decat a limitei de graunti dintr-un material monofazic, pentru ca interfata reprezinta o tranzitie intre graunti cu retea cristalina diferita. Exista doua tipuri de interfete:
a) interfete necoerente, la care nu exista nici o continuitate intre retelele cristaline ale celor doua faze si care nu se deplaseaza usor in cazul deformarii plastice;
b) interfete coerente la care fazele vecine sunt inrudite ca structura cristalina, ceea ce permite ca anumite plane cristaline, cu aranjamentul atomic comun ambelor retele, sa serveasca drept interfata continua intre fazele vecine.
Limitele de subgraunte sunt limite intre grauntii a caror diferente de orientare cristalografica este foarte mica, asa cum este cazul dislocatiei tip pana.
Subgrauntii apar de obicei in cursul cresterii cristalelor. Poligonizarea, care se produce la recoacerea de temperatura joasa a metalelor deformate plastic, consta in distribuirea dislocatiilor si gruparea lor in pereti de tip limita de subgraunte, ca urmare grauntele se divizeaza in mai multi subgraunti usor dezorientati intre ei.
Structura de blocuri mozaic
Regularitatea retelei cristaline nu se mentine in tot volumul unui graunte cristalin. Grauntele se compune din juxtapunerea unei multitudini de mici blocuri cu structura cristalina perfecta avand dimensiuni de cca. 1000 ori mai mari decat celula elementara.
Defectele de impachetare marcheaza planul de separare intre doua portiuni cristaline identice intre care s-a produs o alterare a succesiunii normale a structurii atomice compacte. Aceste defecte apar in cristalele cu retea de maxima compactitate (HC si CFC) in cursul cristalizarii la viteze de solidificare suficient de mari, asa cum se intampla in practica. In cursul deformarii plastice se produc defecte de impachetare delimitate de dislocatii partiale. Energia superficiala a defectelor de impachetare este mica, cca 10 erg/cm2 la cupru si de 100 -200 erg/cm2 la aluminiu.
Limitele de macla reprezinta limita de separare intre cristal si macla si consta dintr-un strat monoatomic, care apartine in comun cristalelor si maclei, aceasta limita poate fi considerata ca o interfata coerenta intr-un material monofazic. Macla reprezinta o portiune dintr-un cristal cu alta orientare cristalina decat restul cristalului. O caracterizare rezumativa a imperfectiunilor din cristalele reale este prezentata in tabelul 5.
Tabelul 5 Imperfectiuni in cristale
|
Tip |
Denumire |
Descriere |
|
Defecte plane |
Limita de graunte Limita de subgraunte Defect de impachetare |
- Limita dintre doua cristale intr-un material policristali; - Limita dintre doua portiuni adiacente perfecte in acelasi cristal care se deosebesc printr-o mica diferenta de orientare; - Limita dintre doua portiuni de cristal care au succesiunea straturilor schimbata |
|
Defecte liniare |
Dislocatie pana Dislocatie elicoidala |
- Sirul de atomi cu care se termina in interiorul cristalului un plan cristalin incomplet (semiplan); - Sirul de atomi in jurul caruia un plan cristalin normal se desfasoara in forma de spirala . |
|
Defecte punctiforme |
Vacanta Atom interstitial Defect complex |
- Atom absent intr-un punct al retelei. - Atom suplimentar in pozitie interstiti-ala ; - Atom deplasat in pozitie interstitiala si vacanta asociata pe care o creeaza. |
Dintre imperfectiunile existente in retelele cristaline metalice prezentate, cele mai importante influente asupra comportarii materialelor metalice o au dislocatiile, astfel:
prezenta unei dislocatii intr-un cristal provoaca deformarea elastica a retelei cristaline in vecinatatea dislocatiei; reteaua cu dislocatii are o energie interna mai mare decat fara dislocatii; metalele si aliajele aflate in apropierea starii de echilibru au densitatea dislocatiilor mai mica;
dislocatiile se pot deplasa cu usurinta prin cristale producand deformarea plastica a acestora;
in calea dislocatiilor in miscare pot apare obstacole care produc blocarea lor. Orice defect al retelei cristaline sau neomogenitate constituie piedici in calea miscarii dislocatiilor ca: atomi stranii, precipitatele microscopice, limitele grauntilor. O consecinta directa a blocarii dislocatiilor o constituie micsorarea plasticitatii materialului (ecruisarea materialelor metalice).
dislocatiile se pot multiplica; s-a dovedit experimental ca in procesul de deformare a metalelor densitatea dislocatiilor creste foarte mult. Astfel, in timp ce in metalele recoapte densitatea dislocatiilor este de cca. 106/ cm2, in metalele deformate plastic densitatea acestora creste pana la 1012 / cm
Copyright © 2024 - Toate drepturile rezervate