 | Biologie | Chimie | Didactica | Fizica | Geografie | Informatica |
| Istorie | Literatura | Matematica | Psihologie |
Universitatea Politehnica
Facultatea de Chimie Industriala si Ingineria
Mediului
PROIECT TEHNOLOGIC
p Nitrofenol
Cuprins
1. Tema proiectului..
2. Introducere..
3. Consideratii teoretice.
3.1. Prezentarea produsului.
3.2. Metode de obtinere.
3.3. Intrebuintari ale produsului
3.4. Toxicitate
4. Proiectarea tehnologica
4.1. Caracterizarea materiilor prime..
4.2. Schema fluxului tehnologic..
4.3. Descrierea procesului tehnologic
4.4. Bilantul de materiale.
5. Bibliografie..
1. Tema proiectului
Sa se proiecteze o instalatie de obtinere a p-nitrofenolului prin nitrarea fenolului cu acid azotic.
2. Introducere
Prin nitrarea fenolilor se pot obtine mononitrofenoli sau polinitrofenoli in functie de concentratia acidului azotic si de temperatura. Astfel, folosind acid azotic diluat (20%) si temperatura putin ridicata (25oC) se obtine un amestec de o- si p-nitrofenol.
3. Consideratii teoretice
3.1. Prezentarea produsului
Denumire: p-Nitrofenol
Formula moleculara: C6H5NO3
Formula structurala:
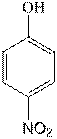
Masa moleculara: 139,11
Punct de topire: 113-114˚C
Punct de fierbere: 279˚C
Solubilitate in apa:10 g/L (15˚C); 11,6 g/L (20˚C); 16 g/L(25˚C)
p-Nitrofenolul mai poate fi numit si 4-nitrofenol sau 4-hidroxinitrobenzen si este un compus fenolic ce are o grupare nitro in pozitia opusa gruparii hidroxi pe inelul benzenic.
p-Nitrofenolul formeaza cristale de culoare galben deschis, aproape incolore, acestea fiind de fapt un amestec a doua stari polimorfe:
-forma α − cristale aproape incolore,instabile la temperatura camerei;
-forma β − cristale galbene,treptat devin rosii la actiunea radiatiilor solare,stabile la temperatura camerei .
p-Nitrofenolul se dizolva usor in alcool cu formarea unei coloratii galbene,precum si in solutii de hidroxizi si carbonati ai metalelor alcaline.Nu este antrenabil cu vapori de apa.
Solutiile galbene de p-nitrofenol in alcalii diluate se coloreaza prin acidulare.
3.2. Metode de obtinere
1. Tratarea cu NaOHaq a p-nitroclorbenzenului:
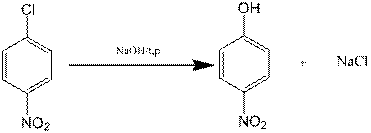
2. Tratarea fenolului cu NaNO2 cand rezulta p-nitrozofenolul care se oxideaza cu acid azotic la p-nitrofenol:
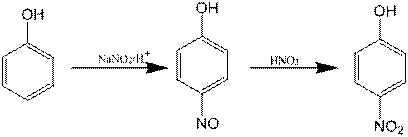
3. Nitrarea fenolului prin tratare directa cu acid azotic:
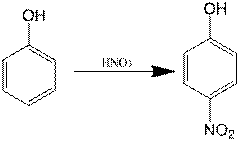
Intrebuintari ale produsului
p-Nitrofenolul are multiple intrebuintari atat in industrie cat si in obtinerea de medicamente :
p-Nitrofenolul poate fi folosit ca materie prima in obtinerea p-aminofenolului (reducere).
Se poate folosi impreuna cu izomerul sau orto in sinteza acidului picric (inainte se folosea foarte mult ca exploziv in proiectilele de artilerie,el este putin sensibil la lovire, dar explodeaza puternic sub actiunea unei capse de fulminat de mercur).
In solutie p-nitrofenolul are o constanta de disociere pKa de 7,08 la 22˚C. Solutia doar de p-nitrofenol este incolora sau galben pal, in timp ce sarea sa fenolica are tendinta de a forma o coloratie galben intens.Aceasta schimbare de culoare face ca acest compus sa fie folosit ca indicator de pH monocromatic,cu virarea coloratiei de la incolor la galben in intervalul de pH 5,6..7,4.
Sarea anhidra de sodiu a p-nitrofenolului de culoare rosie este folosita la determinarea si absorbtia apei.
Esterul mixt al acidului tiofosforic cu p-nitrofenol si etanol se utilizeaza ca insecticid agricol sub numele de "paration" .
p-Nitrofenolul este folosit ca precursor in prepararea fenitidinei si a acetofenitidinei (antitermice).
3.4. Toxicitate
p-Nitrofenolul irita ochii, pielea si caile respiratorii si poate cauza inflamatii ale acestora. Interactioneaza intarziat cu sangele si formeaza methemoglobina care cauzeaza cianoza, confuzie si pierderea cunostiintei.
4. Proiectarea tehnologica
4.1. Caracterizarea materiilor prime
Fenol − conform STAS 6555-87
Formula moleculara: C6H5OH
Formula structurala:
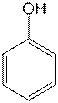
Aspect: cristale albe, prin oxidare galbui-portocalii
Masa moleculara: 94,112
Stare de agregare: solid
Densitate: 1,06 g/cm3
Punct de topire: 40,9˚C
Punct de fierbere: 181,9˚C
Fenolul tehnic de sinteza se livreaza in trei calitati:
Calitatea I II III
Punct de cristalizare 40,6˚C 40,2˚C 39,5˚C
Cloroform − conform STAS 9643-74
Formula moleculara:CHCl3
Formula structurala:
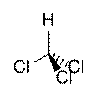
Aspect: lichid incolor
Masa moleculara: 119,38
Stare de agregare:lichid
Densitate: 1,489g/cm3
Punct de topire: -63˚C
Punct de fierbere: 61˚C
Acid azotic − conform SR 447:1995
Formula moleculara: HNO3
Formula structurala:
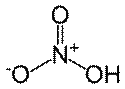
Aspect: lichid galbui-roscat
Masa moleculara: 63,01
Stare de agregare:lichid
Densitate: 1,52g/cm3(pur);1,40g/ cm3(65%)
Punct de topire: -42˚C
Punct de fierbere: 86 ˚C
Sulfat de sodiu − conform STAS 2126-84
Formula moleculara: Na2SO4
Aspect: cristale albe
Masa moleculara: 142.04(anhidru); 268,15(heptahidrat); 322,2(decahidrat)
Stare de agregare:solid
Densitate: 2,68g/cm3
Punct de topire: 884˚C
Acid clorhidric − conform STAS 339-80
Formula moleculara: HCl
Aspect: lichid incolor
Masa moleculara: 36,46
Stare de agregare: lichid
Densitate: 1,16g/ cm3
Punct de topire: -25˚C
Punct de fierbere: 83 - 90 ˚C
Semnificatiile notatiilor:
rezervor CHCl3;
pompa centrifuga;
vas de dozare CHCl3;
dozator pentru solide C6H6OH;
rezervor HNO3;
pompa centrifuga;
vas de dozare HNO3;
reactor de nitrare;
vas de spalare - separare;
vas de separare;
dozator pentru solideNa2SO4;
vas prevazut cu agitator;
pompa centrifuga
vas prevazut cu agitator;
coloana de distilare;
schimbator de caldura - racitor ;
vas de colectare CHCl3;
vas de colectare o-nitrofenol;
rezervor HCl;
pompa centrifuga;
vas de dozare HCl;
dozator de solide Cactiv;
filtru Nutsche;
pompa cu vid;
pompa centrifuga;
reactor precipitare;
filtru Nutsche;
pompa cu vid;
uscator dulap;
R1.R25 - ventile .
4.3. Descrierea procesului tehnologic
La tratarea fenolului cu acid azotic se obtine un amestec de izomeri orto si para ai nitrofenolului conform reactiei:
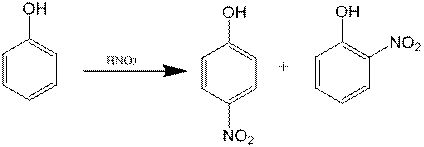
Etapele procesului sunt urmatoarele
1.Dizolvarea
In reactorul de nitrare (8) se introduce cu ajutorul pompei centrifuge (2) o cantitate de cloroform din rezervorul (1) masurata cu vasul de dozare (3) peste care se adauga o cantitate de fenol cu ajutorul dozatorului de solide (4) si se porneste agitarea.
2.Nitrarea
La solutia obtinuta in reactorul (8) se adauga in decurs de o ora o cantitate de acid azotic de concentratie 65% din rezervorul (5) mentinand temperatura sub 15˚C.Dupa adaugarea acidului azotic masa de reactie se mentine inca cateva ore la temperatura sub 15˚C si cu agitare pentru perfectarea reactiei.
3. Diluare - Spalare
Masa de reactie ce contine p-nitrofenolul impreuna materiile prime netransformate si cu produsele secundare rezultate in urma nitrarii se transvazeaza in vasul de spalare-separare (9) prin deschiderea robinetului R6,iar peste aceasta se adauga 1000 L apa rece pentru diluarea excesului de acid azotic.Se lasa in repaus pentru decantare dupa care se scoate stratul apos superior prin deschiderea robinetului R8,el fiind depozitat in vasul de separare (10) .Peste stratul cloroformic ramas in vasul (9) se adauga inca 1000 L apa rece cu care se procedeaza la fel.
4.Extractia
Peste cele doua ape acide reunite in vasul (10) se aduga o cantitate de cloroform pentru a extrage micile cantitati de nitrofenoli solubilizati.Dupa separare apele acide se arunca iar extrasul cloroformic se reuneste cu solutia cloroformica principala in vasul (12).
5. Uscarea
Solutia cloroformica se usuca prin adaugare de sulfat de sodiu anhidru care aditioneaza apa rezultand sulfatul de sodiu heptahidrat. Rezulta un reziduu uleios galben rosiatic care este trecut in vasul (14).
6.Distilarea
Vasul (14) este incalzit cu abur pentru a realiza distilarea cloroformului care este trecut prin coloana de distilare (5) prin schimbatorul de caldura - racitor (16) ajungand in vasul de colectare (17).
7. Antrenarea cu vapori
Dupa distilarea cloroformului amestecul ce contine p-nitrofenolul este antrenat cu vapori de apa pentru separarea o-nitrofenolului care este antrenabil cu vapori de apa si este colectat in vasul de colectare (18) .
8.Fierberea
Reziduul ramas dupa antrenarea o-nitrofenolului cu vapori de apa si care contine p-nitrofenolul impreuna cu ceva dinitroderivat si rasini se incalzeste la fierbere cu acid clorhidric 2% si Cactiv.
9. Precipitare
Dupa fierbere amestecul este lasat sa se raceasca pana la 80˚C cand precipita mici cantitati de produse secundare separate pe filtrul Nutsche (23) peste care se adauga o cantitate de acid clorhidric pentru a nu pierde p-nitrofenolul.
Filtratele fierbinti si limpezi se trec in reactorul de precipitare 26 unde se racesc sub agitare dupa care sunt trecute pe filtrul Nutsche (27) unde precipita p-nitrofenolul care se filtreaza si se spala cu apa rece pentru indepartarea aciditatii.
10. Uscarea
Precipitatul umed se trece in uscatorul dulap (29) unde se usuca la 60 ˚C rezultand produsul finit: p-nitrofenolul.
Copyright © 2024 - Toate drepturile rezervate